Clear Sky Science · pt
O TNF alfa revela disfunção da via malato‑aspartato enteral conectando a doença de Parkinson e a inflamação intestinal
O elo oculto entre o intestino e o Parkinson
Muitas pessoas com doença de Parkinson percebem problemas no banheiro muito antes de as mãos começarem a tremer. Prisão de ventre e inchaço podem surgir anos antes dos problemas de movimento, sugerindo que o “segundo cérebro” do intestino — o sistema nervoso entérico — pode estar envolvido precocemente na doença. Este estudo faz uma pergunta simples, porém urgente: como a inflamação intestinal perturba esses nervos intestinais, e essa perturbação poderia contribuir para impulsionar o Parkinson e outros distúrbios intestinais?
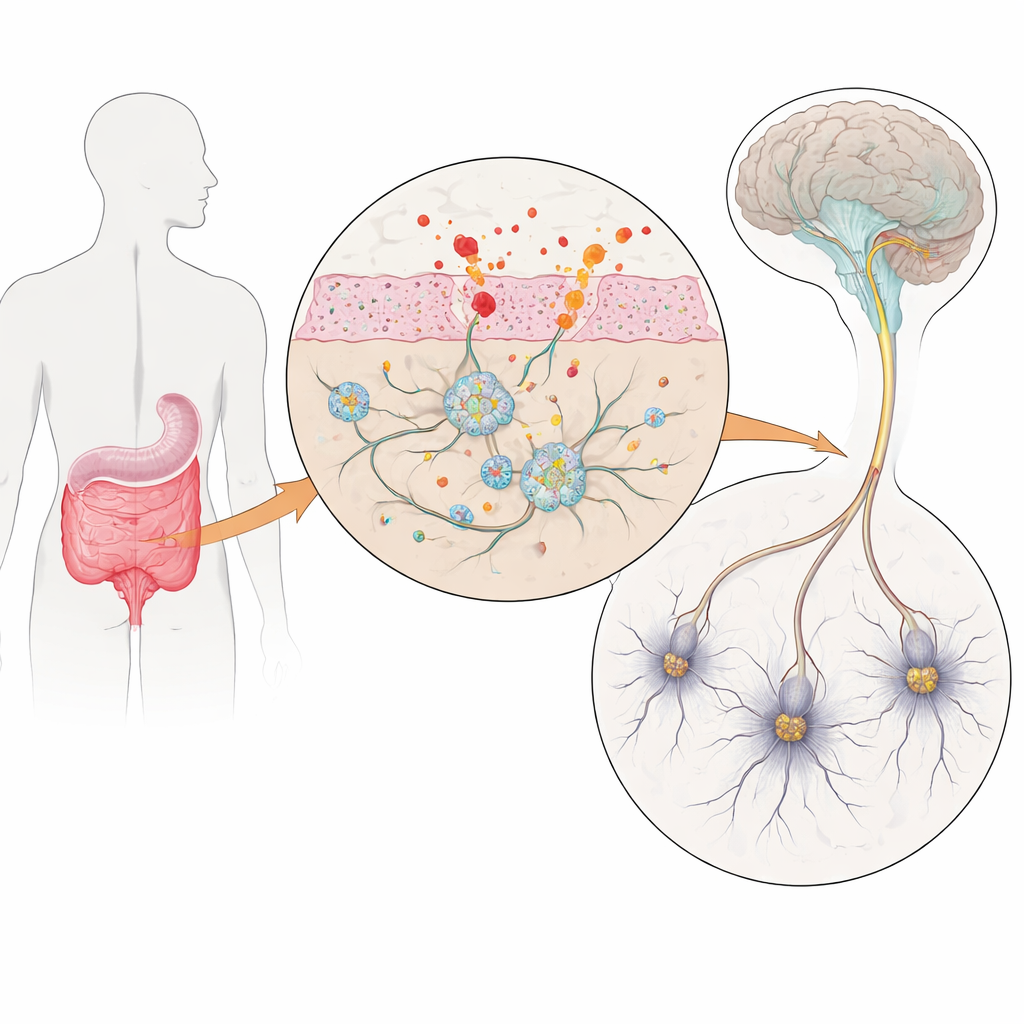
Nervos intestinais em cultura
Para investigar isso, os pesquisadores construíram um modelo laboratorial de nervos intestinais humanos usando células-tronco pluripotentes induzidas — células adultas reprogramadas de volta a um estado semelhante ao de células-tronco e então direcionadas para se tornarem neurônios entéricos e células de suporte chamadas glia. Algumas linhagens de células-tronco carregavam três cópias do gene da alfa‑sinucleína, uma proteína que se agrega de forma anômala na doença de Parkinson, enquanto linhagens controle pareadas tinham dosagem genética normal. Após cerca de dez semanas de desenvolvimento guiado, essas culturas continham uma mistura rica de neurônios e glia com características intestinais que se assemelhavam de perto à diversidade celular encontrada em intestinos humanos reais. Crucialmente, as células com fenótipo semelhante ao do Parkinson produziram alfa‑sinucleína em excesso, criando um modelo controlável de doença inicial no intestino.
Uma vulnerabilidade pré‑existente na energia celular
Mesmo antes de qualquer inflamação ser aplicada, células com excesso de alfa‑sinucleína exibiam sinais generalizados de estresse em seus sistemas energéticos. Perfilamento genético detalhado em célula única revelou perturbações em vias que lidam com gorduras, colesterol e blocos de construção essenciais para o combustível celular. A microscopia mostrou que suas mitocôndrias — as pequenas usinas dentro das células — eram em menor número, menores e mais fragmentadas. A comunicação entre neurônios e glia também foi reconfigurada, com vias de sinalização relacionadas ao estresse ganhando destaque. Em conjunto, esses achados desenharam o retrato de células nervosas intestinais que, embora externamente semelhantes a células saudáveis, já viviam perto do limite em termos de energia e resiliência.
A inflamação desequilibra a balança
A equipe então introduziu fator de necrose tumoral alfa (TNF), um importante sinal inflamatório que está elevado tanto na doença de Parkinson quanto em transtornos intestinais, como a colite ulcerativa. O TNF teve um impacto marcadamente diferente nas duas culturas. Nas células com fenótipo de Parkinson, o TNF aumentou os níveis de alfa‑sinucleína tanto em neurônios quanto em glia e elevou o contato físico da proteína com as mitocôndrias, uma combinação associada a danos e estresse oxidativo. Registros elétricos mostraram que redes controle saudáveis podiam aumentar sua atividade após o TNF, mas as redes semelhantes ao Parkinson permaneceram lentas, revelando uma capacidade prejudicada de se adaptar ao desafio inflamatório. Ao nível molecular, medidas de proteínas e metabólitos convergiram para um sistema chave de transferência de energia chamado shuttle malato–aspartato, que normalmente transporta poder redutor para dentro das mitocôndrias. Sob TNF, esse shuttle enfraqueceu especificamente nas células com fenótipo de Parkinson, esgotando moléculas essenciais e forçando as células a recorrerem à queima de glutamina como combustível de emergência.
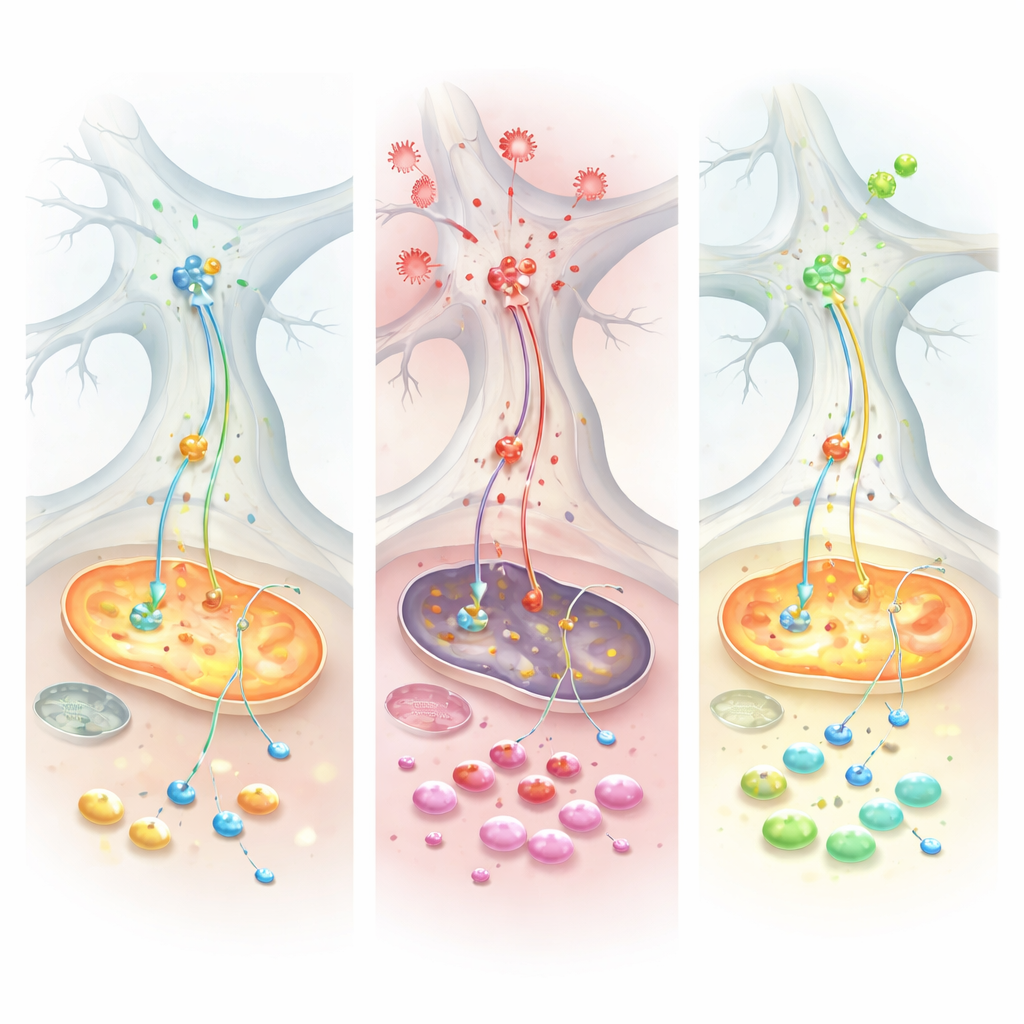
Uma potencial resgate e pistas vindas de pacientes
Quando os pesquisadores trataram as culturas com Chicago‑Sky‑Blue 6B, um composto que modula o manejo do glutamato, o quadro mudou. O fármaco restaurou várias medidas da respiração mitocondrial, reduziu a dependência anômala de glutamina e normalizou parcialmente o equilíbrio energético nas células estressadas. Para testar se o mesmo tema metabólico aparece em pessoas reais, a equipe analisou tecido intestinal de pacientes com colite ulcerativa e grandes conjuntos públicos de dados de expressão gênica. Em múltiplas coortes, encontraram atividade reduzida de enzimas que sustentam o shuttle malato–aspartato, juntamente com aumento da alfa‑sinucleína em tecido intestinal inflamado. Pacientes que responderam bem à terapia anti‑TNF tendiam a recuperar a expressão dessas enzimas energéticas e apresentavam níveis mais baixos de alfa‑sinucleína, sugerindo que o padrão inflamatório‑metabólico observado nas culturas laboratoriais se reflete na doença humana.
Por que isso importa para os pacientes
Em resumo, o estudo sugere que a sobrecarga de alfa‑sinucleína torna os nervos intestinais metabolicamente frágeis, e a inflamação intestinal, por meio de sinais como o TNF, explora essa fraqueza. Ao prejudicar um shuttle energético chave e empurrar as células para um modo de combustível reserva, a inflamação aumenta o estresse oxidativo, favorece a associação da alfa‑sinucleína com as mitocôndrias e compromete a função normal dos neurônios intestinais. Como assinaturas similares são vistas tanto em modelos de Parkinson quanto em intestinos humanos inflamados, o trabalho aponta para um ponto fraco metabólico compartilhado que poderia ser alvo de terapias futuras. Modular o metabolismo do glutamato e da glutamina — como faz o Chicago‑Sky‑Blue 6B neste estudo — surge como uma estratégia promissora para proteger o sistema nervoso do intestino, potencialmente aliviando sintomas como a prisão de ventre e talvez retardando os estágios iniciais do Parkinson e de outras condições intestinais inflamatórias.
Citação: Ghirotto, B., Gonçalves, L.E., Ruder, V. et al. TNF alpha unmasks enteric malate aspartate shuttle dysfunction bridging Parkinson disease and intestinal inflammation. Nat Commun 17, 3217 (2026). https://doi.org/10.1038/s41467-026-71317-y
Palavras-chave: Doença de Parkinson, sistema nervoso entérico, inflamação intestinal, metabolismo mitocondrial, alfa‑sinucleína