Clear Sky Science · sv
TNF alfa blottlägger dysfunktion i enterisk malat‑aspartat‑shuttle som länkar Parkinsons sjukdom och tarminflammation
Den dolda länken mellan tarmen och Parkinsons
Många personer med Parkinsons sjukdom märker först problem i toaletten långt innan händerna börjar darra. Förstoppning och uppblåsthet kan uppträda år innan rörelsestörningarna, vilket antyder att tarmens eget ”andra hjärna” – det enteriska nervsystemet – kan vara involverat tidigt i sjukdomen. Denna studie ställer en enkel men angelägen fråga: hur stör inflammation i tarmen dessa tarmnerver, och kan den störningen bidra till att driva Parkinsons och andra tarmsjukdomar?
Tarmnerver i ett laboratorium
För att undersöka detta byggde forskarna en laboratoriemodell av mänskliga tarmnerver med hjälp av inducerade pluripotenta stamceller – vuxna celler som omprogrammerats till ett stamliknande tillstånd och sedan styrts att bli enteriska neuroner och stödjeceller som kallas gliaceller. Några stamcellslinjer bar tre kopior av genen för alfa‑synuklein, ett protein som klumpar sig onormalt vid Parkinsons sjukdom, medan matchade kontrollinjer hade normal genmängd. Efter ungefär tio veckors styrd utveckling innehöll dessa kulturer en rik blandning av tarmliknande neuroner och gliaceller som nära efterliknade den cellulära mångfald som finns i verkliga mänskliga tarmar. Viktigt var att Parkinson‑lika celler producerade extra alfa‑synuklein, vilket skapade en kontrollerbar modell av tidig sjukdom i tarmen.
En förinställd sårbarhet i cellernas energi
Redan innan någon inflammation tillsattes visade celler med extra alfa‑synuklein utbredda tecken på belastning i sina energisystem. Detaljerad enkelcellsgenprofilering avslöjade störningar i vägar som hanterar fetter, kolesterol och viktiga byggstenar för cellbränsle. Mikroskopi visade att deras mitokondrier – cellernas små kraftverk – var färre, mindre och mer fragmenterade. Kommunikationsmönstren mellan neuroner och gliaceller var också omkopplade, med stressrelaterade signalvägar som blev mer framträdande. Tillsammans målade dessa fynd bilden av tarmnervceller som utåt sett liknar friska celler men redan lever nära gränsen när det gäller energi och motståndskraft.
Inflammation rubbar balansen
Teamet tillsatte sedan tumörnekrosfaktor alfa (TNF), en huvudsignal för inflammation som är förhöjd både vid Parkinsons och vid tarmsjukdomar som ulcerös kolit. TNF hade en slående annorlunda effekt på de två typerna av kulturer. I de Parkinson‑lika cellerna ökade TNF nivåerna av alfa‑synuklein i både neuroner och gliaceller och ökade proteinets fysiska kontakt med mitokondrierna — en kombination som förknippas med skada och oxidativ stress. Elektriska mätningar visade att friska kontrollnätverk kunde öka sin aktivitet efter TNF, men de Parkinson‑lika nätverken förblev slöa, vilket visade en nedsatt förmåga att anpassa sig till inflammatorisk påfrestning. På molekylär nivå konvergerade protein‑ och metabolitmätningar mot ett nyckelsystem för energitransfer kallat malat–aspartat‑shuttle, som normalt för över reduktionskraft till mitokondrierna. Under TNF sviktade denna shuttle specifikt i de Parkinson‑lika cellerna, vilket tömde viktiga molekyler och tvingade cellerna att förlita sig på att bränna glutamin som ett nödbränsle.
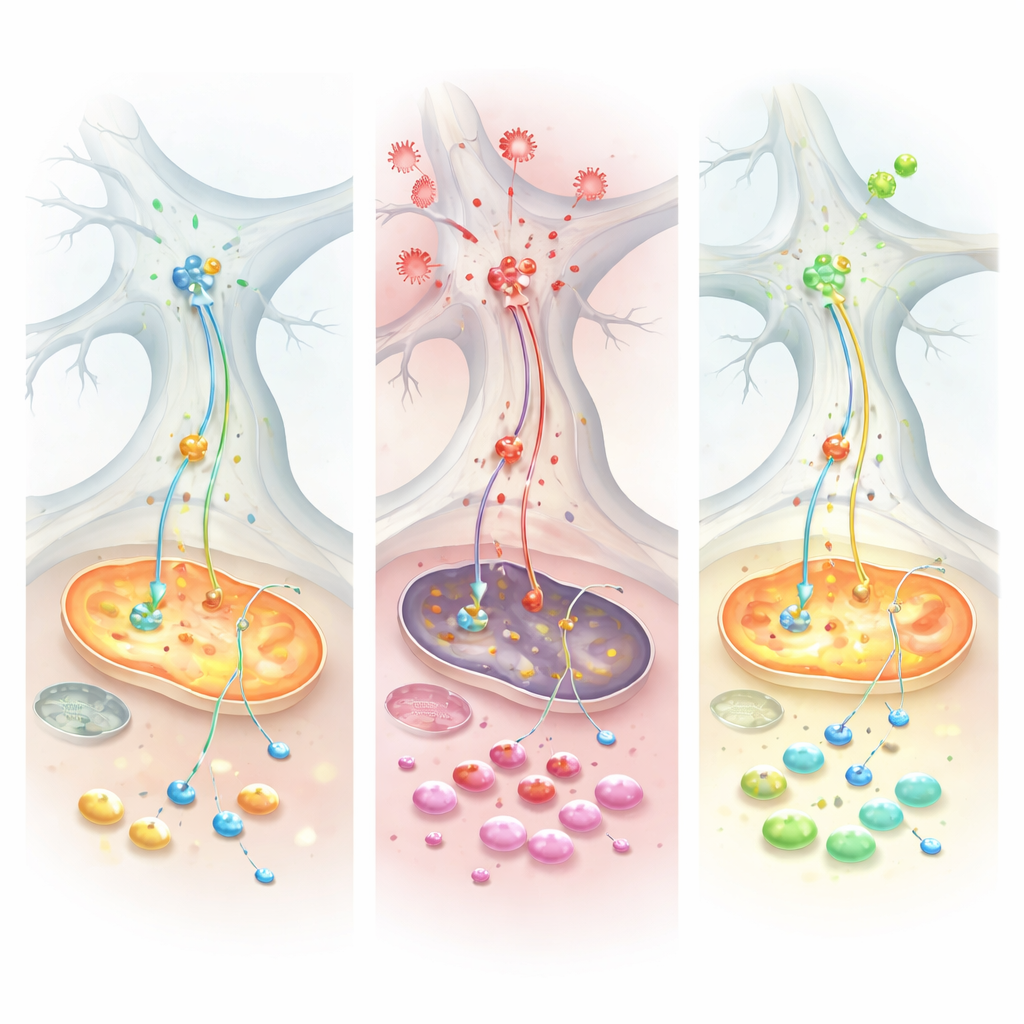
En möjlig räddning och ledtrådar från patienter
När forskarna behandlade kulturerna med Chicago‑Sky‑Blue 6B, en förening som påverkar glutamathantering, förändrades bilden. Läkemedlet återställde flera mått på mitokondriell andning, minskade det onormala beroendet av glutamin och normaliserade delvis energibalansen i de stressade cellerna. För att testa om samma metaboliska tema förekom hos riktiga människor analyserade teamet tarmvävnad från patienter med ulcerös kolit och stora offentliga genuttrycksdatamängder. I flera kohorter fann de minskad aktivitet i enzymer som driver malat–aspartat‑shuttlen, tillsammans med ökat alfa‑synuklein i inflammerad tarmvävnad. Patienter som svarade väl på anti‑TNF‑behandling återfick ofta uttryck av dessa energienzymer och visade lägre nivåer av alfa‑synuklein, vilket tyder på att det inflammatoriska‑metaboliska mönstret som sågs i laboratoriekulturerna speglas i mänsklig sjukdom.
Varför detta är viktigt för patienter
Enkelt uttryckt tyder studien på att en överbelastning av alfa‑synuklein gör tarmnerver metaboliskt sårbara, och att tarminflammation, genom signaler som TNF, utnyttjar denna svaghet. Genom att försvaga en nyckel‑energishuttle och pressa cellerna in i ett ansträngt reservbränsleläge ökar inflammationen oxidativ stress, uppmuntrar alfa‑synuklein att associera med mitokondrier och undergräver tarmnervens normala funktion. Eftersom liknande signaturer ses både i Parkinsonsmodeller och i inflammerade mänskliga tarmar pekar arbetet på en gemensam metabolisk svag punkt som kan riktas av framtida terapier. Att modulera glutamat‑ och glutaminmetabolism — som Chicago‑Sky‑Blue 6B gör i denna studie — framstår som en lovande strategi för att skydda tarmens nervsystem, potentiellt lindra symtom som förstoppning och kanske bromsa de tidigaste skedena av Parkinsons och andra inflammatoriska tarmsjukdomar.
Citering: Ghirotto, B., Gonçalves, L.E., Ruder, V. et al. TNF alpha unmasks enteric malate aspartate shuttle dysfunction bridging Parkinson disease and intestinal inflammation. Nat Commun 17, 3217 (2026). https://doi.org/10.1038/s41467-026-71317-y
Nyckelord: Parkinsons sjukdom, enteriska nervsystemet, tarminflammation, mitokondriell metabolism, alfa‑synuklein