Clear Sky Science · pl
TNF alfa ujawnia dysfunkcję jelitowego przenośnika jabłczan‑asparaginianu łączącą chorobę Parkinsona z zapaleniem jelit
Ukryte powiązanie między jelitami a chorobą Parkinsona
Wiele osób z chorobą Parkinsona zauważa problemy w toalecie na długo przed pojawieniem się drżeń rąk. Zaparcia i wzdęcia mogą występować na wiele lat przed zaburzeniami ruchu, co sugeruje, że „drugie mózg” jelit — jelitowy układ nerwowy — może być zaangażowany we wczesne stadia choroby. W tym badaniu zadano proste, ale ważne pytanie: w jaki sposób zapalenie w jelicie zaburza te nerwy jelitowe i czy to zaburzenie może przyczyniać się do rozwoju choroby Parkinsona oraz innych schorzeń jelit?
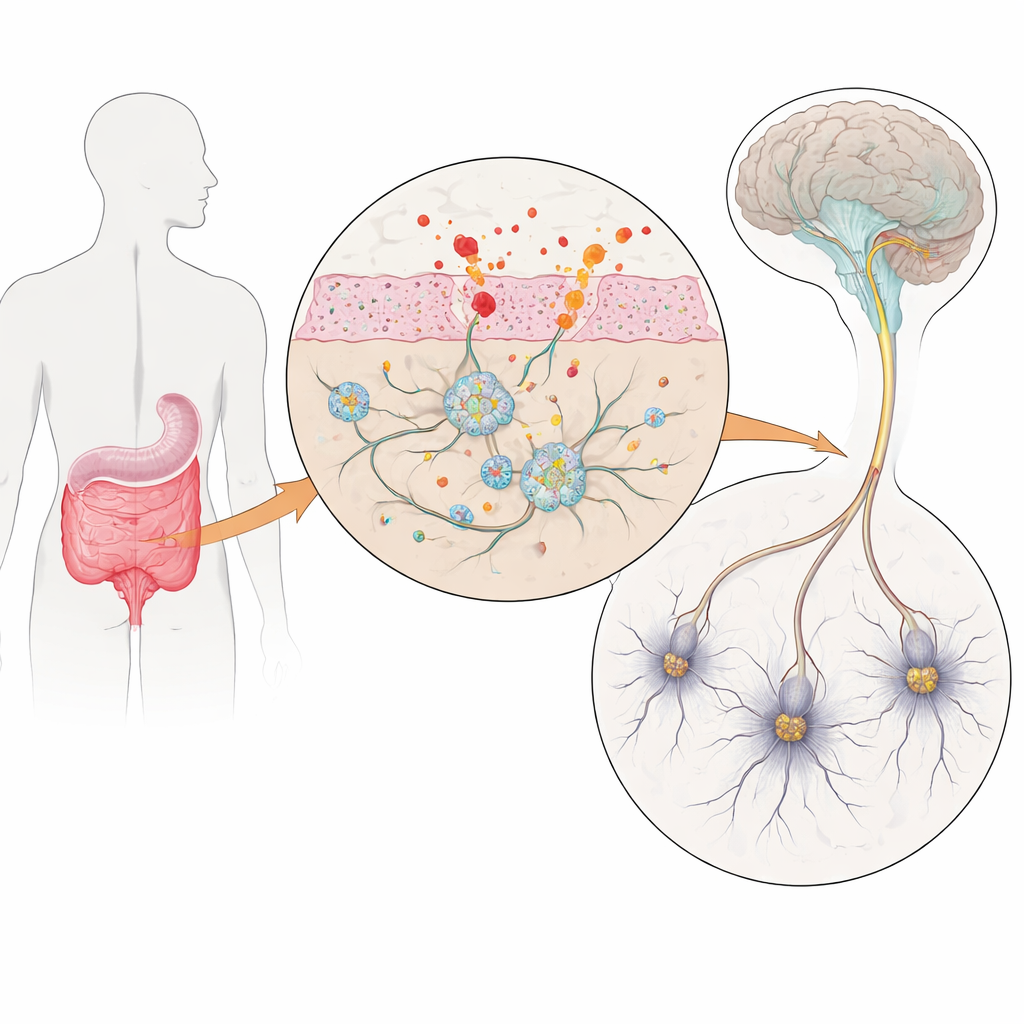
Nerwy jelitowe w hodowli
Aby to zbadać, naukowcy zbudowali laboratoryjny model ludzkich nerwów jelitowych, wykorzystując indukowane pluripotentne komórki macierzyste — komórki dorosłe przeprogramowane do stanu przypominającego komórki macierzyste, a następnie ukierunkowane, by stać się neuronami jelitowymi i komórkami wspierającymi zwanymi glejem. Niektóre linie komórkowe miały trzy kopie genu dla alfa‑synukleiny, białka, które nieprawidłowo się agreguje w chorobie Parkinsona, podczas gdy linie kontrolne miały normalną liczbę kopii genu. Po około dziesięciu tygodniach ukierunkowanego rozwoju hodowle zawierały bogatą mieszankę neuronów i gleju przypominających te z prawdziwego ludzkiego jelita. Co istotne, komórki przypominające stan Parkinsona produkowały dodatkową alfa‑synukleinę, tworząc sterowalny model wczesnej choroby w jelicie.
Wstępna wrażliwość w systemie energetycznym komórek
Nawet zanim dodano jakiekolwiek zapalenie, komórki z nadmiarem alfa‑synukleiny wykazywały rozległe objawy przeciążenia systemów energetycznych. Szczegółowe profilowanie genów na poziomie pojedynczych komórek ujawniło zaburzenia w szlakach zajmujących się tłuszczami, cholesterolem i kluczowymi składnikami budulcowymi paliwa komórkowego. Mikroskopia wykazała, że ich mitochondria — małe elektrownie w komórkach — były mniej liczne, mniejsze i bardziej pofragmentowane. Komunikacja między neuronami a glejem również uległa przestawieniu, a szlaki sygnalizacji związane ze stresem stały się bardziej widoczne. Razem te ustalenia naszkicowały obraz komórek nerwowych jelita, które z zewnątrz wyglądają podobnie do zdrowych, ale od strony energetycznej i odpornościowej żyją już blisko krawędzi.
Zapalenie przechyla szalę
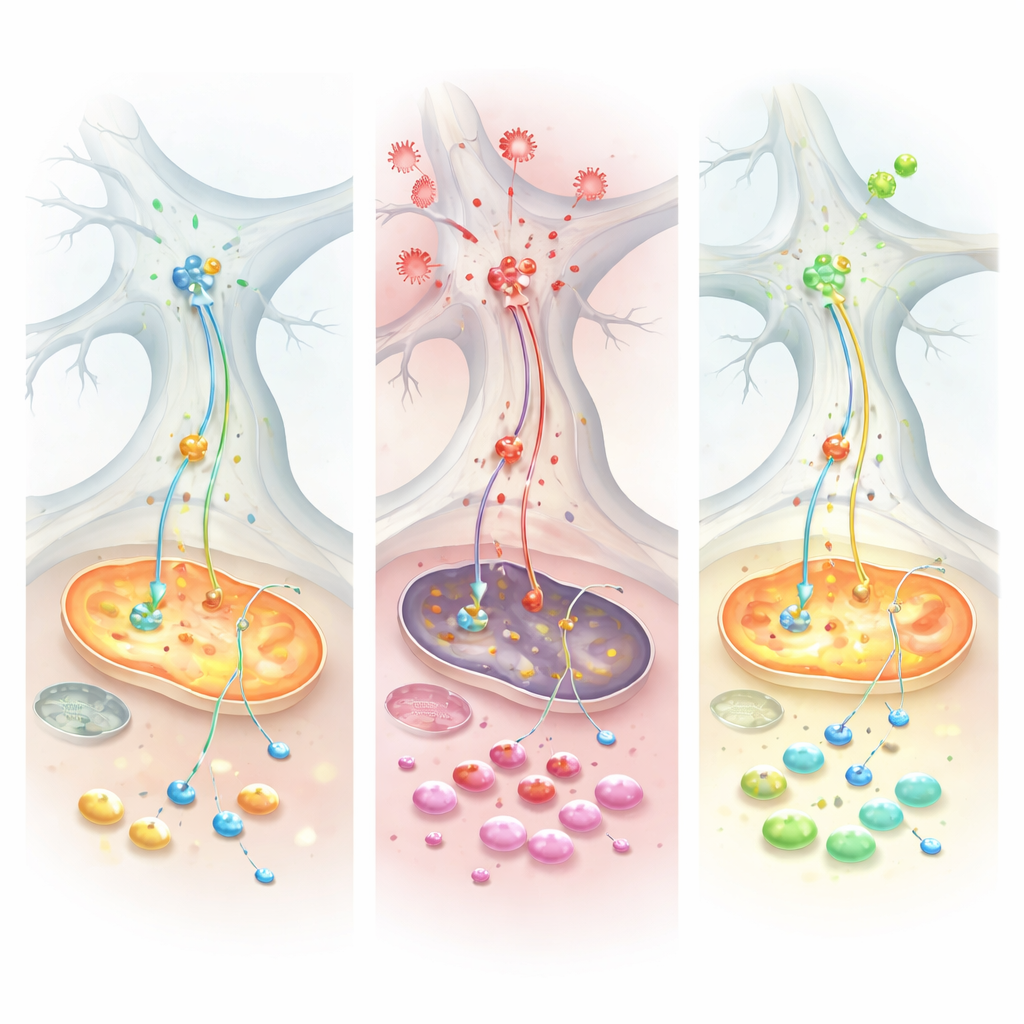
Zespół następnie wprowadził czynnik martwicy nowotworów alfa (TNF), główny sygnał zapalny podwyższony zarówno w chorobie Parkinsona, jak i w zaburzeniach jelit, takich jak wrzodziejące zapalenie jelita grubego. TNF wywołał wyraźnie różny wpływ na oba typy hodowli. W komórkach przypominających Parkinsona TNF zwiększył poziomy alfa‑synukleiny zarówno w neuronach, jak i w gleju oraz nasilił fizyczne kontaktowanie tego białka z mitochondriami — kombinację związaną ze uszkodzeniem i stresem oksydacyjnym. Nagrania elektryczne pokazały, że zdrowe sieci kontrolne potrafiły zwiększyć swoją aktywność po ekspozycji na TNF, podczas gdy sieci przypominające Parkinsona pozostały ospałe, ujawniając upośledzoną zdolność do adaptacji na wyzwanie zapalne. Na poziomie molekularnym pomiary białek i metabolitów zbiegały się na kluczowym systemie transferu energii zwanym przenośnikiem jabłczan–asparaginian, który normalnie przemieszcza siłę redukującą do mitochondriów. Pod wpływem TNF ten przenośnik zawodził specyficznie w komórkach przypominających Parkinsona, wyczerpując niezbędne cząsteczki i zmuszając komórki do polegania na spalaniu glutaminy jako paliwie awaryjnym.
Potencjalna interwencja i wskazówki od pacjentów
Gdy badacze potraktowali hodowle związkiem Chicago‑Sky‑Blue 6B, modulującym gospodarowanie glutaminianem, sytuacja uległa zmianie. Lek przywrócił kilka miar „oddychania” mitochondrialnego, zmniejszył nieprawidłowe uzależnienie od glutaminy i częściowo znormalizował równowagę energetyczną w zestresowanych komórkach. Aby sprawdzić, czy ten sam motyw metaboliczny pojawia się u ludzi, zespół przeanalizował tkankę jelitową pacjentów z wrzodziejącym zapaleniem jelita grubego oraz duże publiczne zestawy danych ekspresji genów. W wielu kohortach stwierdzono zmniejszoną aktywność enzymów napędzających przenośnik jabłczan–asparaginian, obok zwiększonej alfa‑synukleiny w zapalnej tkance jelitowej. Pacjenci dobrze reagujący na terapię przeciw‑TNF mieli tendencję do odzyskiwania ekspresji tych enzymów energetycznych i niższych poziomów alfa‑synukleiny, co sugeruje, że wzorzec zapalno‑metaboliczny obserwowany w hodowlach laboratoryjnych ma odzwierciedlenie w chorobie u ludzi.
Dlaczego to ma znaczenie dla pacjentów
Mówiąc wprost, badanie sugeruje, że nadmiar alfa‑synukleiny czyni nerwy jelitowe metabolicznie kruche, a zapalenie jelit, za pośrednictwem sygnałów takich jak TNF, wykorzystuje tę słabość. Paraliżując kluczowy przenośnik energii i popychając komórki w tryb awaryjnego spalania paliwa, zapalenie zwiększa stres oksydacyjny, sprzyja łączeniu się alfa‑synukleiny z mitochondriami i podważa normalne funkcje neuronów jelitowych. Ponieważ podobne sygnatury widoczne są zarówno w modelach Parkinsona, jak i we wrażliwej, zapalnej tkance jelitowej u ludzi, praca wskazuje na wspólny metaboliczny punkt słabości, który można byłoby celować w przyszłych terapiach. Modulacja metabolizmu glutaminianu i glutaminy — tak jak robi to Chicago‑Sky‑Blue 6B w tym badaniu — pojawia się jako obiecująca strategia ochrony układu nerwowego jelit, potencjalnie łagodząc objawy takie jak zaparcia i być może spowalniając najwcześniejsze etapy choroby Parkinsona oraz innych zapalnych schorzeń jelit.
Cytowanie: Ghirotto, B., Gonçalves, L.E., Ruder, V. et al. TNF alpha unmasks enteric malate aspartate shuttle dysfunction bridging Parkinson disease and intestinal inflammation. Nat Commun 17, 3217 (2026). https://doi.org/10.1038/s41467-026-71317-y
Słowa kluczowe: choroba Parkinsona, układ nerwowy jelit, zapalenie jelit, metabolizm mitochondrialny, alfa-synukleina