Clear Sky Science · de
TNF-alpha legt eine Dysfunktion der enterischen Malat-Aspartat-Shuttle offen, die Morbus Parkinson und Darmentzündung verbindet
Die verborgene Verbindung zwischen Darm und Parkinson
Viele Menschen mit Morbus Parkinson bemerken Probleme auf der Toilette lange bevor ihre Hände zu zittern beginnen. Verstopfung und Blähungen können Jahre vor motorischen Symptomen auftreten und deuten darauf hin, dass das „zweite Gehirn“ des Darms – das enterische Nervensystem – früh in der Krankheit beteiligt sein könnte. Diese Studie stellt eine einfache, aber drängende Frage: Wie stört Entzündung im Darm diese Darmnerven, und könnte diese Störung dazu beitragen, Parkinson und andere Darmkrankheiten voranzutreiben?
Darmnerven im Reagenzglas
Um das zu untersuchen, bauten die Forschenden ein Labor‑Modell menschlicher Darmnerven mithilfe induzierter pluripotenter Stammzellen – umprogrammierte erwachsene Zellen, die wieder in einen stammesähnlichen Zustand zurückversetzt und dann zu enterischen Neuronen und Stützzellen (Gliazellen) differenziert wurden. Einige Stammzelllinien trugen drei Kopien des Gens für Alpha‑Synuclein, ein Protein, das bei Morbus Parkinson abnorm aggregiert, während passende Kontrolllinien die normale Genkopienzahl hatten. Nach etwa zehn Wochen gesteuerter Entwicklung enthielten diese Kulturen eine reiche Mischung darmähnlicher Neuronen und Gliazellen, die der zellulären Vielfalt im menschlichen Darm sehr ähnlich war. Entscheidend produzierten die Parkinson‑ähnlichen Zellen zusätzliches Alpha‑Synuclein und schufen so ein kontrollierbares Modell früher krankheitsbezogener Veränderungen im Darm.
Eine vorab bestehende Verwundbarkeit der Zellenergie
Sogar bevor irgendeine Entzündung hinzugefügt wurde, zeigten Zellen mit erhöhtem Alpha‑Synuclein weit verbreitete Hinweise auf Belastung ihres Energiestoffwechsels. Detaillierte Einzelzell‑Genanalysen offenbarten Störungen in Wegen, die Fette, Cholesterin und zentrale Bausteine für Zellenergie verarbeiten. Die Mikroskopie zeigte, dass ihre Mitochondrien – die winzigen Kraftwerke in Zellen – seltener, kleiner und stärker fragmentiert waren. Die Kommunikation zwischen Neuronen und Glia war ebenfalls umgebaut, wobei stressbezogene Signalwege prominenter wurden. Zusammen zeichneten diese Befunde das Bild von Darmnervenzellen, die äußerlich gesunden Zellen ähneln, aber energie‑ und widerstandsfähigkeitsmäßig bereits nahe an der Belastungsgrenze leben.
Entzündung kippt die Balance
Das Team setzte dann Tumor‑Nekrose‑Faktor alpha (TNF) zu, ein wichtiges entzündliches Signal, das sowohl bei Morbus Parkinson als auch bei Darmerkrankungen wie Colitis ulcerosa erhöht ist. TNF hatte einen auffallend unterschiedlichen Einfluss auf die beiden Kulturtypen. In den Parkinson‑ähnlichen Zellen erhöhte TNF die Alpha‑Synuclein‑Spiegel in Neuronen und Glia und verstärkte die physische Nähe dieses Proteins zu Mitochondrien – eine Kombination, die mit Schäden und oxidativem Stress einhergeht. Elektrische Messungen zeigten, dass gesunde Kontrollnetzwerke ihre Aktivität nach TNF hochfahren konnten, die Parkinson‑ähnlichen Netzwerke blieben hingegen träge und offenbarten eine eingeschränkte Fähigkeit, sich an entzündliche Belastung anzupassen. Auf molekularer Ebene konzentrierten sich Protein‑ und Metabolitmessungen auf ein zentrales Energietransfersystem, das Malat–Aspartat‑Shuttle, das normalerweise Reduktionskraft in die Mitochondrien transportiert. Unter TNF versagte dieses Shuttle speziell in den Parkinson‑ähnlichen Zellen, entleerte essenzielle Moleküle und zwang die Zellen, als Notfallbrennstoff auf den Abbau von Glutamin zurückzugreifen.
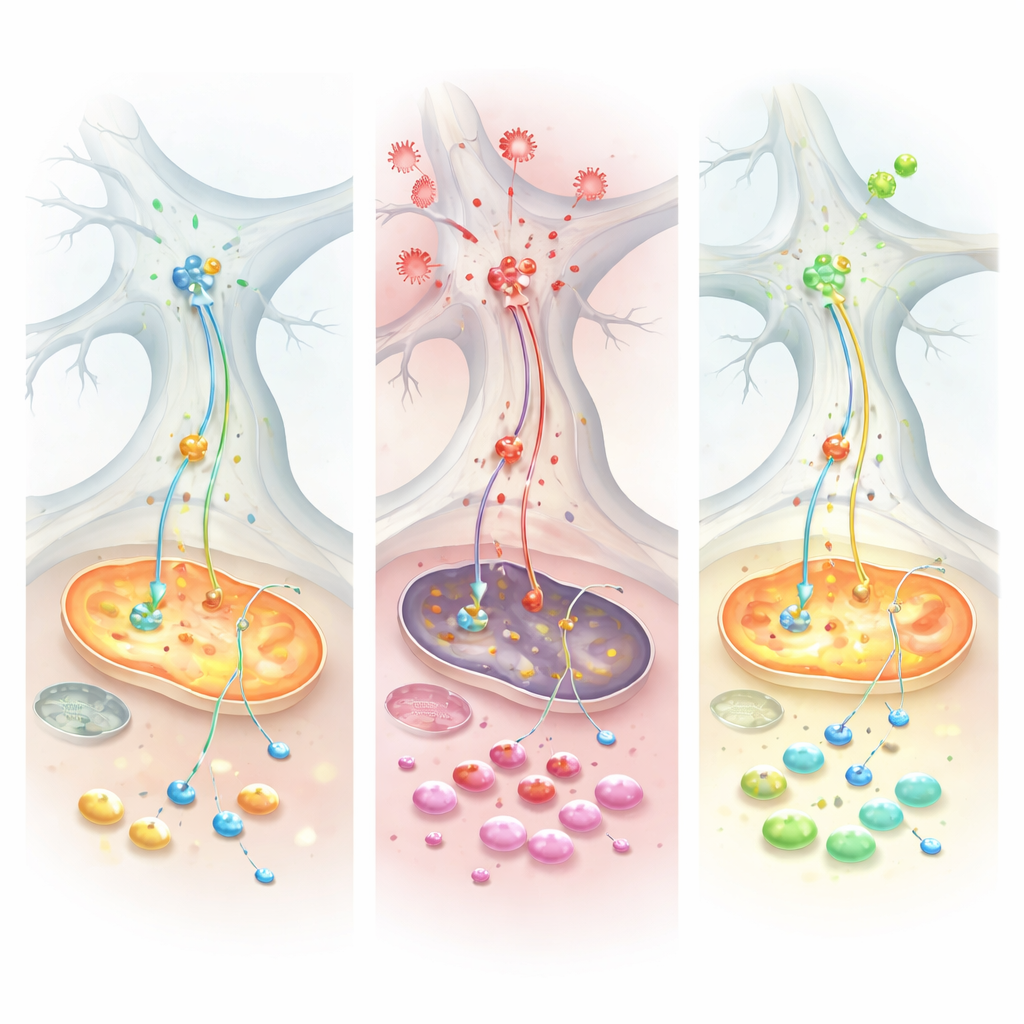
Eine mögliche Rettung und Hinweise aus Patientendaten
Als die Forschenden die Kulturen mit Chicago‑Sky‑Blue 6B behandelten, einer Verbindung, die den Glutamathaushalt moduliert, änderte sich das Bild. Der Wirkstoff stellte mehrere Maße der mitochondrialen Atmung wieder her, reduzierte die abnormale Abhängigkeit von Glutamin und normalisierte teilweise das Energiegleichgewicht in den gestressten Zellen. Um zu prüfen, ob dasselbe metabolische Muster auch bei Menschen vorkommt, analysierte das Team Darmgewebe von Patienten mit Colitis ulcerosa und große öffentliche Genexpressions‑Datensätze. In mehreren Kohorten fanden sie eine verringerte Aktivität von Enzymen, die das Malat–Aspartat‑Shuttle antreiben, zusammen mit erhöhtem Alpha‑Synuclein im entzündeten Darmgewebe. Patienten, die gut auf eine Anti‑TNF‑Therapie ansprachen, zeigten tendenziell eine Wiederherstellung der Expression dieser Energie‑Enzyme und niedrigere Alpha‑Synuclein‑Werte, was darauf hindeutet, dass das im Labor beobachtete entzündlich‑metabolische Muster auch in der menschlichen Krankheit widergespiegelt wird.
Warum das für Patienten wichtig ist
Kurz gesagt legt die Studie nahe, dass Alpha‑Synuclein‑Überladung Darmnerven metabolisch verwundbar macht und dass intestinale Entzündung über Signale wie TNF diese Schwäche ausnutzt. Indem sie ein zentrales Energieshuttle lahmlegt und die Zellen in einen belasteten Backup‑Brennstoffmodus zwingt, erhöht Entzündung den oxidativen Stress, fördert die Assoziation von Alpha‑Synuclein mit Mitochondrien und untergräbt die normale Funktion der Darmneurone. Da ähnliche Signaturen sowohl in Parkinson‑Modellen als auch in entzündetem menschlichem Darmgewebe gesehen werden, weist die Arbeit auf eine gemeinsame metabolische Schwachstelle hin, die therapeutisch angegangen werden könnte. Die Modulation von Glutamat‑ und Glutamin‑Stoffwechsel – wie durch Chicago‑Sky‑Blue 6B in dieser Studie gezeigt – erscheint als vielversprechende Strategie, das enterische Nervensystem zu schützen, möglicherweise Symptome wie Verstopfung zu lindern und früheste Stadien von Morbus Parkinson und anderen entzündlichen Darmerkrankungen zu verlangsamen.
Zitation: Ghirotto, B., Gonçalves, L.E., Ruder, V. et al. TNF alpha unmasks enteric malate aspartate shuttle dysfunction bridging Parkinson disease and intestinal inflammation. Nat Commun 17, 3217 (2026). https://doi.org/10.1038/s41467-026-71317-y
Schlüsselwörter: Morbus Parkinson, enterisches Nervensystem, Darmentzündung, mitochondriale Stoffwechsel, Alpha-Synuclein