Clear Sky Science · fr
Le TNF alpha révèle un dysfonctionnement de la navette malate‑aspartate entérique reliant la maladie de Parkinson et l’inflammation intestinale
Le lien caché entre l’intestin et la maladie de Parkinson
Beaucoup de personnes atteintes de la maladie de Parkinson remarquent d’abord des troubles digestifs bien avant que leurs mains ne commencent à trembler. La constipation et les ballonnements peuvent apparaître des années avant les troubles moteurs, ce qui suggère que le « second cerveau » de l’intestin – le système nerveux entérique – pourrait être impliqué dès les stades précoces de la maladie. Cette étude pose une question simple mais pressante : comment l’inflammation intestinale perturbe‑t‑elle ces nerfs entériques, et cette perturbation pourrait‑elle contribuer à la maladie de Parkinson et à d’autres troubles intestinaux ?
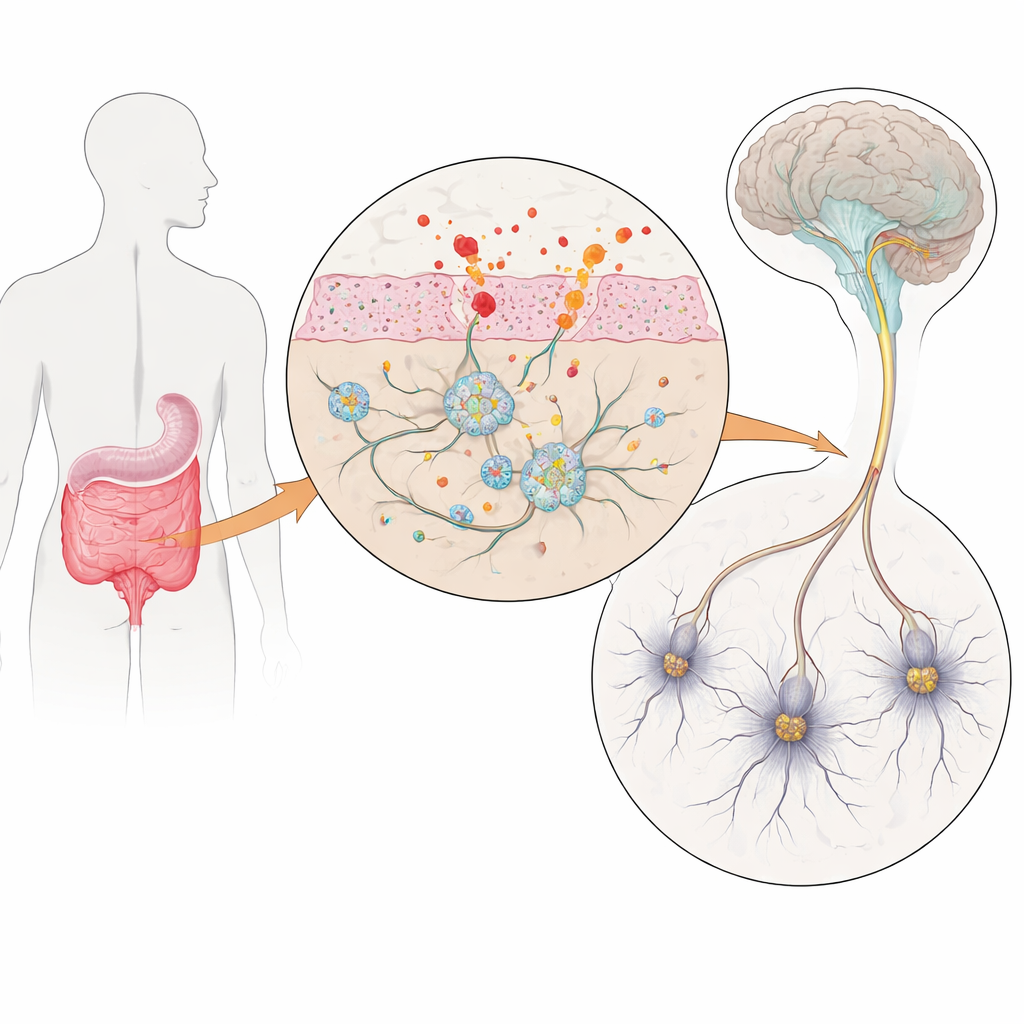
Des nerfs intestinaux en culture
Pour explorer cela, les chercheurs ont construit un modèle de laboratoire des nerfs intestinaux humains en utilisant des cellules souches pluripotentes induites – des cellules adultes reprogrammées en état proche de la souche puis orientées pour devenir des neurones entériques et des cellules gliales de soutien. Certaines lignées cellulaires portaient trois copies du gène codant l’alpha‑synucléine, une protéine qui s’agrège anormalement dans la maladie de Parkinson, tandis que des lignées témoins appariées présentaient un dosage génique normal. Après environ dix semaines de différenciation guidée, ces cultures contenaient un riche mélange de neurones et de glies d’allure intestinale reproduisant étroitement la diversité cellulaire des intestins humains réels. De façon cruciale, les cellules de type Parkinson produisaient un excès d’alpha‑synucléine, créant un modèle contrôlable des premiers stades de la maladie dans l’intestin.
Une vulnérabilité énergétique préexistante
Même avant toute exposition à l’inflammation, les cellules portant un excès d’alpha‑synucléine montraient des signes étendus de tension de leurs systèmes énergétiques. Un profilage génétique en cellules uniques a révélé des perturbations dans des voies traitant les lipides, le cholestérol et des éléments clés de la production d’énergie cellulaire. La microscopie a montré que leurs mitochondries – les petites centrales énergétiques intracellulaires – étaient moins nombreuses, plus petites et davantage fragmentées. La communication entre neurones et glies était aussi remodelée, avec une mise en avant des voies de signalisation liées au stress. Ensemble, ces observations dessinent le portrait de cellules nerveuses intestinales qui, malgré une apparence extérieure proche de cellules saines, vivent déjà à la limite en termes d’énergie et de résilience.
L’inflammation fait pencher la balance
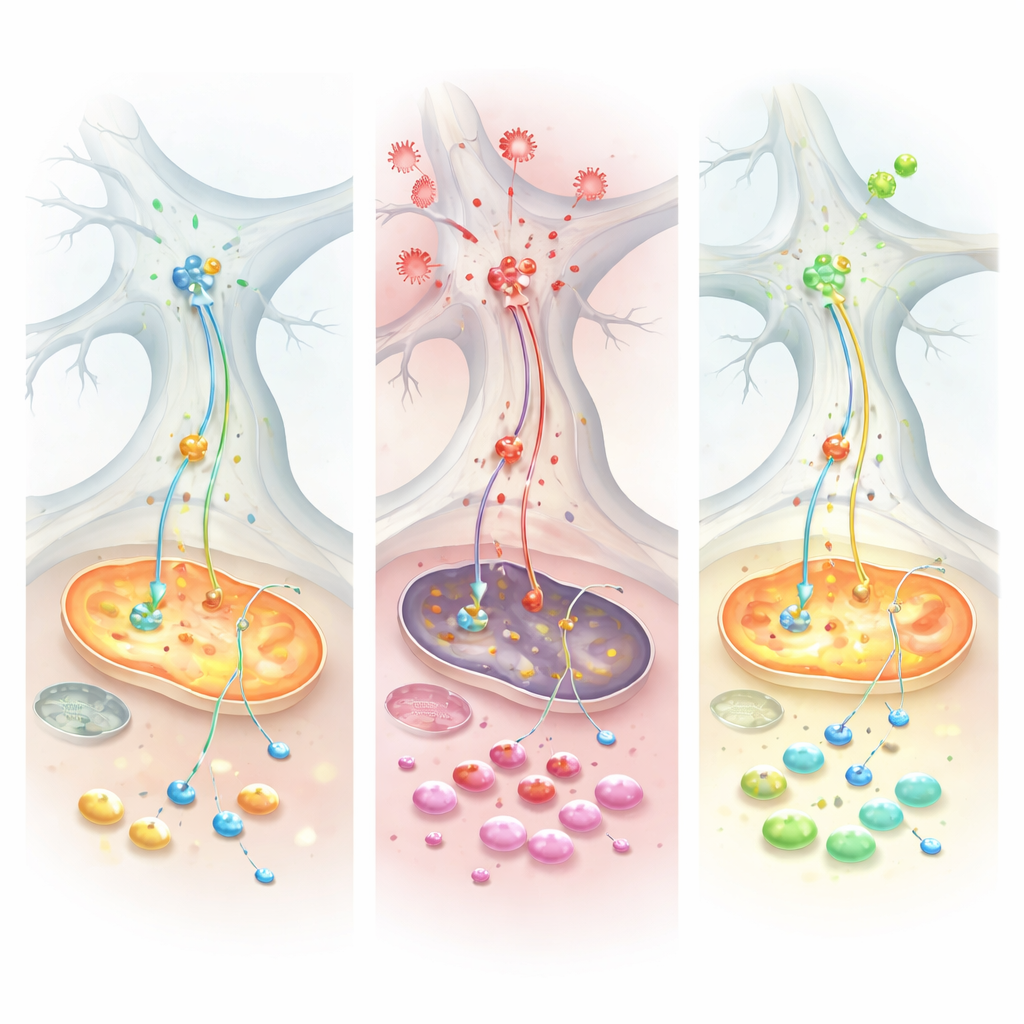
L’équipe a ensuite exposé les cultures au facteur de nécrose tumorale alpha (TNF), un signal inflammatoire majeur augmenté à la fois dans la maladie de Parkinson et dans des affections intestinales comme la rectocolite hémorragique. Le TNF a eu un impact nettement différent selon le type de culture. Dans les cellules de type Parkinson, le TNF a augmenté les niveaux d’alpha‑synucléine à l’intérieur des neurones et des glies et augmenté le contact physique de cette protéine avec les mitochondries, une combinaison associée à des dommages et au stress oxydatif. Les enregistrements électriques ont montré que les réseaux témoins sains pouvaient accroître leur activité après le TNF, tandis que les réseaux de type Parkinson restaient apathiques, révélant une capacité altérée à s’adapter à un défi inflammatoire. Au niveau moléculaire, les mesures de protéines et de métabolites ont convergé vers un système clé de transfert d’énergie appelé la navette malate–aspartate, qui achemine normalement le pouvoir réducteur vers les mitochondries. Sous TNF, cette navette défaillait spécifiquement dans les cellules de type Parkinson, épuisant des molécules essentielles et contraignant les cellules à recourir à l’oxydation du glutamine comme carburant d’urgence.
Une possible réparation et des indices chez les patients
Lorsque les chercheurs ont traité les cultures avec le Chicago‑Sky‑Blue 6B, un composé qui module la gestion du glutamate, le tableau a changé. Le médicament a restauré plusieurs paramètres de la respiration mitochondriale, réduit la dépendance anormale au glutamine et partiellement normalisé l’équilibre énergétique des cellules stressées. Pour vérifier si le même thème métabolique apparaît chez l’humain, l’équipe a analysé des tissus intestinaux de patients atteints de rectocolite hémorragique et de grands jeux de données publics d’expression génique. Dans plusieurs cohortes, ils ont observé une activité réduite des enzymes alimentant la navette malate–aspartate, parallèlement à une augmentation de l’alpha‑synucléine dans le tissu intestinal enflammé. Les patients répondant bien à une thérapie anti‑TNF avaient tendance à retrouver l’expression de ces enzymes énergétiques et à présenter des niveaux d’alpha‑synucléine plus bas, ce qui suggère que le schéma inflammatoire‑métabolique vu dans les cultures reflète la maladie humaine.
Pourquoi cela compte pour les patients
En termes simples, l’étude suggère qu’un excès d’alpha‑synucléine rend les nerfs intestinaux fragiles sur le plan métabolique, et que l’inflammation intestinale, via des signaux comme le TNF, exploite cette faiblesse. En paralysant une navette énergétique clé et en poussant les cellules vers un mode de carburant de secours sous tension, l’inflammation augmente le stress oxydatif, favorise l’association de l’alpha‑synucléine aux mitochondries et compromet la fonction normale des neurones entériques. Parce que des signatures similaires sont observées à la fois dans les modèles de Parkinson et dans les intestins humains enflammés, ce travail met en évidence une faiblesse métabolique partagée qui pourrait être ciblée par des thérapies futures. La modulation du métabolisme du glutamate et du glutamine – comme le fait le Chicago‑Sky‑Blue 6B dans cette étude – apparaît comme une stratégie prometteuse pour protéger le système nerveux intestinal, soulager potentiellement des symptômes tels que la constipation et peut‑être ralentir les stades précoces de la maladie de Parkinson et d’autres affections intestinales inflammatoires.
Citation: Ghirotto, B., Gonçalves, L.E., Ruder, V. et al. TNF alpha unmasks enteric malate aspartate shuttle dysfunction bridging Parkinson disease and intestinal inflammation. Nat Commun 17, 3217 (2026). https://doi.org/10.1038/s41467-026-71317-y
Mots-clés: Maladie de Parkinson, système nerveux entérique, inflammation intestinale, métabolisme mitochondrial, alpha‑synucléine