Clear Sky Science · he
TNF אלפא חושף לקות במעבר המלצט‑אספרטט הנטי שמגשרת בין מחלת פרקינסון לדלקת מעיים
הקשר המוסתר בין המעי לפרקינסון
רבים מהחולים במחלת פרקינסון מבחינים בבעיות בשירותים זמן רב לפני שידיהם מתחילות לרעוד. עצירות ונפיחות עלולות להופיע שנים לפני התסמינים התנועתיים, דבר המצביע על כך ש"המוח השני" של המעי — המערכת העצבית המעיונית — עשוי להיות מעורב בשלב מוקדם של המחלה. המחקר שואל שאלה פשוטה אך דחופה: כיצד דלקת במעיים מפריעה לעיצבוב המעי, והאם ההפרעה הזו עלולה לקדם את פרקינסון ומחלות מעיים אחרות?
עיצבובי מעיים בתרבית
כדי לחקור זאת בנו החוקרים מודל מעבדתי של עצבי המעי האנושיים באמצעות תאי גזע מנוונים מוחלטים (iPSCs) — תאים בוגרים שתוכנתו מחדש למצב דמוי‑גזע ואז הונחו להפוך לנוירונים המעיוניים ותאי תמיכה הנקראים גלייה. בקווי תאים מסוימים היו שלוש עותקים של הגן של אלפא‑סינוקלאין, חלבון שנוטה להצטבר באופן לא תקין בפרקינסון, בעוד שקווי בקרה תואמים נשאו דוזה גנטית תקינה. לאחר כעשרה שבועות של התפתחות מונחית, תרביות אלו הכילו תערובת עשירה של נוירונים וגלייה בדומה לגיוון התאי שנמצא במעי האנושי. באופן מהותי, תאי הדמיית‑פרקינסון ייצרו עודפי אלפא‑סינוקלאין, ויצרו מודל מבוקר של שלבי המחלה המוקדמים במעי.
פגיעות טעונה מראש באנרגיית התאים
עוד לפני שנוספה דלקת, תאים עם עודפי אלפא‑סינוקלאין הראו סימני עייפות נרחבים במערכות האנרגיה שלהם. פרופיילינג גנטי מיחיד‑תא חשף שיבושים בנתיבים המטפלים בשומנים, כולסטרול ובאבני בניין מרכזיות לדלקת תאית. מיקרוסקופיה הראתה כי המיטוכונדריות — תחנות הכוח הקטנות בתוך התאים — היו פחותות במספרן, קטנות יותר ומפורקות יותר. התקשורת בין נוירונים וגלייה עובדה מחדש גם היא, כאשר מסלולי איתות הקשורים ללחץ הפכו בולטים יותר. יחד, הממצאים ציירו תמונה של תאי עצב מעי שנראים מבחינה חיצונית דומים לתאים בריאים אך כבר חיים על סף מבחינה מטבולית וחוסן תאי.
דלקתמשנה את המאזן
צוות החוקרים הוסיף אז גורם דלקתי מרכזי — טומור נקרוזיס פקטור אלפא (TNF) — שהיווה איתות דלקתי גבוה הן במחלת פרקינסון והן במצבים מעיים דלקתיים כמו קוליטיס כיבית. ל‑TNF היה השפעה שונה בולטת על שני סוגי התרביות. בתרביות המדמות פרקינסון, TNF הגביר את רמות האלפא‑סינוקלאין בתאי הנוירון והגלייה והגביר את המגע הפיזי של החלבון עם המיטוכונדריות — שילוב המקושר לנזק ולחמצון. רישומי חשמל הראו כי רשתות הביקורת הבריאות יכלו להגביר את פעילותן לאחר TNF, אך הרשתות המדמות פרקינסון נותרו איטיות, מה שגילה חוסר יכולת להסתגל לאתגר דלקתי. ברמה המולקולרית, מדידות חלבון ומטבוליטים הצביעו אל מערכת מרכזית להעברת אנרגיה — מעבר המלצט–אספרטט (malate–aspartate shuttle), שלרוב מובילה כוח מחזר אל המיטוכונדריות. תחת TNF, המעבר הזה כשל ספציפית בתאים המדמים פרקינסון, התרוקנו מולקולות חיוניות והתאים נאלצו להסתמך על בעירה של גלוטמין כדלק חירום.
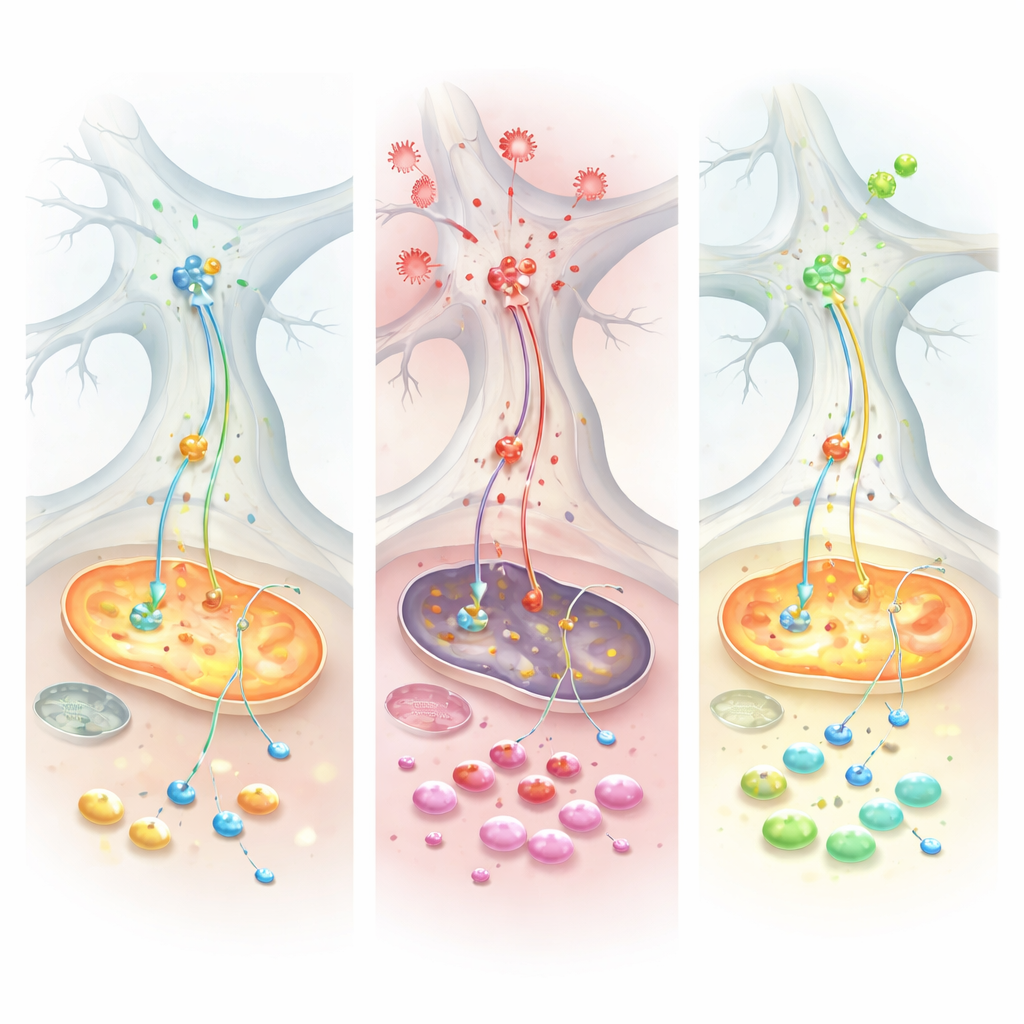
הצלה פוטנציאלית ורמזים ממטופלים
כאשר החוקרים טיפלו בתרביות בחומר Chicago‑Sky‑Blue 6B, תרכובת שמווסתת טיפול בגלוטמט, התמונה השתנתה. התרופה השיבה מספר מדדי נשימה מיטוכונדריאלית, צמצמה את התלות החריגה בגלוטמין וחיזקה חלקית את מאזן האנרגיה בתאים המותשים. כדי לבדוק האם אותו דפוס מטבולי מופיע באנשים אמיתיים, הצוות ניתח רקמות מעי של חולים עם קוליטיס כיבית וכן מערכי נתוני ביטוי גנים ציבוריים גדולים. במגוון קבוצות נמצאה פעילות מופחתת של אנזימים המפעילים את מעבר המלצט–אספרטט, לצד עליה באלפא‑סינוקלאין ברקמה מעולפת. מטופלים שענו טוב לטיפול אנטי‑TNF נטו לשחזר את הביטוי של אנזימי האנרגיה הללו והציגו רמות נמוכות יותר של אלפא‑סינוקלאין, מה שמרמז כי הדפוס הדלקתי‑מטבולי שנצפה בתרביות שיקף גם מחלה אנושית.
מדוע זה חשוב למטופלים
באופן פשוט, המחקר מרמז שעודף אלפא‑סינוקלאין עושה את עצבי המעי פגיעים מטבולית, ודלקת מעיים, דרך אותות כמו TNF, מנצלת חולשה זו. על‑ידי שיבוש מעבר אנרגיה מרכזי ודחיפת התאים למצב חירום תזונתי, הדלקת מגבירה מתח חמצוני, מעודדת את יצירת הקשר של אלפא‑סינוקלאין עם מיטוכונדריות ופוגעת בתפקוד התקין של נוירוני המעי. מאחר שחתימות דומות נצפות גם במודלים של פרקינסון וגם במעיים דלקתיים אנושיים, העבודה מצביעה על נקודת תורפה מטבולית משותפת שניתן לכוון בעזרתה טיפולים עתידיים. ויסות מטבוליזם של גלוטמט וגלוטמין — כפי שעושה Chicago‑Sky‑Blue 6B במחקר זה — מתגלה כאסטרטגיה מבטיחה להגן על מערכת העצבים של המעי, ולשפר תסמינים כמו עצירות ואולי להאט את שלבי ההתחלה של פרקינסון ומחלות מעיים דלקתיות אחרות.
ציטוט: Ghirotto, B., Gonçalves, L.E., Ruder, V. et al. TNF alpha unmasks enteric malate aspartate shuttle dysfunction bridging Parkinson disease and intestinal inflammation. Nat Commun 17, 3217 (2026). https://doi.org/10.1038/s41467-026-71317-y
מילות מפתח: מחלת פרקינסון, המערכת העצבית המעיונית, דלקת מעיים, מטבוליזם מיטוכונדריאלי, אלפא‑סינוקלאין