Clear Sky Science · nl
TNF-alpha onthult dysfunctie van de enterische malaat‑aspartaatshuttle als schakel tussen de ziekte van Parkinson en darmontsteking
De verborgen verbinding tussen de darm en Parkinson
Veel mensen met de ziekte van Parkinson merken eerst problemen bij het toilet op, jaren voordat hun handen beginnen te trillen. Obstipatie en een opgeblazen gevoel kunnen jaren aan bewegingstoornissen voorafgaan, wat suggereert dat het "tweede brein" van de darm – het enterische zenuwstelsel – al vroeg bij de ziekte betrokken kan zijn. Deze studie stelt een eenvoudige maar urgente vraag: hoe verstoort ontsteking in de darm deze darmazenuwen, en kan die verstoring bijdragen aan Parkinson en andere darmaandoeningen?
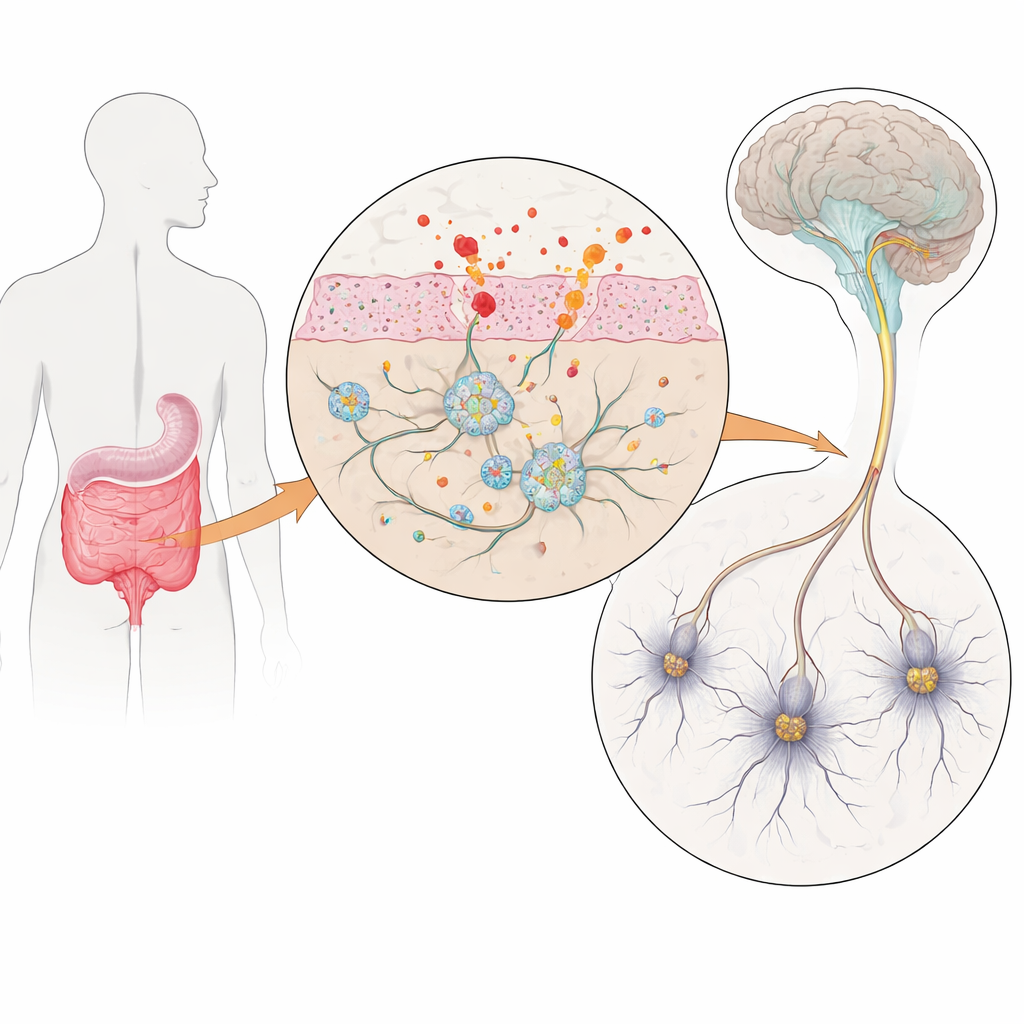
Darmazenuwen in een schaaltje
Om dit te onderzoeken bouwden de onderzoekers een laboratoriummodel van menselijke darmazenuwen met behulp van geïnduceerde pluripotente stamcellen – volwassen cellen die teruggebracht zijn naar een stamcelachtige staat en vervolgens gestuurd zijn om enterische neuronen en ondersteunende gliacellen te worden. Sommige stamcellijnen droegen drie kopieën van het gen voor alpha‑synucleïne, een eiwit dat abnormaal samenklontert bij de ziekte van Parkinson, terwijl overeenkomstige controlegroepen een normale genendosering hadden. Na ongeveer tien weken gerichte ontwikkeling bevatten deze kweekjes een rijke mix van darmachtige neuronen en glia die sterk leken op de cellulaire diversiteit in echte menselijke darmen. Cruciaal was dat de Parkinson‑achtige cellen extra alpha‑synucleïne produceerden, waarmee een controleerbaar model van vroege ziekte in de darm ontstond.
Een vooraf bestaande kwetsbaarheid in de celenergie
Al voordat enige ontsteking werd toegevoegd, vertoonden cellen met extra alpha‑synucleïne wijdverbreide tekenen van stress in hun energiesystemen. Gedetailleerde enkelcelsgenprofilering liet verstoringen zien in routes die vetten, cholesterol en belangrijke bouwstenen voor celbrandstof verwerken. Microscopen toonden dat hun mitochondriën – de kleine energiecentrales in cellen – minder talrijk, kleiner en meer gefragmenteerd waren. De communicatie tussen neuronen en glia was ook veranderd, met stressgerelateerde signaalroutes die prominenter werden. Samen schetsten deze bevindingen het beeld van darmazenuwcellen die er van buitenaf grotendeels gezond uitzien, maar energetisch en qua veerkracht al dicht bij het kantelpunt leven.
Ontsteking kantelt de balans
Vervolgens introduceerde het team tumor necrose factor alpha (TNF), een belangrijk ontstekingssignaal dat verhoogd is zowel bij de ziekte van Parkinson als bij darmaandoeningen zoals colitis ulcerosa. TNF had een opvallend verschillend effect op de twee typen kweekjes. In de Parkinson‑achtige cellen verhoogde TNF de alpha‑synucleïne‑niveaus in zowel neuronen als glia en vergrootte het de fysieke associatie van het eiwit met mitochondriën, een combinatie die geassocieerd wordt met schade en oxidatieve stress. Elektrische opnames lieten zien dat gezonde controlednetwerken hun activiteit konden opvoeren na TNF, maar de Parkinson‑achtige netwerken bleven traag, wat een beperkte aanpassingscapaciteit aan inflammatoire prikkels aantoont. Op moleculair niveau kwamen eiwit‑ en metabolietmetingen samen op een belangrijk energieshuttlesysteem: de malaat–aspartaatshuttle, die normaal reducerende kracht naar de mitochondriën transporteert. Onder TNF faalde deze shuttle specifiek in de Parkinson‑achtige cellen, waardoor essentiële moleculen uitgeput raakten en de cellen gedwongen werden glutamine als noodbrandstof te verbranden.
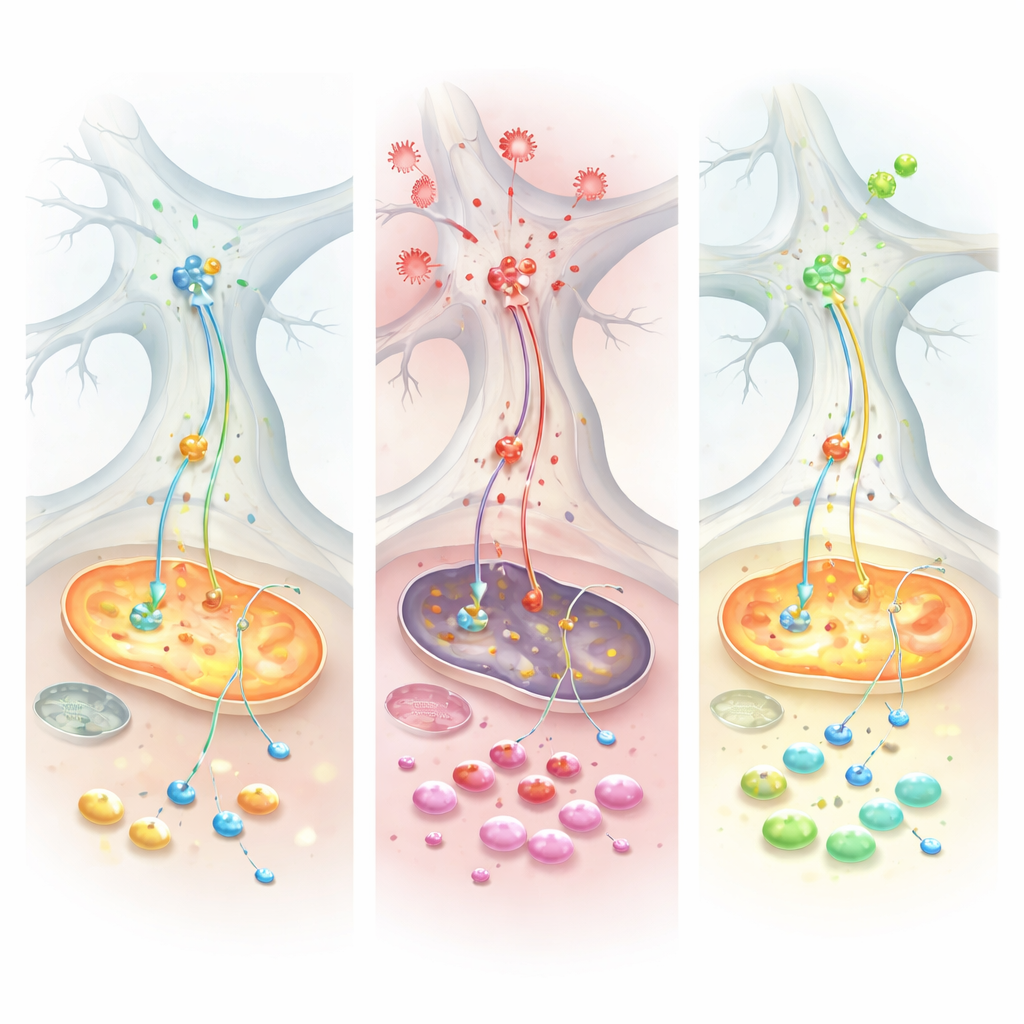
Een mogelijke redding en aanwijzingen uit patiëntgegevens
Toen de onderzoekers de kweekjes behandelden met Chicago‑Sky‑Blue 6B, een verbinding die het glutamaat‑verkeer moduleert, veranderde het beeld. Het middel herstelde meerdere maten van mitochondriale ademhaling, verminderde de abnormale afhankelijkheid van glutamine en normaliseerde deels het energiebalans in de gestreste cellen. Om te testen of hetzelfde metabole thema in echte mensen voorkomt, analyseerde het team darmweefsel van patiënten met colitis ulcerosa en grote openbare genexpressiedatasets. In meerdere cohorten vonden ze verminderde activiteit van enzymen die de malaat–aspartaatshuttle aandrijven, samen met verhoogde alpha‑synucleïne in ontstoken darmweefsel. Patiënten die goed reageerden op anti‑TNF‑therapie herkregen vaak de expressie van deze energieenzymen en toonden lagere alpha‑synucleïne‑niveaus, wat suggereert dat het ontstekings‑en metabolische patroon dat in de kweekjes werd gezien ook in de menselijke ziekte wordt weerspiegeld.
Waarom dit belangrijk is voor patiënten
Simpel gezegd suggereert de studie dat een overmaat aan alpha‑synucleïne darmazenuwen metabolisch kwetsbaar maakt, en dat darmontsteking, via signalen zoals TNF, deze zwakke plek uitbuit. Door een cruciale energieshuttle te verlammen en cellen in een uitgeputte noodbrandstofmodus te drukken, verhoogt ontsteking oxidatieve stress, bevordert het de associatie van alpha‑synucleïne met mitochondriën en ondermijnt het de normale functie van darmazenuwen. Omdat vergelijkbare signaturen gezien worden in zowel Parkinson‑modellen als ontstoken menselijke darmen, wijst het werk op een gedeeld metabool zwak punt dat met toekomstige therapieën kan worden aangepakt. Het moduleren van glutamaat‑ en glutamine‑metabolisme – zoals Chicago‑Sky‑Blue 6B in deze studie doet – komt naar voren als een veelbelovende strategie om het darmzenuwstelsel te beschermen, mogelijk klachten als obstipatie te verlichten en wellicht de vroegste stadia van Parkinson en andere inflammatoire darmcondities te vertragen.
Bronvermelding: Ghirotto, B., Gonçalves, L.E., Ruder, V. et al. TNF alpha unmasks enteric malate aspartate shuttle dysfunction bridging Parkinson disease and intestinal inflammation. Nat Commun 17, 3217 (2026). https://doi.org/10.1038/s41467-026-71317-y
Trefwoorden: Ziekte van Parkinson, enterisch zenuwstelsel, darmontsteking, mitochondriaal metabolisme, alpha-synucleïne