Clear Sky Science · ar
عامل النخر الورمي ألفا يكشف خللاً في ناقل المالييت-أسبارتات المعوي يربط مرض باركنسون بالتهاب الأمعاء
الرابط الخفي بين الأمعاء ومرض باركنسون
يلاحظ كثير من المصابين بمرض باركنسون مشاكل في الحمام قبل أن تبدأ أيديهم بالاهتزاز بفترة طويلة. قد تظهر الإمساك والانتفاخ قبل سنوات من ظهور مشاكل الحركة، مما يشير إلى أن «الدماغ الثاني» في الأمعاء — الجهاز العصبي المعوي — قد يشارك مبكراً في المرض. تطرح هذه الدراسة سؤالاً بسيطاً لكنه ملح: كيف يزعج الالتهاب المعوي هذه الأعصاب المعوية، وهل يمكن أن يساهم هذا الاضطراب في دفع مرض باركنسون واضطرابات معوية أخرى؟
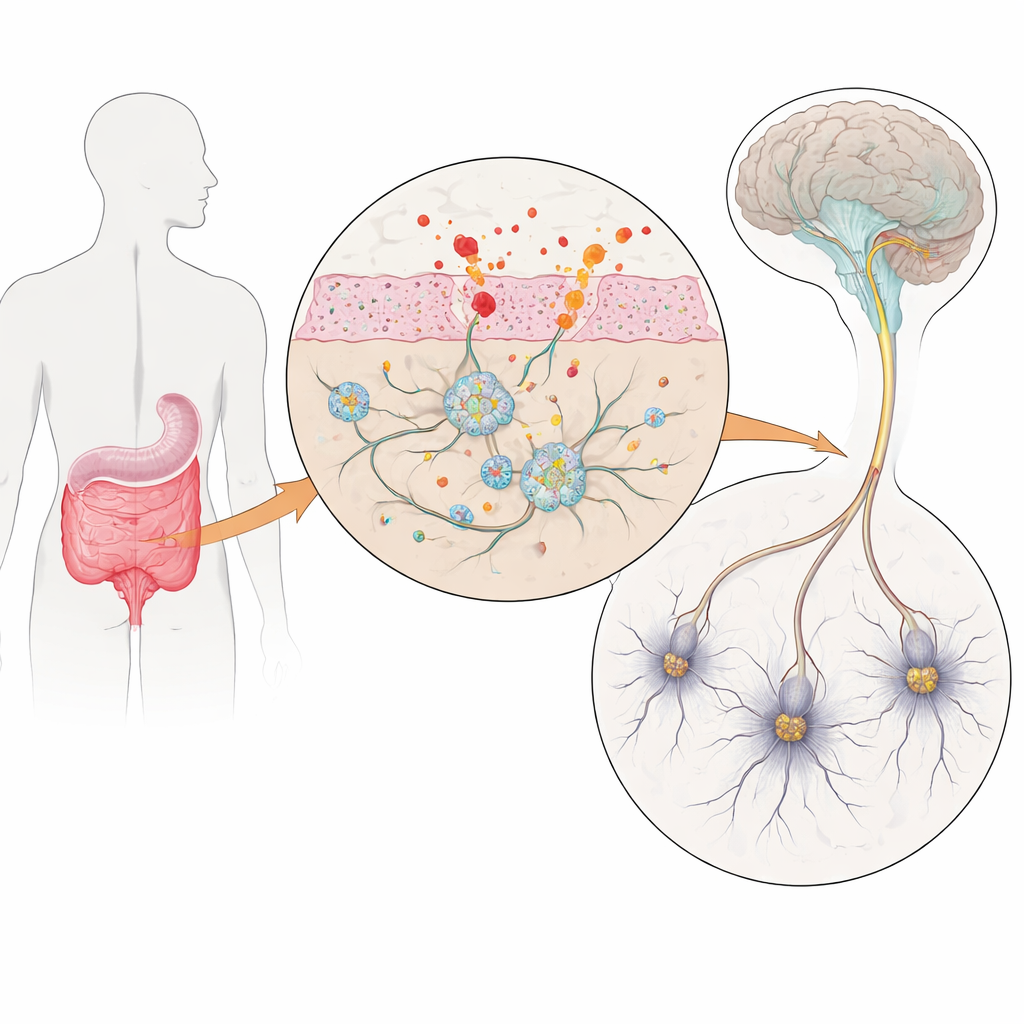
أعصاب الأمعاء في طبق مخبري
لاستكشاف ذلك، بنى الباحثون نموذجاً مخبرياً لأعصاب الأمعاء البشرية باستخدام الخلايا الجذعية المحفزة متعددة القدرات — خلايا بالغة أعيد برمجتها إلى حالة شبيهة بالخلايا الجذعية ثم وجهت لتصبح خلايا عصبية معوية وخلايا داعمة تُدعى الخلايا الدبقية. حملت بعض خطوط الخلايا الجذعية ثلاث نسخ من جين الألفا‑سينوكلين، وهو بروتين يتجمع بشكل غير طبيعي في مرض باركنسون، بينما كانت خطوط الضابطة المطابقة ذات جرعة جينية طبيعية. بعد نحو عشرة أسابيع من التوجيه التطوري، احتوت هذه المزارع على مزيج غني من الخلايا العصبية المعوية والخلايا الدبقية يشبه تنوع الخلايا الموجود في الأمعاء البشرية الحقيقية. والأهم من ذلك، أن الخلايا الشبيهة بباركنسون أنتجت فائضاً من الألفا‑سينوكلين، ما وفّر نموذجاً يمكن التحكم به لمرحلة مبكرة من المرض في الأمعاء.
عَرْض ضعف مسبق في طاقة الخلايا
حتى قبل إضافة أي التهاب، أظهرت الخلايا التي تنتج فائض الألفا‑سينوكلين علامات انتشارية من الضغط على أنظمة طاقتها. كشفت بيانات تفصيلية على مستوى الخلية الواحدة عن اضطرابات في المسارات التي تتعامل مع الدهون والكولسترول والعناصر الأساسية لتوليد وقود الخلية. أظهرت الميكروسكوبي أن الميتوكوندريا — محطات الطاقة الصغيرة داخل الخلايا — كانت أقل عدداً وأصغر وأكثر تهشماً. كما أعيد ترتيب التواصل بين الخلايا العصبية والخلايا الدبقية، مع بروز مسارات إشارية مرتبطة بالإجهاد. مجتمعة، رسمت هذه النتائج صورة لخلايا عصبية معوية تبدو شبيهة خارجياً بالخلايا السليمة لكنها بالفعل تعيش قرب حافة التحمل من حيث الطاقة والقدرة على الصمود.
الالتهاب يقلب المعادلة
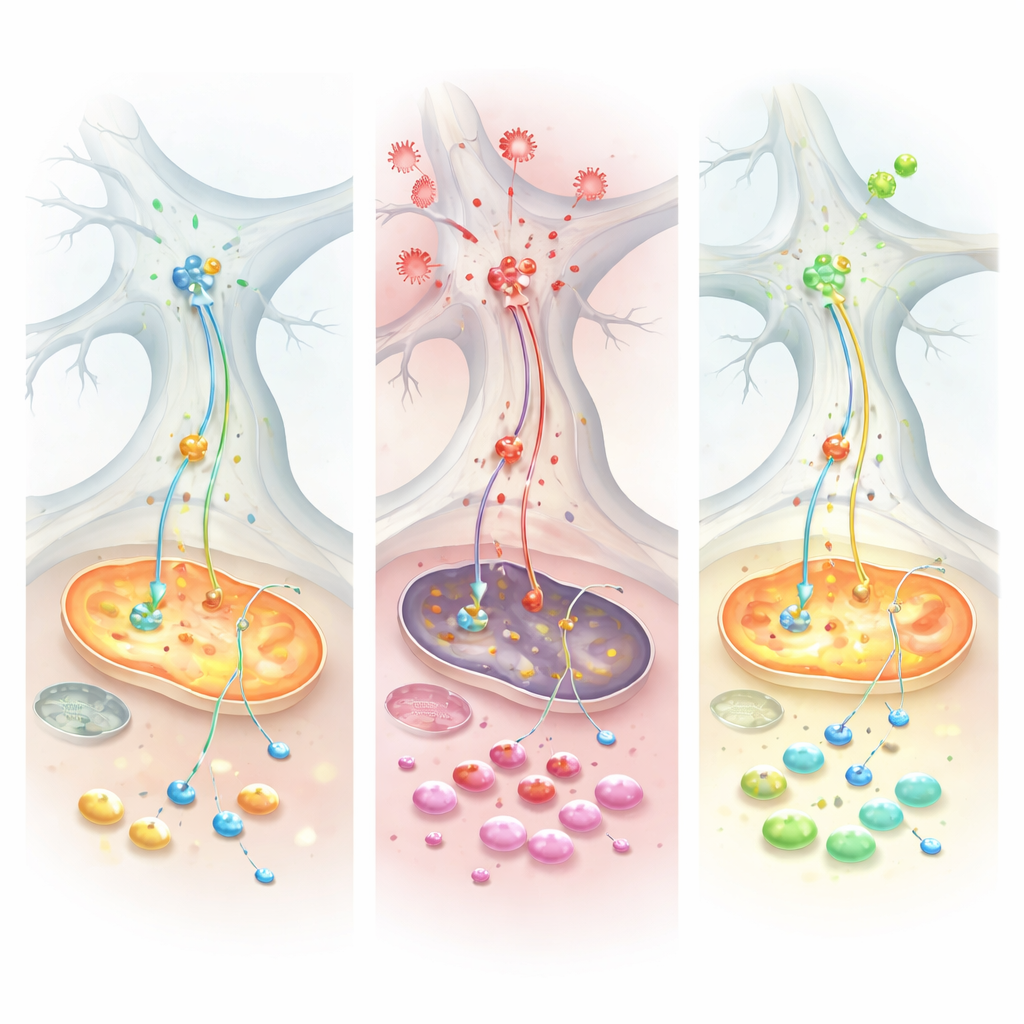
ثم قدم الفريق عامل النخر الورمي ألفا (TNF)، إشارة التهابية رئيسية مرتفعة في كل من مرض باركنسون واضطرابات الأمعاء مثل التهاب القولون التقرحي. كان لتأثير TNF اختلاف ملحوظ بين نوعي المزارع. في الخلايا الشبيهة بباركنسون، رفع TNF مستويات الألفا‑سينوكلين داخل الخلايا العصبية والخلايا الدبقية وزاد من تماس البروتين مع الميتوكوندريا، وهو توليفة مرتبطة بالضرر والإجهاد التأكسدي. أظهرت القياسات الكهربائية أن الشبكات الضابطة الصحية تستطيع زيادة نشاطها بعد TNF، لكن شبكات شبيهة باركنسون بقيت خاملة نسبياً، ما كشف عن قصور في القدرة على التكيف مع التحدي الالتهابي. على المستوى الجزيئي، اتفقت قياسات البروتينات والوسطاء الأيضيّة على نظام نقل طاقة رئيسي يُدعى ناقل المالييت‑الأسبارتات، الذي عادةً ينقل قدرة الاختزال إلى الميتوكوندريا. تحت تأثير TNF، انهار هذا الناقل بشكل خاص في الخلايا الشبيهة بباركنسون، مستنزفاً جزيئات أساسية ومجبرًا الخلايا على التحول لحرق الجلوتامين كوقود طارئ.
إنقاذ محتمل ودلائل من مرضى حقيقيين
عندما عالج الباحثون المزارع بمركب Chicago‑Sky‑Blue 6B، وهو مركب يؤثر على معالجة الجلوتامات، تغيرت الصورة. أعاد الدواء عدة مقاييس للتنفس الميتوكوندري، وقلّص الاعتماد غير الطبيعي على الجلوتامين، وعاد جزئياً توازن الطاقة في الخلايا المتوترة. لاختبار ما إذا كان نفس النمط الأيضي يظهر لدى البشر، حلل الفريق نسيج أمعاء من مرضى التهاب القولون التقرحي وبيانات عامة كبيرة للتعبير الجيني. عبر مجموعات متعددة، وجدوا انخفاضاً في نشاط الإنزيمات المسؤولة عن تشغيل ناقل المالييت‑الأسبارتات، جنباً إلى جنب مع زيادة في الألفا‑سينوكلين في النسيج المعوي الملتهب. الميلادون الذين استجابوا جيداً للعلاج المضاد لـ TNF بدت لديهم إعادة تعبير لهذه الإنزيمات الطاقية وانخفضت لديهم مستويات الألفا‑سينوكلين، مما يوحي بأن النمط الالتهابي‑الأيضي المرصود في المزارع المخبرية ينعكس أيضاً في المرض البشري.
لماذا يهم هذا المرضى
ببساطة، تقترح الدراسة أن فرط الألفا‑سينوكلين يجعل أعصاب الأمعاء هشة من الناحية الأيضية، وأن الالتهاب المعوي عبر إشارات مثل TNF يستغل هذه الضعف. من خلال إعطاب ناقل طاقة رئيسي ودفع الخلايا إلى وضع احتياطي مرهق من حيث الوقود، يزيد الالتهاب الإجهاد التأكسدي، ويشجع ارتباط الألفا‑سينوكلين بالميتوكندريا، ويقوض الوظيفة الطبيعية للخلايا العصبية المعوية. وبما أن توقيعات مماثلة تُرى في نماذج باركنسون والأمعاء الملتهبة لدى البشر، يشير العمل إلى نقطة ضعف أيضية مشتركة قد تُستغل لعلاجات مستقبلية. يظهر تعديل أيض الغلوتامات والجلوتامين — كما يفعل Chicago‑Sky‑Blue 6B في هذه الدراسة — كاستراتيجية واعدة لحماية الجهاز العصبي المعوي، مما قد يخفف أعراضاً مثل الإمساك وربما يبطئ المراحل المبكرة من باركنسون وحالات الأمعاء الالتهابية الأخرى.
الاستشهاد: Ghirotto, B., Gonçalves, L.E., Ruder, V. et al. TNF alpha unmasks enteric malate aspartate shuttle dysfunction bridging Parkinson disease and intestinal inflammation. Nat Commun 17, 3217 (2026). https://doi.org/10.1038/s41467-026-71317-y
الكلمات المفتاحية: مرض باركنسون, الجهاز العصبي المعوي, التهاب الأمعاء, الأيض الميتوكوندري, ألفا-سينوكلين