Clear Sky Science · ru
TNF альфа выявляет дисфункцию малат‑аспартатного шунта в энтерической системе, связывая болезнь Паркинсона и кишечное воспаление
Скрытая связь между кишечником и болезнью Паркинсона
У многих людей с болезнью Паркинсона проблемы с туалетом возникают задолго до того, как начинают дрожать руки. Запор и вздутие могут появляться за годы до моторных симптомов, что намекает на то, что «второй мозг» кишечника — энтерическая нервная система — может быть вовлечён в болезнь на ранних стадиях. В этом исследовании поставлен простой, но важный вопрос: как воспаление в кишечнике нарушает работу этих кишечных нервов и может ли такое нарушение способствовать развитию болезни Паркинсона и других кишечных расстройств?
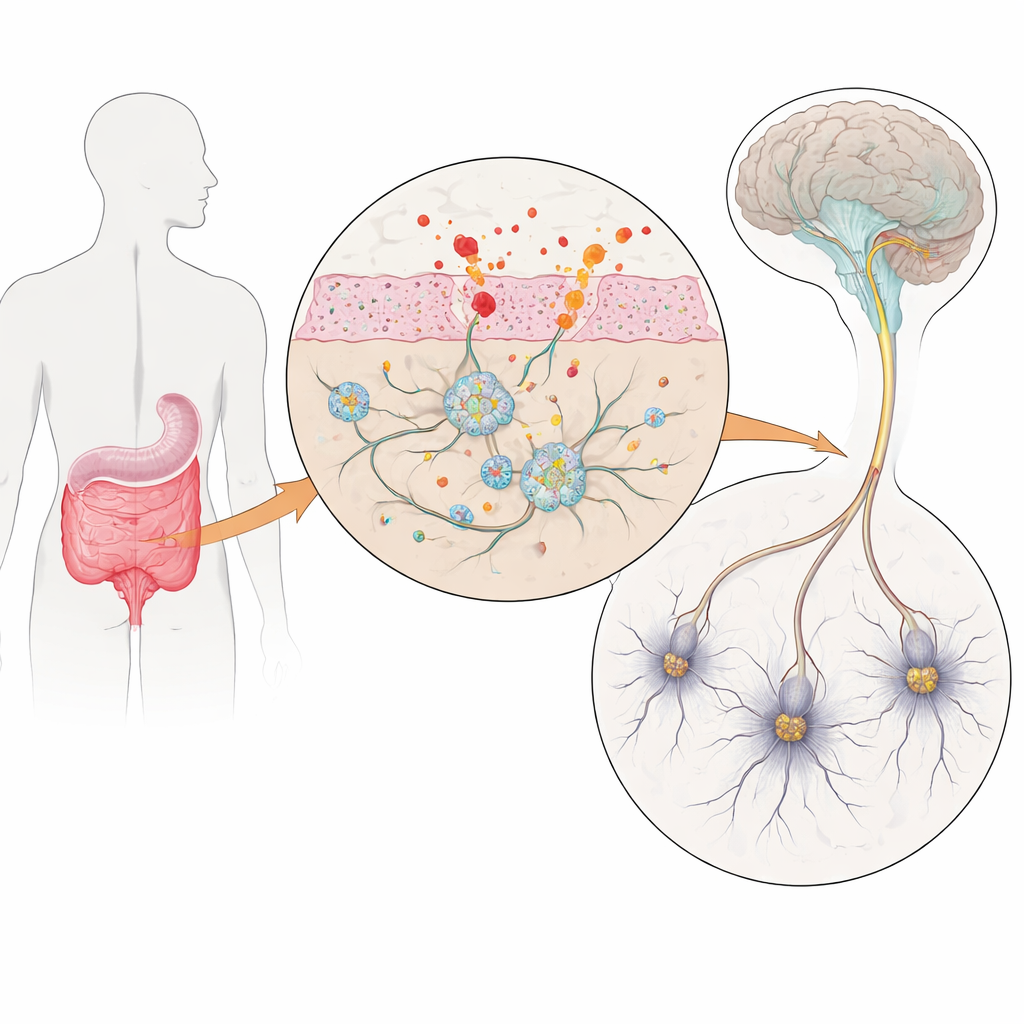
Кишечные нейроны в чашке Петри
Чтобы изучить это, исследователи создали лабораторную модель человеческих кишечных нервов, используя индуцированные плюрипотентные стволовые клетки — взрослые клетки, перепрограммированные в стволоподобное состояние и затем направленные в развитие в энтерические нейроны и поддерживающие клетки — глии. Некоторые линии стволовых клеток несли три копии гена альфа‑синуклеина — белка, который аномально агрегирует при болезни Паркинсона, в то время как контрольные линии имели нормальную дозу гена. Примерно через десять недель направленного развития эти культуры содержали богатую смесь кишечноподобных нейронов и глии, тесно напоминавшую клеточное разнообразие настоящего человеческого кишечника. Важным было то, что клетки, моделировавшие Паркинсон, производили повышенное количество альфа‑синуклеина, создавая управляемую модель ранней патологии в кишечнике.
Заложенная уязвимость в энергетике клеток
Ещё до введения воспаления клетки с избыточным альфа‑синуклеином демонстрировали широкие признаки напряжения в системах производства энергии. Подробный одно‑клеточный генетический профиль выявил нарушения в путях, обрабатывающих жиры, холестерин и ключевые строительные блоки для клеточного топлива. Микроскопия показала, что их митохондрии — крошечные электростанции внутри клеток — были менее многочисленны, мельче и более фрагментированы. Коммуникация между нейронами и глией также была перестроена, с усилением сигнальных путей, связанных со стрессом. В совокупности эти результаты рисуют картину клеток кишечных нервов, которые внешне похожи на здоровые, но уже находятся на грани по запасам энергии и устойчивости.
Воспаление нарушает равновесие
Команда затем ввела фактор некроза опухоли альфа (TNF), главный воспалительный сигнал, повышенный при болезни Паркинсона и при кишечных расстройствах, таких как язвенный колит. TNF оказал поразительно разный эффект на два типа культур. В клетках, моделировавших Паркинсон, TNF повышал уровни альфа‑синуклеина как в нейронах, так и в глии и усиливал физический контакт этого белка с митохондриями — сочетание, связанное с повреждением и оксидативным стрессом. Электрофизиологические записи показали, что здоровые контрольные сети могли увеличивать свою активность после TNF, тогда как паркинсоноподобные сети оставались вялотекущими, что указывает на нарушенную способность адаптироваться к воспалительному вызову. На молекулярном уровне измерения белков и метаболитов сошлись на ключевой системе переноса энергии — малат‑аспартатном шунте, который обычно переносит восстановительную силу в митохондрии. Под воздействием TNF этот шунт давал сбой специфически в паркинсоноподобных клетках, истощая необходимые молекулы и заставляя клетки переключаться на окисление глутамина в качестве аварийного топлива.
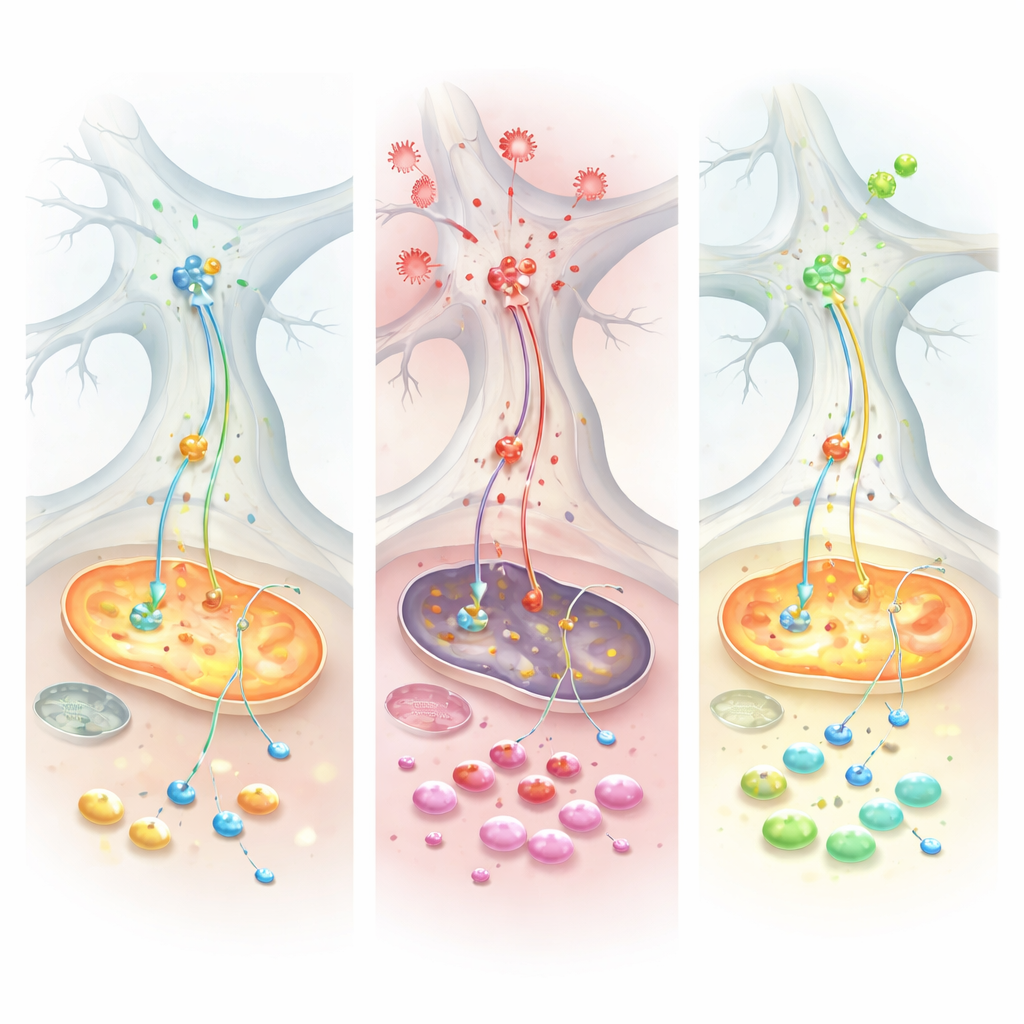
Возможное спасение и подтверждение в образцах пациентов
Когда исследователи обработали культуры соединением Chicago‑Sky‑Blue 6B, модифицирующим обращение с глутаматом, ситуация изменилась. Препарат восстановил несколько показателей «дыхания» митохондрий, снизил аномальную зависимость от глутамина и частично нормализовал энергетический баланс в подвергнутых стрессу клетках. Чтобы проверить, проявляется ли та же метаболическая тема у реальных людей, команда проанализировала кишечную ткань пациентов с язвенным колитом и большие публичные наборы данных экспрессии генов. В нескольких когортах они обнаружили пониженную активность ферментов, обеспечивающих работу малат‑аспартатного шунта, наряду с повышением уровня альфа‑синуклеина в воспалённой ткани кишечника. Пациенты, хорошо ответившие на анти‑TNF‑терапию, как правило, восстанавливали экспрессию этих энергетических ферментов и демонстрировали более низкие уровни альфа‑синуклеина, что говорит о том, что воспалительно‑метаболический профиль, увиденный в культурах, отражается и в человеческой болезни.
Почему это важно для пациентов
Проще говоря, исследование предполагает, что избыток альфа‑синуклеина делает кишечные нервы метаболически уязвимыми, а кишечное воспаление, через сигналы вроде TNF, эксплуатирует эту слабость. Парализуя ключевой энергетический шунт и заставляя клетки переходить на режим аварийного топлива, воспаление увеличивает оксидативный стресс, способствует ассоциации альфа‑синуклеина с митохондриями и подрывает нормальную функцию кишечных нейронов. Поскольку похожие сигнатуры наблюдаются и в моделях Паркинсона, и во воспалённой ткани человека, работа указывает на общую метаболическую «слабую точку», которую можно было бы нацелить в будущих терапиях. Модуляция метаболизма глутамата и глутамина — как это делает Chicago‑Sky‑Blue 6B в данном исследовании — предстает как многообещающая стратегия защиты нервной системы кишечника, потенциально облегчая симптомы, такие как запор, и, возможно, замедляя ранние стадии болезни Паркинсона и других воспалительных кишечных состояний.
Цитирование: Ghirotto, B., Gonçalves, L.E., Ruder, V. et al. TNF alpha unmasks enteric malate aspartate shuttle dysfunction bridging Parkinson disease and intestinal inflammation. Nat Commun 17, 3217 (2026). https://doi.org/10.1038/s41467-026-71317-y
Ключевые слова: Болезнь Паркинсона, энтерическая нервная система, кишечное воспаление, митохондриальный метаболизм, альфа‑синуклеин