Clear Sky Science · zh
多功能且高灵敏的单体与多聚(ADP‑核糖基化)检测揭示了XRCC1依赖的PARP1信号重塑
为什么我们DNA修复体系上的微小化学标签很重要
我们体内的每个细胞都在不断修复DNA损伤。如果修复出错,可能导致癌症、神经退行性疾病或细胞死亡。该修复网络中的关键参与者之一是名为PARP1的蛋白,它会用来自NAD+的小糖状标签修饰自身和邻近蛋白。这些标签既有短链也有长链,作为信号招募其他修复因子。直到现在,科学家们缺乏能在细胞内精确观测并区分这些不同标签类型的工具,尤其是在疾病状态下。本研究构建了此类工具,并利用它们揭示了在另一修复蛋白XRCC1缺失时DNA修复信号出乎意料的改变。
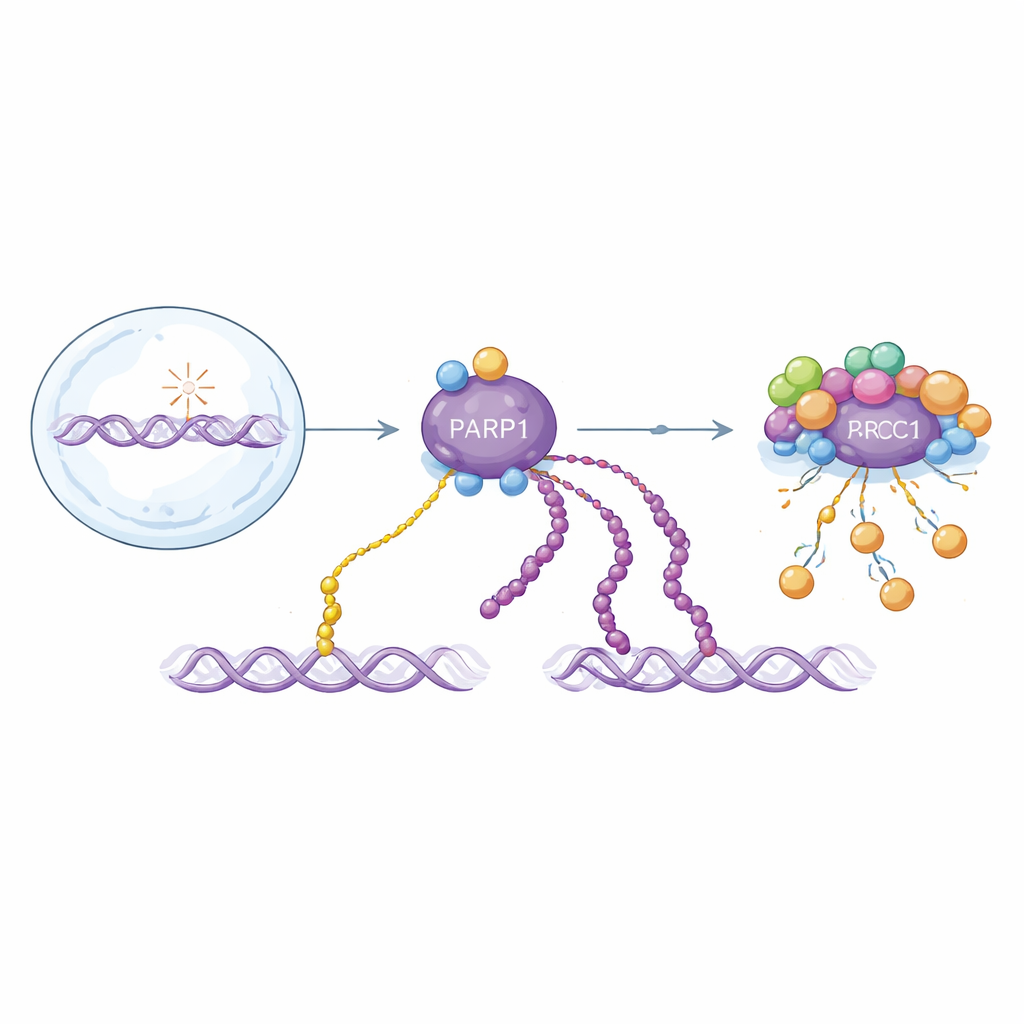
关键DNA修复信号的两种“口味”
PARP1对DNA链断裂的反应是将ADP‑核糖单元连接到自身及其他蛋白上。这些修饰可以是单个单元(单体ADP‑核糖基化)或长链(多聚ADP‑核糖基化)。两种形式都参与组织修复,但在时间上的行为不同:长链在最初迅速出现并被快速去除,而单体则累积较慢且持续时间更长。因为两者都由相同的构件构成,大多数现有检测方法会将它们混为一谈。这使得难以理解它们各自如何影响健康与疾病,或针对PARP1的药物究竟如何发挥作用。
构建高度选择性的分子“眼睛”
作者扩展了一种化学生物学平台,能够以程序化方式在短肽的特定位点(丝氨酸残基)上放置ADP‑核糖。他们使用这些定制肽作为诱饵,从大型展示文库中筛选抗体片段。关键在于引入了一步“单体封堵”:用单体修饰的肽吸收识别单体的抗体,从而保留偏好长链的候选者。该策略生成了模块化抗体,这些抗体在借助SpyTag/SpyCatcher体系组装后,可以快速转换为用于印迹、显微镜和拉下实验的不同格式。团队还在质谱中发现了一种独特的片段离子模式,特异性标识携带两个ADP‑核糖单元的肽,帮助准确标定蛋白上多聚修饰的位置。
在他人看不到的地方捕捉微弱信号
借助新工具,研究人员展示了这些多聚特异性抗体能检测到非常短的链、长链,甚至游离的ADP‑核糖聚合物,其灵敏度远高于现有商业试剂。抗体能跨越不同的氨基酸连接类型(不仅限于丝氨酸),并能在先前工具无信号可见的条件下(例如未受应激的细胞或低氧增殖的细胞)可视化多聚ADP‑核糖。同时,团队对早期的单体特异性和位点特异性抗体进行了亲和力成熟,以在保持选择性的同时提升灵敏度。总体而言,这套工具箱允许在同一细胞中同时成像单体与多聚信号,揭示多聚修饰出现在局部的核内焦点,而单体修饰则形成更弥散且持久的染色质波。
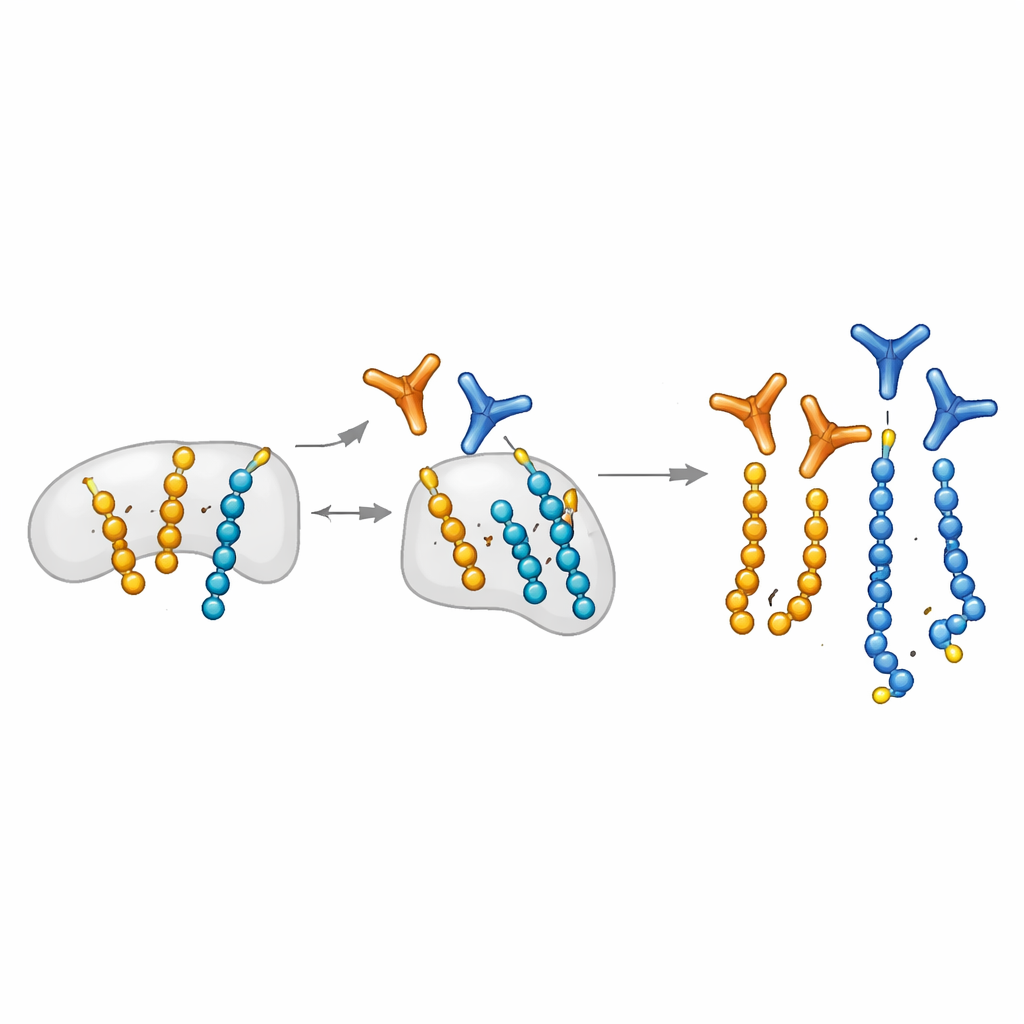
XRCC1 缺失如何重塑DNA修复波
XRCC1 通常作为支架,帮助PARP1与DNA修复中间体结合并随后脱离。当XRCC1 丢失时,PARP1会过度活化,长期以来人们已知它会过度合成长链ADP‑核糖,这一状态与神经退行性有关。利用他们优化的抗体组,作者表明XRCC1 丢失带来的影响不仅是长链的增多:单体ADP‑核糖化波也被显著放大。在来自不同致损剂的持续DNA损伤过程中,缺乏XRCC1 的细胞对长链和短链修饰都表现出更高且更早的峰值,且不同损伤类型的时序存在差异。单体修饰通常比快速波动的多聚信号更稳定且分布更均匀。该研究还鉴定出组蛋白H1作为一个主要的单体修饰靶点,其持续的标记可能使损伤周围的染色质保持更放松的状态。
从改变的信号到改变的蛋白质流动
丝氨酸上的单体ADP‑核糖本身还可以通过一种罕见的化学连接被进一步连接到泛素,形成一种混合标记,称为ADP‑核糖‑泛素化。泛素连接酶RNF114识别这种复合信号并被吸引到DNA损伤位点,在那里它可能修饰或重新定位其他蛋白。利用一种专门的识别蛋白(ZUD)与他们的抗体并行使用,作者显示XRCC1 缺失不仅增加了单体ADP‑核糖,还增加了这种混合标记以及RNF114对断裂位点的募集。这表明失调的单体信号及其与泛素的串话可能促成XRCC1 突变时观察到的细胞应激与疾病表型。
这对理解与治疗疾病意味着什么
对非专业读者而言,核心信息是:曾被视为单一的DNA修复信号其实是两种重叠的微小化学标签波,各自具有不同的时序与后果。通过构建高度选择性的分子工具,本研究将这两种波分离开来,并显示XRCC1 缺失不仅强化了人们熟知的长链爆发,还放大了持续的单体潮以及其相关的泛素标记。这些发现细化了我们对PARP1 工作方式的理解,帮助解释为何XRCC1及相关酶的缺陷会导致脑部疾病,并提供了一套工具箱,供其他研究者在癌症、免疫学等领域解剖ADP‑核糖基化——有望促成更精确地使用针对PARP的药物。
引用: Dauben, H., Mihaljević, M., Kolvenbach, A. et al. Versatile and sensitive detection of mono- and poly(ADP-ribosyl)ation reveals XRCC1-dependent remodelling of PARP1 signalling. Nat Commun 17, 3216 (2026). https://doi.org/10.1038/s41467-026-71311-4
关键词: ADP‑核糖基化, DNA 损伤修复, PARP1 信号, XRCC1 缺失, 泛素化