Clear Sky Science · es
Detección versátil y sensible de mono- y poli(ADP-ribosil)ación revela remodelado dependiente de XRCC1 de la señalización de PARP1
Por qué importan las pequeñas etiquetas químicas en nuestro sistema de reparación del ADN
Cada célula de nuestro cuerpo está continuamente reparando daños en su ADN. Si esa reparación falla, el resultado puede ser cáncer, neurodegeneración o muerte celular. Un actor clave en esta red de reparación es una proteína llamada PARP1, que se marca a sí misma y a proteínas cercanas con pequeñas etiquetas tipo azúcar derivadas de NAD+. Estas etiquetas aparecen en formas cortas y largas y actúan como señales que reclutan otros factores de reparación. Hasta ahora, los científicos carecían de herramientas precisas para ver y distinguir estos diferentes tipos de etiqueta dentro de las células, especialmente en condiciones de enfermedad. Este estudio construye esas herramientas y las usa para revelar un cambio inesperado en la señalización de la reparación del ADN cuando falta otra proteína reparadora, XRCC1.
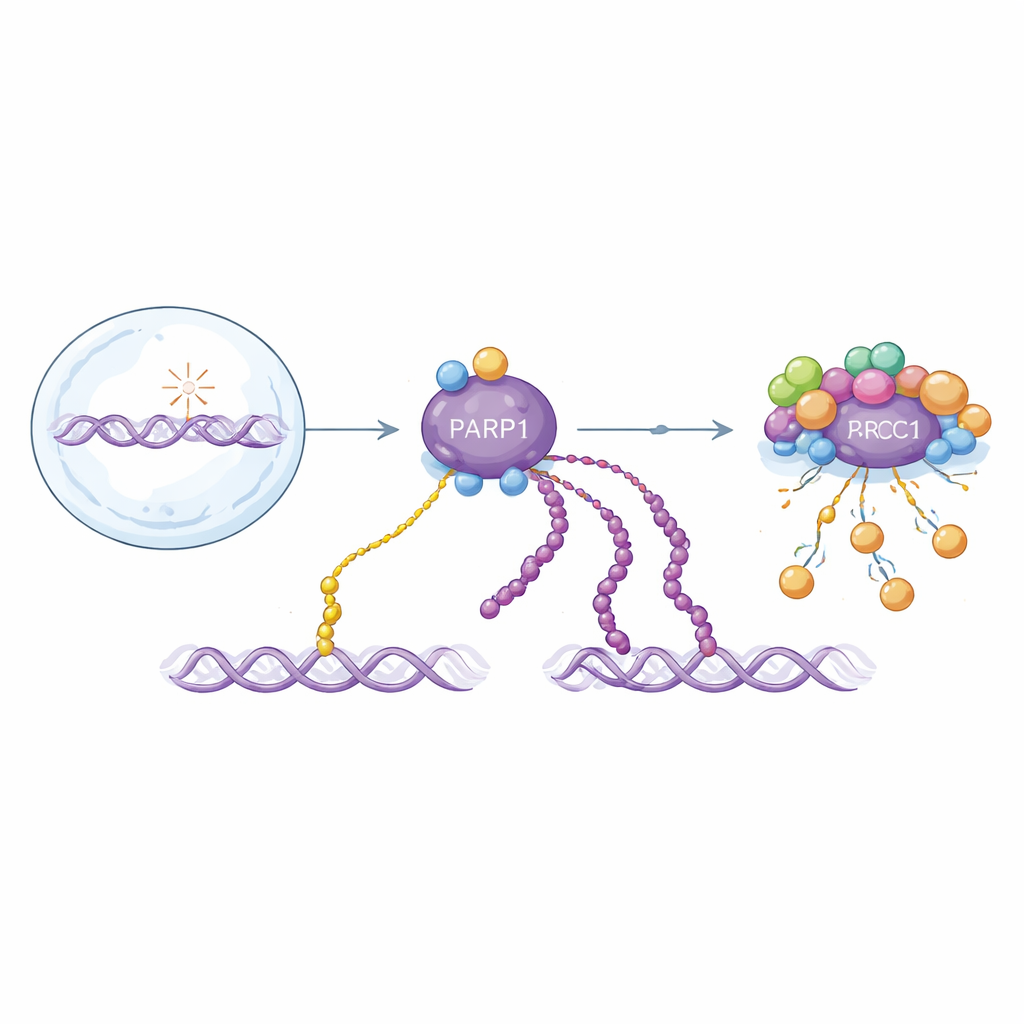
Dos versiones de una señal crítica de reparación del ADN
PARP1 responde a las roturas de la hebra de ADN añadiendo unidades de ADP-ribosa a sí mismo y a otras proteínas. Estas modificaciones existen como unidades simples (mono-ADP-ribosilación) o como cadenas largas (poli-ADP-ribosilación). Ambas formas ayudan a organizar la reparación, pero se comportan de manera diferente en el tiempo: las cadenas largas aparecen en un estallido inicial rápido y se eliminan con rapidez, mientras que las unidades simples se acumulan más lentamente y persisten por más tiempo. Dado que ambas formas se construyen a partir del mismo bloque de construcción, la mayoría de los métodos de detección existentes las confunden. Eso dificulta entender cómo contribuye cada una a la salud y la enfermedad, o cómo funcionan realmente los fármacos que apuntan a PARP1.
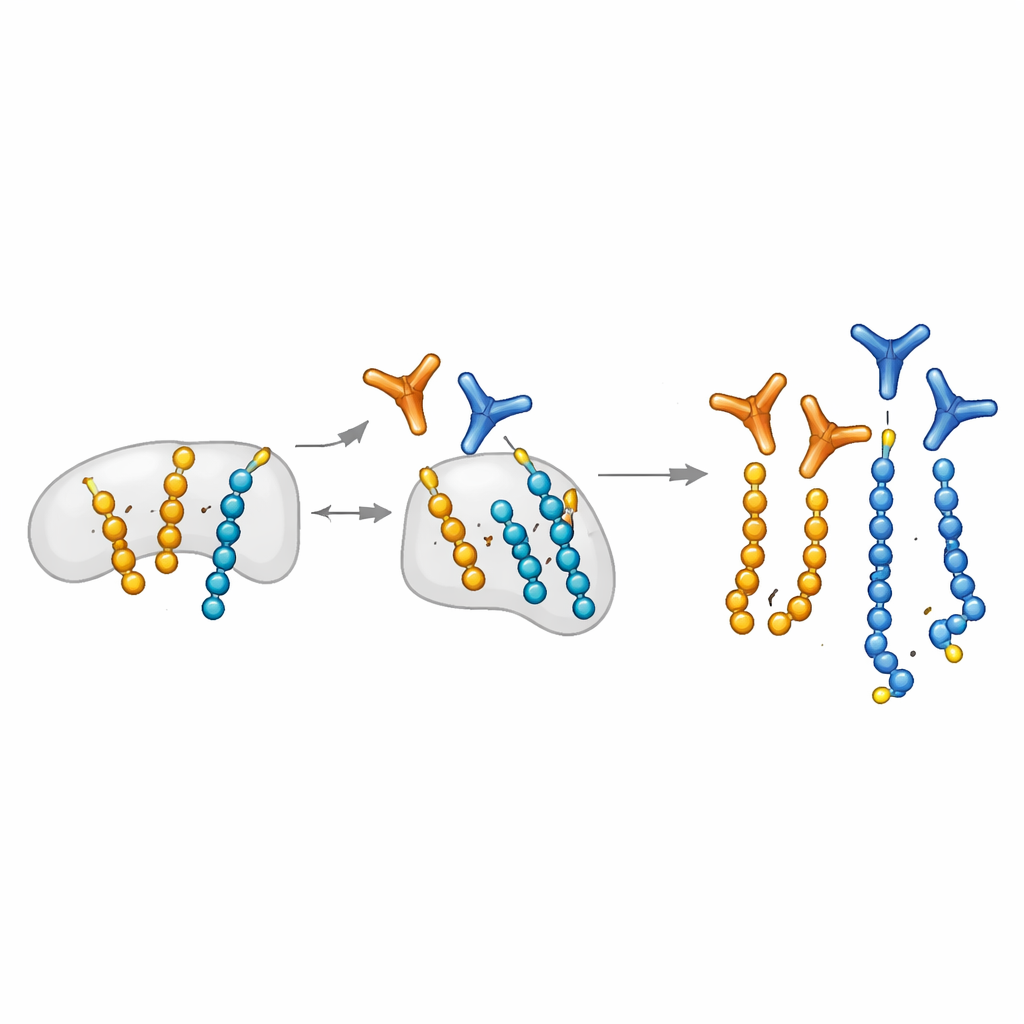
Ingeniería de “ojos” moleculares altamente selectivos
Los autores amplían una plataforma de biología química que puede colocar programáticamente ADP-ribosa en residuos de serina específicos de péptidos cortos. Usan estos péptidos hechos a medida como cebo para capturar fragmentos de anticuerpos de grandes bibliotecas de display. De forma crucial, introducen un paso de “bloqueo mono”: los péptidos mono-modificados se usan para absorber anticuerpos que reconocen unidades simples, dejando candidatos que prefieren las cadenas largas. Esta estrategia produce anticuerpos modulares que, una vez ensamblados mediante un sistema SpyTag/SpyCatcher, pueden convertirse rápidamente en distintos formatos para Western blots, microscopía y pull-downs. El equipo también descubre un patrón distintivo de iones fragmentarios en espectrometría de masas que marca específicamente péptidos que llevan dos unidades de ADP-ribosa, ayudando a mapear correctamente dónde ocurren las poli-modificaciones en las proteínas.
Ver señales sutiles donde otros no ven nada
Con sus nuevas herramientas, los investigadores muestran que los anticuerpos poli-específicos detectan cadenas muy cortas, cadenas largas e incluso polímeros libres de ADP-ribosa, y lo hacen con mucha más sensibilidad que los reactivos comerciales existentes. Los anticuerpos funcionan con distintos enlaces a aminoácidos, no solo serina, y pueden visualizar poli-ADP-ribosa en células en condiciones donde las herramientas anteriores no detectaban señal alguna, por ejemplo en células sin estrés o en células en bajo oxígeno. Paralelamente, el equipo madura por afinidad anticuerpos mono-específicos y específicos de sitio previos para aumentar su sensibilidad sin perder selectividad. Juntas, estas herramientas permiten la imagen simultánea de señales mono y poli en la misma célula, revelando que la poli-modificación aparece en focos nucleares localizados mientras que la mono-modificación forma una onda más difusa y duradera a través de la cromatina.
Cómo la pérdida de XRCC1 remodela las olas de reparación del ADN
XRCC1 actúa normalmente como un andamiaje que ayuda a PARP1 a engancharse y luego desengancharse de los intermediarios de reparación del ADN. Cuando XRCC1 se pierde, PARP1 se vuelve hiperactivo y se sabe que sobreproduce largas cadenas de ADP-ribosa, un estado vinculado a la neurodegeneración. Usando su conjunto refinado de anticuerpos, los autores muestran que la pérdida de XRCC1 hace más que aumentar las cadenas largas: amplifica de forma impresionante también la onda de mono-ADP-ribosilación. Durante un daño continuo del ADN provocado por distintos agentes, las células carentes de XRCC1 muestran picos más altos y tempranos de ambas modificaciones, largas y cortas, con temporizaciones específicas según el tipo de daño. La mono-modificación suele permanecer más estable y homogéneamente distribuida que la señal poli, que fluctúa rápidamente. El trabajo también identifica a la histona H1 como un blanco mono-modificado prominente cuya etiquetación persistente podría mantener la cromatina más relajada alrededor de las lesiones.
De señales alteradas a tráfico proteico alterado
La mono-ADP-ribosa sobre serina puede a su vez ser decorada por un enlace químico inusual a ubiquitina, formando una marca híbrida llamada ADP-ribosil-ubiquitinación. La ligasa de ubiquitina RNF114 reconoce esta señal compuesta y se atrae a los sitios de daño en el ADN donde puede modificar o desplazar otras proteínas. Usando una proteína lectora especializada (ZUD) junto con sus anticuerpos, los autores muestran que la deficiencia de XRCC1 aumenta no solo la mono-ADP-ribosa, sino también esta marca híbrida y el reclutamiento de RNF114 a las roturas. Esto sugiere que la desregulación de la señal mono y su entrecruzamiento con ubiquitina pueden contribuir al estrés celular y a los fenotipos de enfermedad observados cuando XRCC1 está mutado.
Qué significa esto para entender y tratar la enfermedad
Para un público no especializado, el mensaje clave es que lo que antes parecía una única señal de reparación del ADN son en realidad dos olas superpuestas de pequeñas etiquetas químicas, cada una con su propia temporalidad y consecuencias. Al construir herramientas moleculares altamente selectivas, este estudio separa esas olas y muestra que la pérdida de XRCC1 intensifica no solo el conocido estallido de cadenas largas sino también un aumento sostenido de etiquetas de una sola unidad y sus marcas unidas a ubiquitina. Estos hallazgos refinan nuestra comprensión de cómo funciona PARP1, ayudan a explicar por qué los defectos en XRCC1 y enzimas relacionadas causan enfermedades cerebrales, y proporcionan una caja de herramientas que otros investigadores pueden usar para diseccionar la ADP-ribosilación en cáncer, inmunidad y más allá — potencialmente conduciendo a un uso más preciso de los fármacos que se dirigen a PARP.
Cita: Dauben, H., Mihaljević, M., Kolvenbach, A. et al. Versatile and sensitive detection of mono- and poly(ADP-ribosyl)ation reveals XRCC1-dependent remodelling of PARP1 signalling. Nat Commun 17, 3216 (2026). https://doi.org/10.1038/s41467-026-71311-4
Palabras clave: ADP-ribosilación, reparación del daño del ADN, señalización de PARP1, deficiencia de XRCC1, ubiquitinación