Clear Sky Science · it
Rilevamento versatile e sensibile della mono- e poli(ADP-ribosil)azione rivela il rimodellamento dipendente da XRCC1 della segnalazione PARP1
Perché piccole etichette chimiche sul nostro sistema di riparazione del DNA contano
Ogni cellula del nostro corpo sta continuamente riparando i danni al proprio DNA. Se questa riparazione fallisce, il risultato può essere cancro, neurodegenerazione o morte cellulare. Un attore chiave in questa rete di riparazione è una proteina chiamata PARP1, che si decorata sé stessa e le proteine vicine con piccole etichette simili a zuccheri derivate dal NAD+. Queste etichette esistono in forme corte e lunghe e funzionano come segnali che richiamano altri fattori di riparazione. Finora, gli scienziati sono mancati di strumenti precisi per vedere e distinguere questi diversi tipi di etichette all’interno delle cellule, specialmente durante la malattia. Questo studio costruisce tali strumenti e li usa per rivelare un cambiamento inatteso nella segnalazione della riparazione del DNA quando un altro fattore di riparazione, XRCC1, è assente.
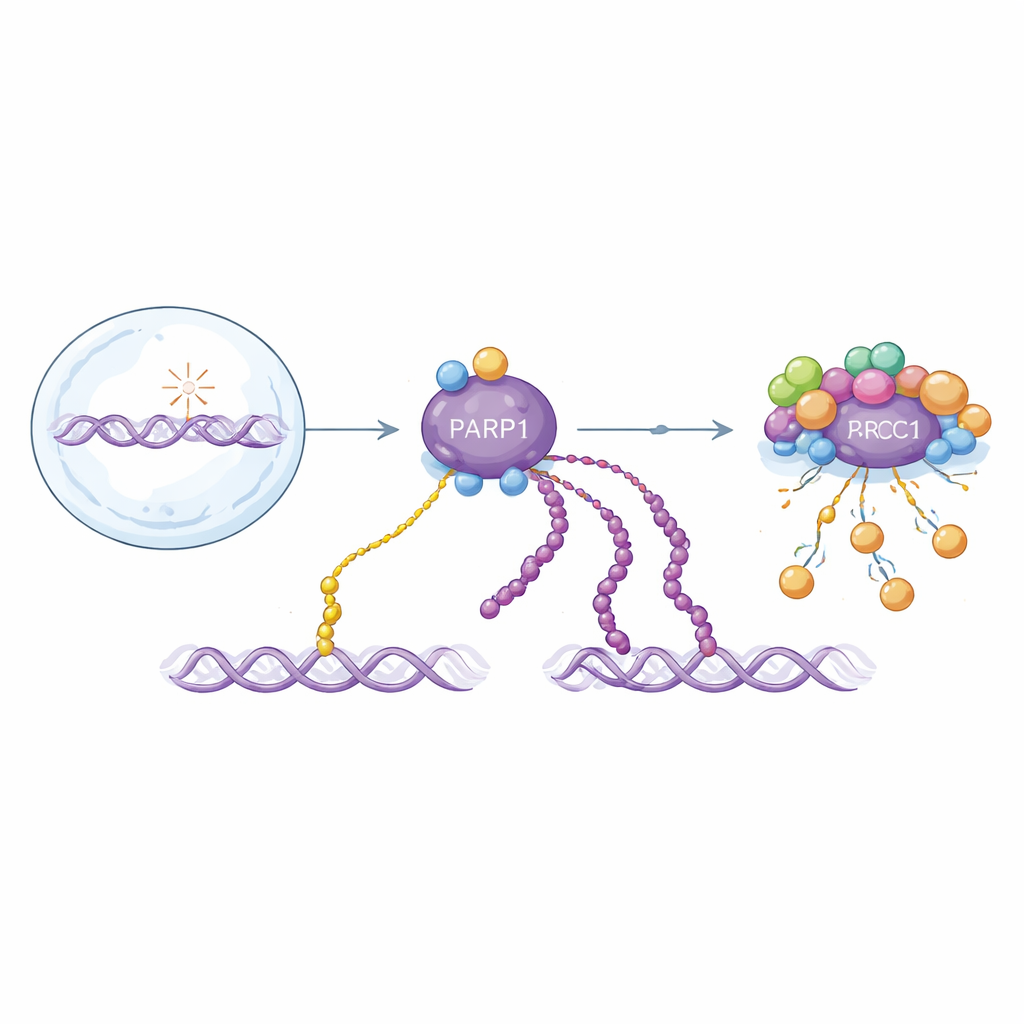
Due versioni di un segnale critico per la riparazione del DNA
PARP1 risponde alle rotture dei filamenti di DNA attaccando unità di ADP-ribosio a sé stesso e ad altre proteine. Queste modificazioni esistono come unità singole (mono-ADP-ribosilazione) o come catene lunghe (poli-ADP-ribosilazione). Entrambe le forme aiutano a organizzare la riparazione, ma si comportano diversamente nel tempo: le catene lunghe compaiono in un rapido impulso iniziale e vengono rimosse in fretta, mentre le unità singole si accumulano più lentamente e persistono più a lungo. Poiché entrambe le forme sono costruite dallo stesso mattoncino, la maggior parte dei metodi di rilevamento esistenti le confonde. Questo rende difficile capire come ciascuna contribuisca alla salute e alla malattia, o come funzionino veramente i farmaci che prendono di mira PARP1.
Progettare “occhi” molecolari altamente selettivi
Gli autori ampliano una piattaforma di biologia chimica che può posizionare in modo programmabile l’ADP-ribosio su specifici residui di serina di brevi peptidi. Usano questi peptidi su misura come esca per pescare frammenti di anticorpi da grandi librerie display. Cruciale è l’introduzione di un passaggio di “blocco mono”: i peptidi mono-modificati vengono usati per assorbire gli anticorpi che riconoscono unità singole, lasciando indietro i candidati che preferiscono le catene lunghe. Questa strategia produce anticorpi modulari che, una volta assemblati usando il sistema SpyTag/SpyCatcher, possono essere rapidamente convertiti in diversi formati per blot, microscopia e pull-down. Il team scopre anche un pattern distintivo di ioni frammento nella spettrometria di massa che marca specificamente i peptidi portatori di due unità di ADP-ribosio, aiutando a mappare correttamente dove avvengono le poli-modificazioni sulle proteine.
Vedere segnali sottili dove altri non vedono nulla
Con i loro nuovi strumenti, i ricercatori mostrano che gli anticorpi polifunzionali rilevano catene molto corte, catene lunghe e persino polimeri di ADP-ribosio liberi, e lo fanno con una sensibilità molto maggiore rispetto ai reagenti commerciali esistenti. Gli anticorpi funzionano su diversi legami aminoacidici, non solo sulla serina, e possono visualizzare il poli-ADP-ribosio nelle cellule in condizioni in cui gli strumenti precedenti non rilevavano alcun segnale, come in cellule non stressate o in condizioni di bassa ossigenazione. Parallelamente, il gruppo affina per affinità anticorpi mono-specifici e site-specific precedenti per aumentare la loro sensibilità mantenendo la selettività. Insieme, questa cassetta di strumenti permette l’imaging simultaneo sia dei segnali mono sia di quelli poli nella stessa cellula, rivelando che la poli-modificazione appare in foci nucleari localizzati mentre la mono-modificazione forma un’onda più diffusa e di più lunga durata attraverso la cromatina.
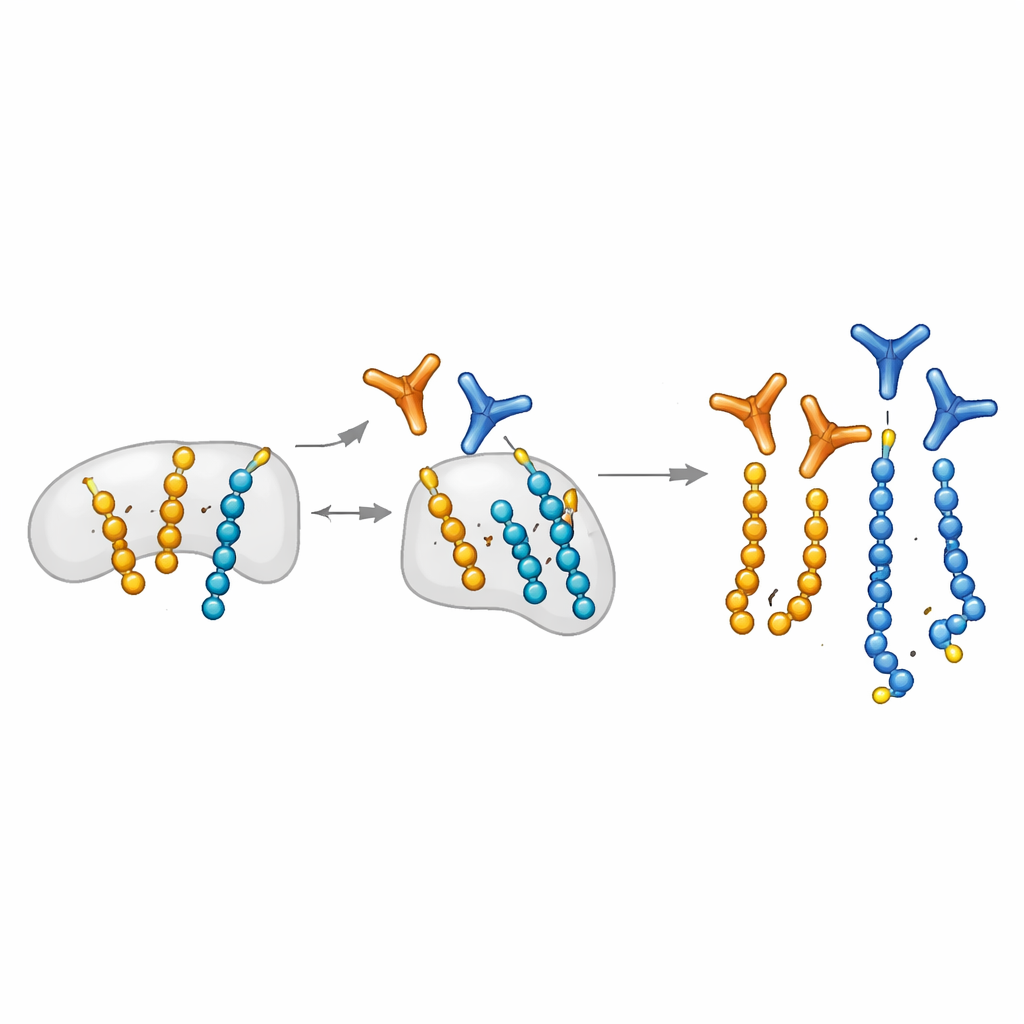
Come la perdita di XRCC1 rimodella le onde di riparazione del DNA
XRCC1 normalmente agisce come impalcatura che aiuta PARP1 a impegnarsi e poi disimpegnarsi dagli intermedi di riparazione del DNA. Quando XRCC1 viene perso, PARP1 diventa iperattivo ed è noto che sovraproduce catene lunghe di ADP-ribosio, uno stato collegato alla neurodegenerazione. Usando il loro set di anticorpi raffinato, gli autori mostrano che la perdita di XRCC1 non si limita ad aumentare le catene lunghe: amplifica in modo drammatico anche l’onda di mono-ADP-ribosilazione. Durante danni al DNA persistenti causati da diversi agenti, le cellule prive di XRCC1 mostrano picchi più alti e più precoci di entrambe le modificazioni, lunghe e corte, con tempistiche specifiche al tipo di danno. La mono-modificazione spesso rimane più stabile e distribuita in modo più omogeneo rispetto al segnale poli che fluttua rapidamente. Il lavoro identifica inoltre l’istone H1 come un target mono-modificato prominente la cui marcatura persistente potrebbe mantenere la cromatina più rilassata intorno alle lesioni.
Dai segnali alterati al traffico proteico alterato
La mono-ADP-ribosio sulla serina può a sua volta essere ulteriormente decorata da un insolito legame chimico all’ubiquitina, formando un marchio ibrido chiamato ADP-ribosil-ubiquitinazione. L’enzima ligasi di ubiquitina RNF114 riconosce questo segnale composito ed è richiamato nei siti di danno al DNA dove può modificare o spostare altre proteine. Usando una proteina reader specializzata (ZUD) insieme ai loro anticorpi, gli autori mostrano che la carenza di XRCC1 aumenta non solo il mono-ADP-ribosio, ma anche questo marchio ibrido e il reclutamento di RNF114 alle rotture. Ciò suggerisce che la disregolazione della segnalazione mono e il suo crosstalk con l’ubiquitinazione possono contribuire allo stress cellulare e ai fenotipi patologici osservati quando XRCC1 è mutato.
Cosa significa per la comprensione e il trattamento delle malattie
Per un non specialista, il messaggio chiave è che ciò che una volta sembrava un unico segnale di riparazione del DNA sono in realtà due onde sovrapposte di piccole etichette chimiche, ciascuna con tempistiche e conseguenze proprie. Costruendo strumenti molecolari altamente selettivi, questo studio separa quelle onde e mostra che la perdita di XRCC1 intensifica non solo il noto impulso di catene lunghe ma anche un’ondata sostenuta di etichette a unità singola e dei loro marchi connessi all’ubiquitina. Queste intuizioni raffinano la nostra comprensione del funzionamento di PARP1, aiutano a spiegare perché i difetti in XRCC1 e in enzimi correlati causano malattie cerebrali, e forniscono una cassetta di strumenti che altri ricercatori possono usare per dissezionare l’ADP-ribosilazione in cancro, immunità e oltre—potenzialmente conducendo a un uso più preciso dei farmaci che prendono di mira PARP.
Citazione: Dauben, H., Mihaljević, M., Kolvenbach, A. et al. Versatile and sensitive detection of mono- and poly(ADP-ribosyl)ation reveals XRCC1-dependent remodelling of PARP1 signalling. Nat Commun 17, 3216 (2026). https://doi.org/10.1038/s41467-026-71311-4
Parole chiave: ADP-ribosilazione, riparazione del danno al DNA, segnalazione PARP1, deficienza di XRCC1, ubiquitinazione