Clear Sky Science · ja
単一およびポリ(ADP-リボシル)化の多用途で高感度な検出により明らかになったXRCC1依存のPARP1シグナルの再編成
なぜDNA修復系の小さな化学タグが重要なのか
私たちの体のすべての細胞は常にDNAの損傷を修復しています。この修復がうまくいかないと、がんや神経変性、細胞死を引き起こすことがあります。修復ネットワークの主要因子の一つがPARP1というタンパク質で、これはNAD+由来の糖様の小さなタグを自身や近傍のタンパク質に付けます。これらのタグは短鎖と長鎖の形で存在し、他の修復因子を呼び寄せるシグナルとして機能します。これまで、特に疾患の文脈で細胞内のこれら異なるタグの種類を正確に識別して可視化する道具が不足していました。本研究はそのような道具を構築し、別の修復タンパク質であるXRCC1が欠損したときにDNA修復シグナルに生じる予期せぬ変化を明らかにします。
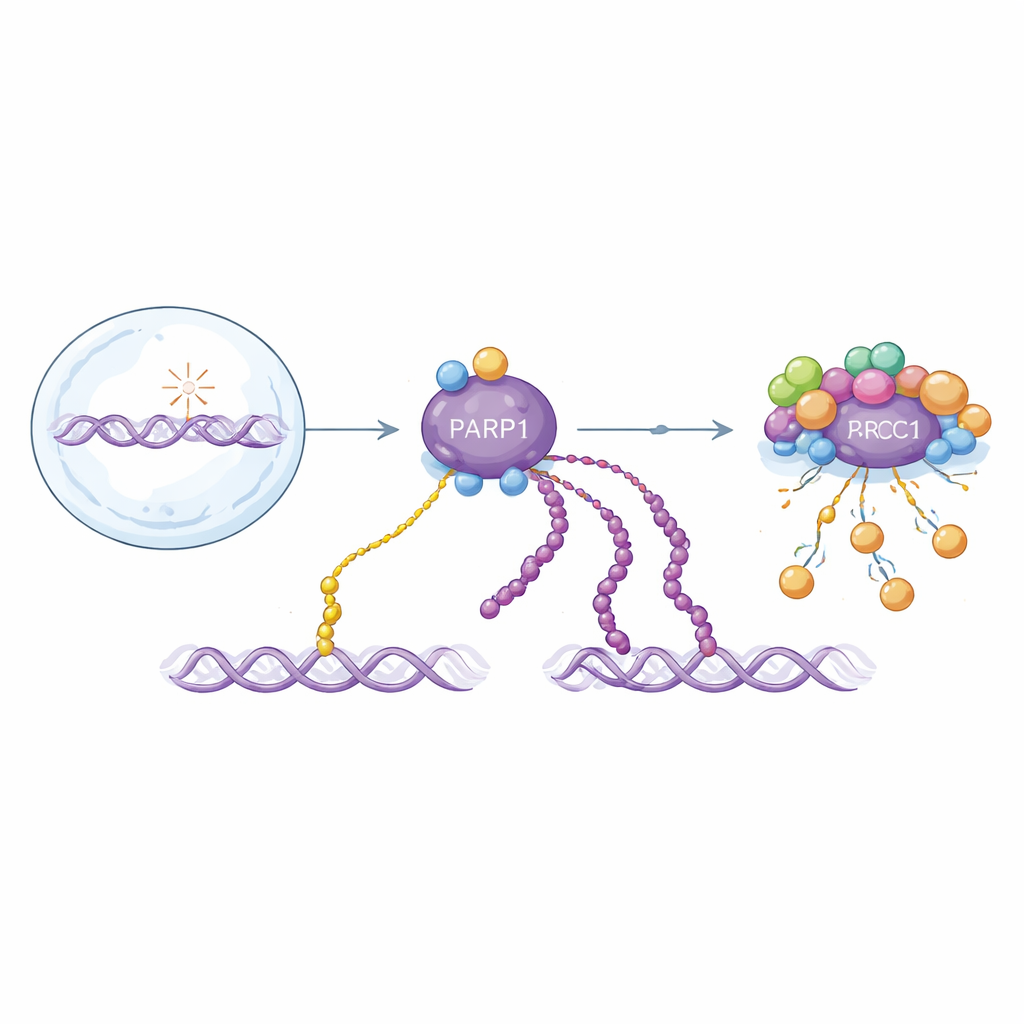
重要なDNA修復シグナルの二つの顔
PARP1はDNAの切断に応答して自身や他のタンパク質にADP-リボース単位を付加します。これらの修飾は単一単位(モノADP-リボシル化)として存在するか、あるいは長い鎖(ポリADP-リボシル化)として存在します。両者は修復の秩序化に寄与しますが、時間的挙動は異なります:長鎖は初期の急速なバーストで現れて速やかに除去され、一方で単一単位はゆっくり蓄積してより長く持続します。両者は同じ構成要素から作られるため、既存の多くの検出法はこれらを混同してしまいます。これにより、それぞれが健康や疾患にどう寄与するのか、あるいはPARP1を標的とする薬の正確な作用機序を理解することが困難になっています。
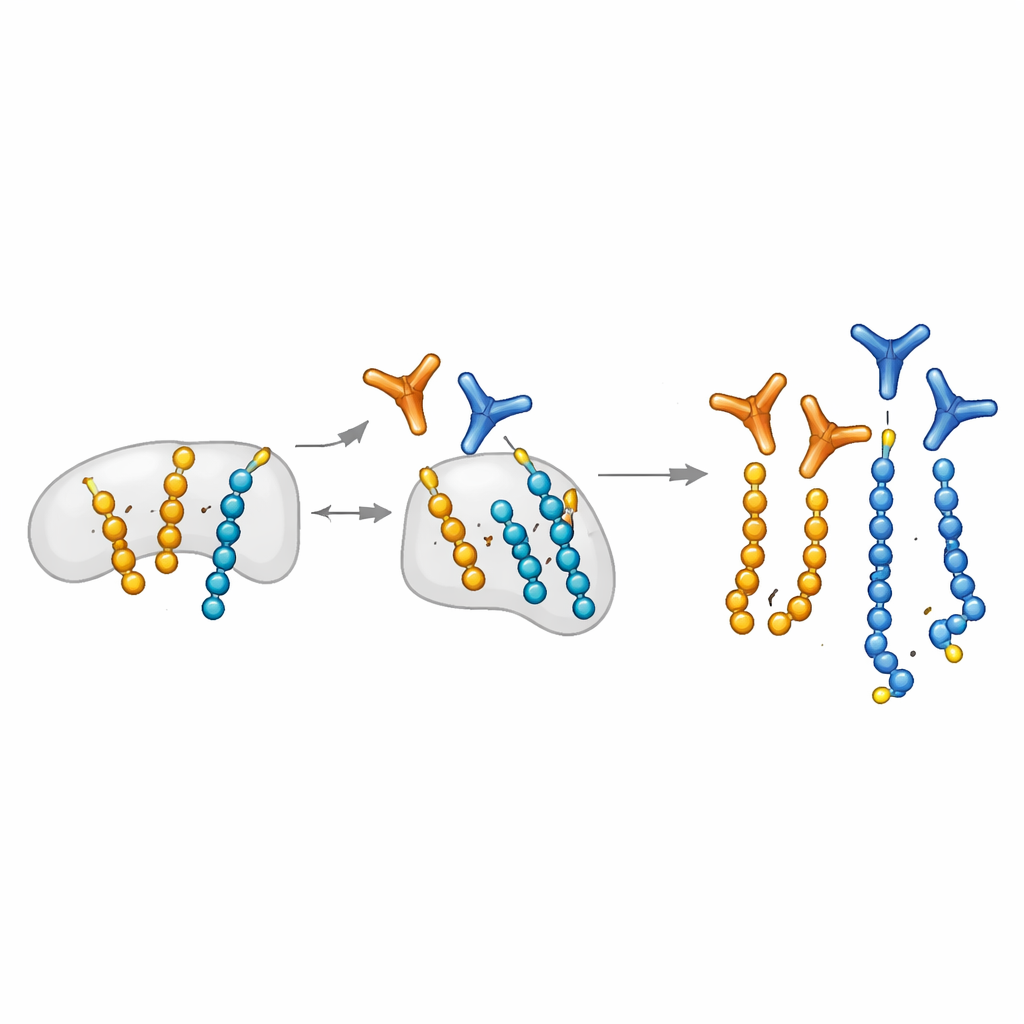
高選択性の分子“目”の設計
著者らは化学生物学プラットフォームを拡張し、短いペプチドの特定のセリン残基にプログラム的にADP-リボースを導入できるようにしました。これらのカスタムペプチドを餌として用い、大規模ディスプレイライブラリから抗体断片を漁り当てます。重要なのは「モノを遮断する」ステップを導入した点で、モノ修飾ペプチドを用いて単一単位を認識する抗体をあらかじめ吸着させ、長鎖を好む候補を残すようにしています。この戦略により、SpyTag/SpyCatcherシステムで組み立てられたモジュラーな抗体が得られ、ブロット、顕微鏡観察、プルダウン用に迅速に異なるフォーマットへ変換できます。さらに、質量分析で二つのADP-リボース単位を持つペプチドに特異的な断片イオンパターンを同定し、ポリ修飾がタンパク質のどこに起きているかを正確にマップする助けとしています。
従来は見えなかった微妙なシグナルの検出
新しい道具を用いて、研究者たちはポリ特異的抗体が非常に短い鎖、長鎖、さらには自由なADP-リボースポリマーまでも検出でき、既存の市販試薬よりはるかに高感度であることを示します。これらの抗体はセリン以外のアミノ酸結合様式にも対応し、従来のツールが全く信号を検出しなかった条件(ストレスのない細胞や低酸素で増殖する細胞など)でも細胞内のポリADP-リボースを可視化できます。同時に、著者らは以前のモノ特異的・部位特異的抗体をアフィニティ成熟させて感度を高めつつ選択性を維持しました。これらを組み合わせたツールボックスにより、同一細胞内でモノとポリの両方のシグナルを同時にイメージングでき、ポリ修飾は局在化した核内フォーカスに現れる一方で、モノ修飾はより拡散的で長く持続する波としてクロマチン全体に形成されることが明らかになりました。
XRCC1欠損がDNA修復の波をどう変えるか
XRCC1は通常、PARP1がDNA修復中間体に結合し、その後離れるのを助ける足場として機能します。XRCC1が失われるとPARP1は過剰に活性化し、長いADP-リボース鎖を過剰に生成することで知られており、これは神経変性と関連しています。精緻化された抗体セットを用いることで、著者らはXRCC1欠損が長鎖を増やすだけでなく、モノADP-リボシル化の波も劇的に増幅することを示します。さまざまな薬剤による持続的なDNA損傷のもとで、XRCC1欠損細胞は長短い修飾ともに高く早いピークを示し、そのタイミングは損傷の種類によって異なります。モノ修飾はしばしばより安定で均一に分布し、急速に変動するポリシグナルより持続することが多いです。さらに本研究は、ヒストンH1を持続的にモノ修飾される顕著なターゲットとして同定しており、その持続的なタグ付けが損傷周辺のクロマチンをより緩んだ状態に保つ可能性を示唆しています。
変化したシグナルがタンパク質の挙動をどう変えるか
セリン上のモノADP-リボースはさらにユニークな化学結合でユビキチンによって修飾され、ADPリボシル-ユビキチン化と呼ばれるハイブリッドマークを形成することがあります。ユビキチンリガーゼRNF114はこの複合シグナルを認識し、損傷部位へ呼び寄せられて他のタンパク質を修飾したり移動させたりする可能性があります。専門のリーダータンパク質(ZUD)と抗体を併用して、著者らはXRCC1欠損がモノADP-リボースだけでなくこのハイブリッドマークとRNF114の損傷部位への動員も増加させることを示します。これは、モノシグナルの誤制御とそのユビキチンとのクロストークが、XRCC1が変異した際に見られる細胞ストレスや疾患表現型に寄与している可能性を示唆します。
疾患理解と治療への示唆
専門外の方に向けた要点は、かつて単一に見えたDNA修復シグナルが、実際には時間軸と結果が異なる二つの重なり合う波であるということです。極めて選択的な分子ツールを構築することにより、本研究はこれらの波を分離し、XRCC1の喪失がよく知られた長鎖のバーストを増強するだけでなく、持続する単一単位の急増およびそれに結びつくユビキチンマークも強めることを示しました。これらの知見はPARP1の働き方を再定義し、XRCC1や関連酵素の欠陥が脳疾患を引き起こす理由を説明する助けとなり、がん、免疫、その他の領域でADP-リボシル化を解析するためのツールキットを提供します。将来的にはより精密なPARP標的薬の利用につながる可能性があります。
引用: Dauben, H., Mihaljević, M., Kolvenbach, A. et al. Versatile and sensitive detection of mono- and poly(ADP-ribosyl)ation reveals XRCC1-dependent remodelling of PARP1 signalling. Nat Commun 17, 3216 (2026). https://doi.org/10.1038/s41467-026-71311-4
キーワード: ADP-リボシル化, DNA損傷修復, PARP1シグナル, XRCC1欠損, ユビキチン化