Clear Sky Science · de
Vielseitige und empfindliche Erkennung von Mono- und Poly(ADP-ribosyl)ierung deckt XRCC1-abhängige Umbauten der PARP1-Signalgebung auf
Warum winzige chemische Markierungen an unserem DNA-Reparatursystem wichtig sind
Jede Zelle in unserem Körper repariert ständig Schäden an ihrer DNA. Wenn diese Reparatur fehlgeht, kann das zu Krebs, Neurodegeneration oder Zelltod führen. Ein zentraler Akteur in diesem Reparaturnetzwerk ist das Protein PARP1, das sich selbst und benachbarte Proteine mit kleinen, zuckerähnlichen Anhängseln aus NAD+ versieht. Diese Anhängsel kommen in kurzen und langen Formen vor und fungieren als Signale, die weitere Reparaturfaktoren herbeirufen. Bislang fehlten den Forschern präzise Werkzeuge, um diese unterschiedlichen Markierungsformen innerhalb von Zellen zu sehen und zu unterscheiden, besonders im Krankheitskontext. Diese Studie baut solche Werkzeuge und nutzt sie, um eine unerwartete Veränderung in der DNA-Reparatursignalgebung aufzuzeigen, wenn ein anderes Reparaturprotein, XRCC1, fehlt.
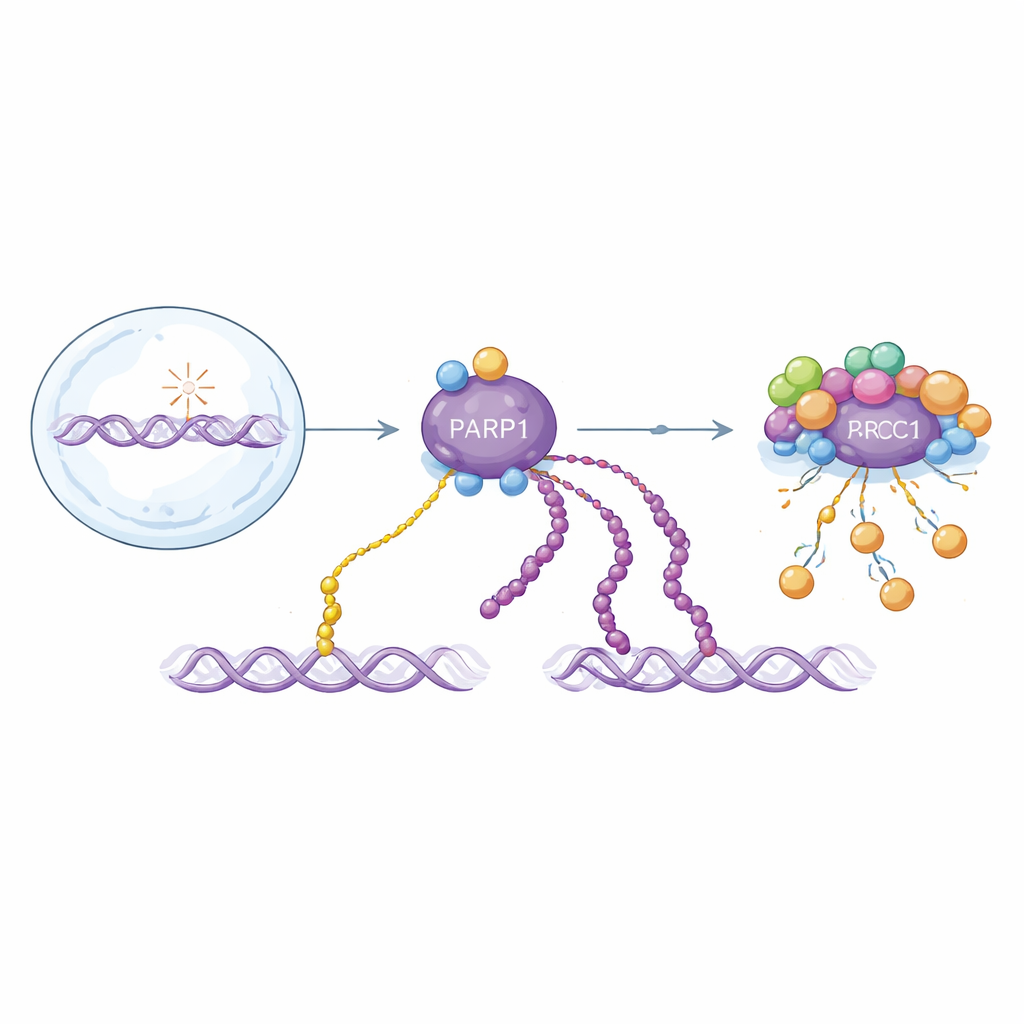
Zwei Varianten eines wichtigen DNA-Reparatursignals
PARP1 reagiert auf DNA-Strangbrüche, indem es ADP-Ribose-Einheiten an sich selbst und andere Proteine anhängt. Diese Modifikationen existieren als Einzelbausteine (Mono-ADP-Ribosylierung) oder als lange Ketten (Poly-ADP-Ribosylierung). Beide Formen helfen bei der Organisation der Reparatur, verhalten sich jedoch zeitlich unterschiedlich: Lange Ketten treten in einem schnellen Anfangsstoß auf und werden rasch entfernt, während Einzelbausteine langsamer zunehmen und länger bestehen bleiben. Da beide Formen aus demselben Baustein aufgebaut sind, vermischen die meisten bestehenden Nachweismethoden sie. Das erschwert das Verständnis, wie jede Form zur Gesundheit und Krankheit beiträgt oder wie Medikamente, die auf PARP1 abzielen, tatsächlich wirken.
Entwicklung hochselektiver molekularer „Augen“
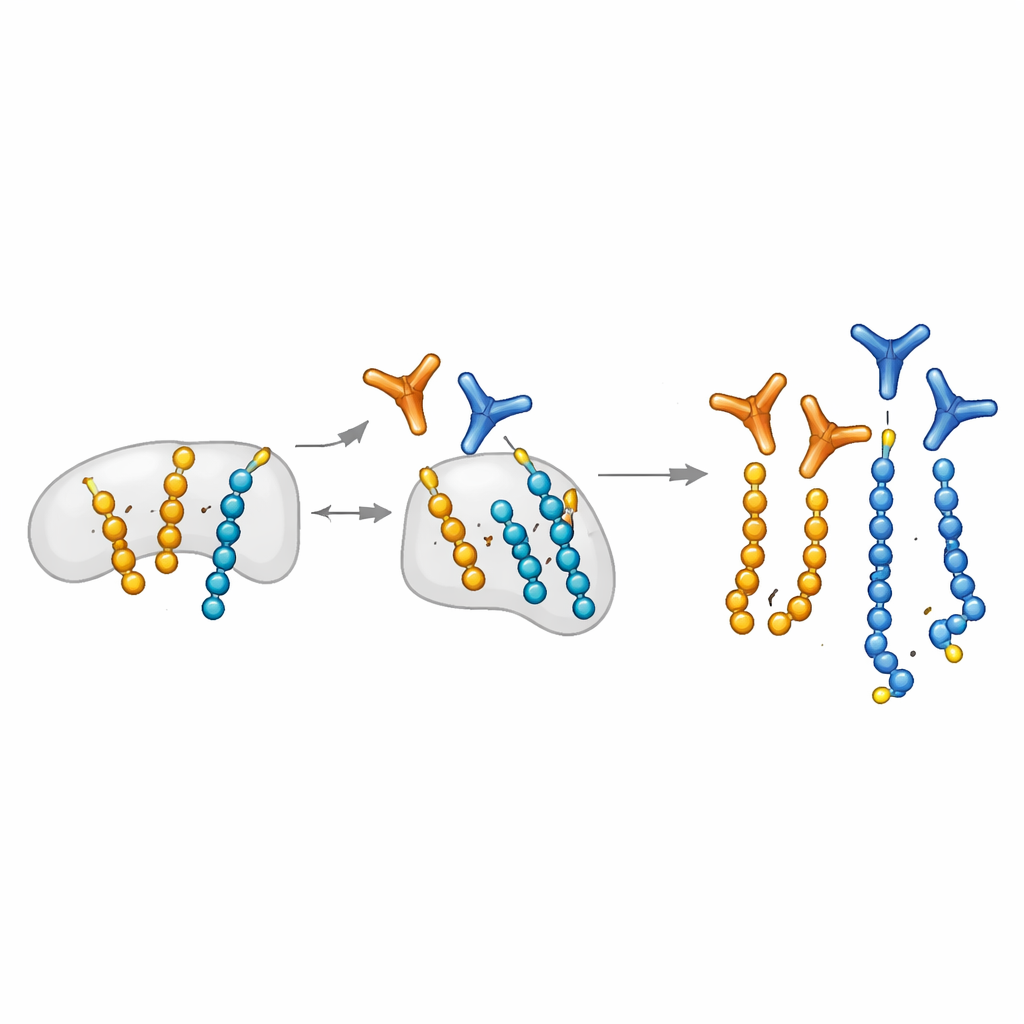
Die Autoren erweitern eine chemisch-biologische Plattform, die programmatisch ADP-Ribose auf bestimmte Serinreste kurzer Peptide platzieren kann. Diese maßgeschneiderten Peptide verwenden sie als Köder, um Antikörperfragmente aus großen Display-Bibliotheken herauszufischen. Entscheidend ist ein „Mono-Blockierschritt“: Mono-modifizierte Peptide werden eingesetzt, um Antikörper zu binden, die Einzelbausteine erkennen, wodurch Kandidaten übrig bleiben, die Ketten bevorzugen. Diese Strategie liefert modulare Antikörper, die nach Zusammenbau mittels eines SpyTag/SpyCatcher-Systems schnell in verschiedene Formate für Westerns, Mikroskopie und Pull-downs umgewandelt werden können. Das Team entdeckt außerdem ein charakteristisches Muster von Fragmentionen in der Massenspektrometrie, das spezifisch Peptide mit zwei ADP-Ribose-Einheiten markiert und so hilft, korrekt zuzuordnen, wo Poly-Modifikationen auf Proteinen vorkommen.
Feine Signale sehen, wo andere nichts sehen
Mit ihren neuen Werkzeugen zeigen die Forschenden, dass die poly-spezifischen Antikörper sehr kurze Ketten, lange Ketten und sogar freie ADP-Ribose-Polymere erkennen und dies mit deutlich höherer Empfindlichkeit als vorhandene kommerzielle Reagenzien. Die Antikörper funktionieren über verschiedene Aminosäure-Verknüpfungen hinweg, nicht nur Serin, und können Poly-ADP-Ribose in Zellen sichtbar machen unter Bedingungen, bei denen frühere Werkzeuge kein Signal zeigten — etwa in ungestressten Zellen oder Zellen, die in niedrigem Sauerstoff wachsen. Parallel dazu verbessert das Team durch Affinitätsreifung frühere mono-spezifische und positionsspezifische Antikörper, um ihre Empfindlichkeit zu erhöhen, ohne die Selektivität zu verlieren. Zusammen ermöglicht dieses Werkzeugset die gleichzeitige Abbildung von Mono- und Poly-Signalen in derselben Zelle und zeigt, dass Poly-Modifikation in lokalisierten nukleären Foci auftritt, während Mono-Modifikation eine diffusere und länger anhaltende Welle über das Chromatin bildet.
Wie der Verlust von XRCC1 die Reparaturwellen umgestaltet
XRCC1 fungiert normalerweise als Gerüst, das PARP1 hilft, sich an DNA-Reparaturzwischenprodukten zu binden und sich anschließend wieder zu lösen. Geht XRCC1 verloren, wird PARP1 hyperaktiv und ist dafür bekannt, vermehrt lange ADP-Ribose-Ketten zu produzieren — ein Zustand, der mit Neurodegeneration in Verbindung gebracht wird. Mit ihrem verfeinerten Antikörper-Set zeigen die Autoren, dass der Verlust von XRCC1 mehr bewirkt als nur die Zunahme langer Ketten: Er verstärkt dramatisch auch die Mono-ADP-Ribosylierungswelle. Bei andauernden DNA-Schäden durch verschiedene Agenzien zeigen Zellen ohne XRCC1 höhere und frühere Spitzen sowohl langer als auch kurzer Modifikationen, mit schadensspezifischem Timing. Mono-Modifikation bleibt oft stabiler und homogener verteilt als das schnell schwankende Poly-Signal. Die Arbeit identifiziert außerdem Histon H1 als ein prominentes mono-modifiziertes Ziel, dessen anhaltende Markierung das Chromatin um Läsionen möglicherweise lockerer hält.
Von veränderten Signalen zu verändertem Proteinverkehr
Mono-ADP-Ribose an Serin kann selbst weiter durch eine ungewöhnliche chemische Verbindung mit Ubiquitin dekoriert werden und damit eine hybride Markierung bilden, die ADP-ribosyl-Ubiquitinierung genannt wird. Die Ubiquitin-Ligase RNF114 erkennt dieses Zusammensignal und wird zu DNA-Schadensstellen angezogen, wo sie möglicherweise andere Proteine modifizieren oder umverteilen kann. Mithilfe eines spezialisierten Leserproteins (ZUD) neben ihren Antikörpern zeigen die Autoren, dass XRCC1-Mangel nicht nur Mono-ADP-Ribose erhöht, sondern auch diese hybride Markierung und die Rekrutierung von RNF114 an Bruchstellen. Das legt nahe, dass fehlregulierte Mono-Signalgebung und deren Ubiquitin-Querkommunikation zu den zellulären Stress- und Krankheitsphänotypen beitragen können, die bei XRCC1-Mutationen beobachtet werden.
Was das für das Verständnis und die Behandlung von Krankheiten bedeutet
Für Nicht-Spezialisten lautet die Kernbotschaft, dass das, was einst wie ein einziges DNA-Reparatursignal erschien, tatsächlich zwei sich überlappende Wellen kleiner chemischer Markierungen sind, jede mit eigener Zeitdynamik und Konsequenzen. Durch den Bau hochselektiver molekularer Werkzeuge trennt diese Studie diese Wellen und zeigt, dass der Verlust von XRCC1 nicht nur den bekannten Anstoss langer Ketten verstärkt, sondern auch eine anhaltende Zunahme der Einzelbausteinsignale und deren verknüpfter Ubiquitin-Markierungen bewirkt. Diese Einsichten verfeinern unser Verständnis der PARP1-Funktion, helfen zu erklären, warum Defekte in XRCC1 und verwandten Enzymen zu Hirnerkrankungen führen, und bieten ein Toolkit, das andere Forschende nutzen können, um ADP-Ribosylierung bei Krebs, Immunität und darüber hinaus zu untersuchen — mit dem Potenzial für präzisere Anwendungen PARP-gerichteter Medikamente.
Zitation: Dauben, H., Mihaljević, M., Kolvenbach, A. et al. Versatile and sensitive detection of mono- and poly(ADP-ribosyl)ation reveals XRCC1-dependent remodelling of PARP1 signalling. Nat Commun 17, 3216 (2026). https://doi.org/10.1038/s41467-026-71311-4
Schlüsselwörter: ADP-Ribosylierung, DNA-Schadensreparatur, PARP1-Signalgebung, XRCC1-Mangel, Ubiquitinierung