Clear Sky Science · ru
Универсальное и чувствительное обнаружение моно- и поли(АДФ-рибозилирования) выявляет ремоделирование сигнализации PARP1, зависящее от XRCC1
Почему маленькие химические метки в системе ремонта ДНК важны
Каждая клетка нашего тела постоянно восстанавливает повреждения ДНК. Если этот процесс идёт неправильно, результатом могут быть рак, нейродегенерация или гибель клетки. Ключевым участником этой сети восстановления является белок PARP1, который помечает сам себя и соседние белки небольшими сахаро-подобными метками, образуемыми из NAD+. Эти метки бывают в коротком и длинном вариантах и действуют как сигналы, привлекающие другие факторы репарации. До сих пор у учёных не было точных инструментов, чтобы видеть и различать эти типы меток внутри клеток, особенно в условиях болезни. В этом исследовании созданы такие инструменты, и с их помощью выявлено неожиданное изменение сигнализации при отсутствии другого репарационного белка — XRCC1.
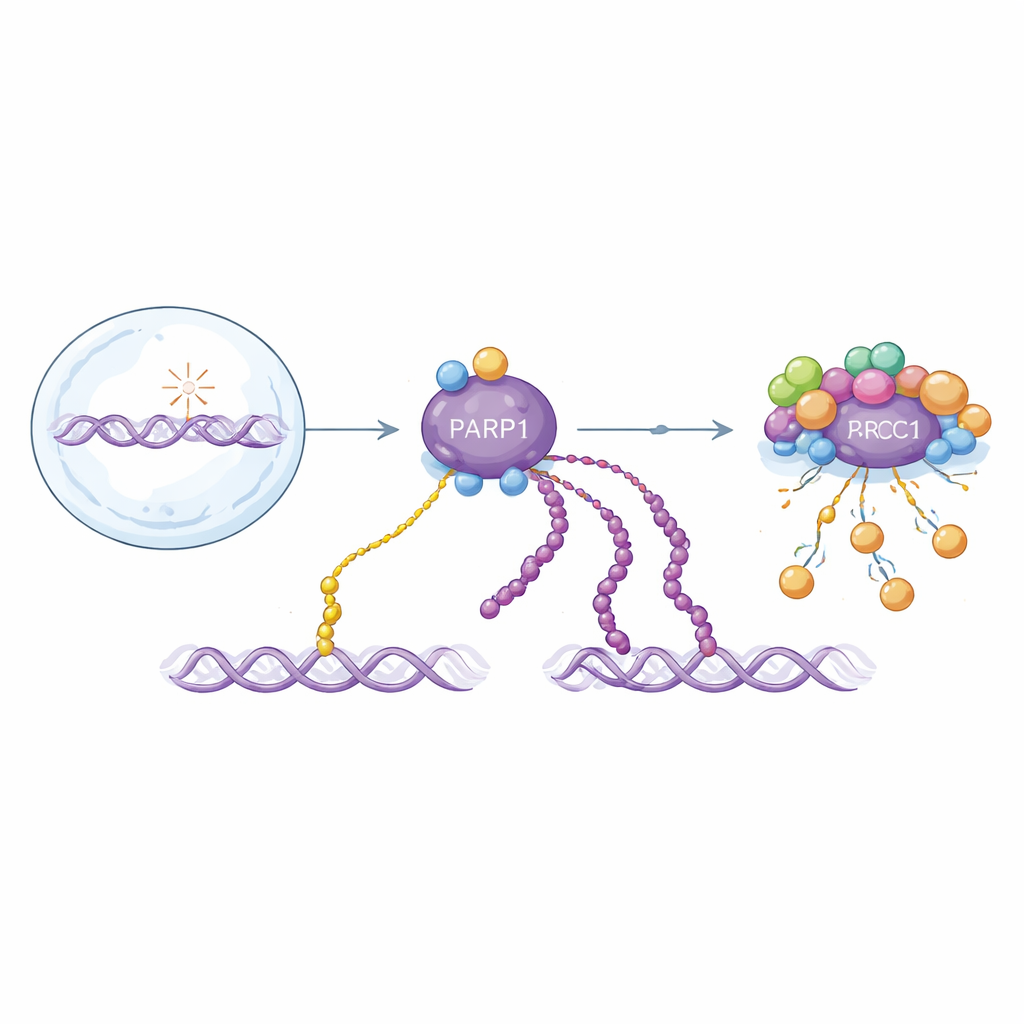
Два варианта критического сигнала ремонта ДНК
PARP1 реагирует на разрывы цепей ДНК присоединением звеньев АДФ-рибозы к себе и другим белкам. Эти модификации существуют в виде одиночных звеньев (моно-АДФ-рибозилирование) или длинных цепочек (поли-АДФ-рибозилирование). Оба типа помогают организовать ремонт, но ведут себя по-разному во времени: длинные цепочки появляются в быстром начальном всплеске и быстро удаляются, тогда как одиночные звенья накапливаются медленнее и дольше сохраняются. Поскольку оба варианта собираются из одного и того же строительного блока, большинство существующих методов обнаружения смешивает их вместе. Это затрудняет понимание вклада каждого из них в здоровье и болезнь, а также механизма действия лекарств, нацеленных на PARP1.
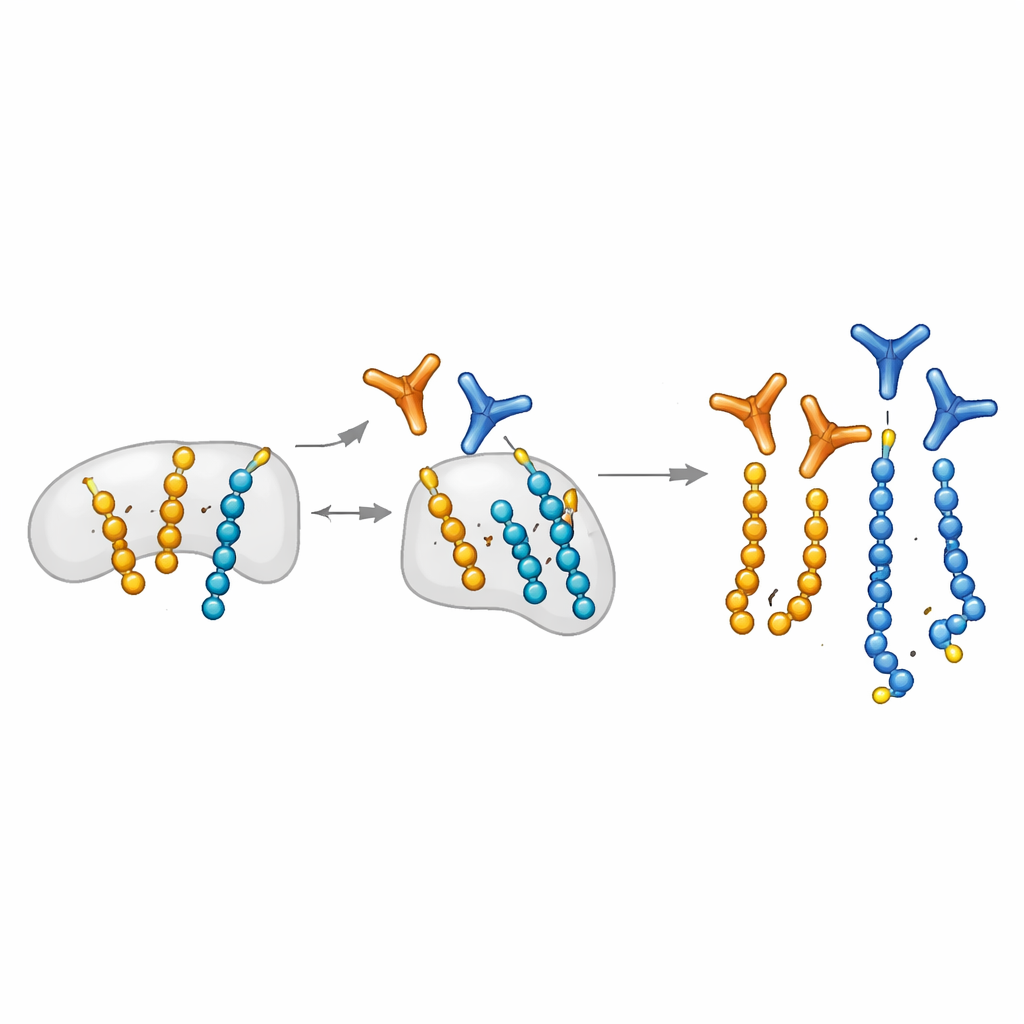
Создание высокоспецифичных молекулярных «глаз»
Авторы расширяют платформу химической биологии, которая программируемо размещает АДФ-рибозу на определённых сериновых остатках коротких пептидов. Эти индивидуально изготовленные пептиды используют как приманку для отлова фрагментов антител из больших библиотек. Критически важным является введение шага «блокировки моно»: пептиды с моно-модификацией используются для поглощения антител, распознающих одиночные звенья, оставляя кандидатов, предпочитающих длинные цепочки. Такая стратегия даёт модульные антитела, которые, собранные с помощью системы SpyTag/SpyCatcher, могут быстро переводиться в разные форматы для вестерн-блоттинга, микроскопии и вытягивания белков. Команда также обнаруживает характерный рисунок фрагментов в масс-спектрометрии, который специфически маркирует пептиды с двумя АДФ-рибозными звеньями, что помогает правильно картировать места поли-модификаций на белках.
Видеть тонкие сигналы там, где раньше их не замечали
С помощью новых инструментов исследователи показывают, что поли-специфичные антитела обнаруживают очень короткие цепочки, длинные цепочки и даже свободные полимеры АДФ-рибозы, и делают это с гораздо большей чувствительностью, чем существующие коммерческие реагенты. Антитела работают через разные аминокислотные связи, не только через серин, и могут визуализировать поли-АДФ-рибозу в клетках в условиях, где предыдущие инструменты не давали сигнала, например в нестрессовых клетках или при низком содержании кислорода. Параллельно команда аффинной зрелости улучшает ранее созданные моно-специфичные и сайт-специфичные антитела, повышая их чувствительность при сохранении селективности. В совокупности этот набор инструментов позволяет одновременно визуализировать как моно-, так и поли-сигналы в одной клетке, показывая, что поли-модификация возникает в локализованных ядерных фокусах, тогда как моно-модификация формирует более диффузную и долгоживущую волну по хроматину.
Как потеря XRCC1 перекраивает волны ремонта ДНК
XRCC1 обычно действует как каркасный белок, помогающий PARP1 взаимодействовать с промежуточными продуктами ремонта и затем отключаться от них. При потере XRCC1 PARP1 становится гиперактивным и, как известно, может чрезмерно продуцировать длинные цепочки АДФ-рибозы — состояние, связанное с нейродегенерацией. Используя свой усовершенствованный набор антител, авторы показывают, что потеря XRCC1 делает не только усиление длинных цепочек: она драматически усиливает и волну моно-АДФ-рибозилирования. При продолжающемся повреждении ДНК разными агентами клетки без XRCC1 демонстрируют более высокие и более ранние пики как длинных, так и коротких модификаций, с временными особенностями, зависящими от типа повреждения. Часто моно-модификация остаётся более стабильной и равномерно распределённой по сравнению с быстро изменяющимся поли-сигналом. Работа также идентифицирует гистон H1 как заметную мишень с моно-модификацией, чья постоянная пометка может поддерживать хроматин в более разрыхлённом состоянии вокруг очагов повреждений.
От изменённых сигналов к изменённому движению белков
Моно-АДФ-рибоза на серине сама по себе может дальше модифицироваться необычной связью с убиквитином, образуя гибридную метку, называемую ADP-ribosyl-ubiquitylation. Лигаза убиквитина RNF114 распознаёт этот составной сигнал и притягивается к участкам повреждений ДНК, где она может модифицировать или перемещать другие белки. Используя специализированный «ридер» (ZUD) вместе со своими антителами, авторы показывают, что дефицит XRCC1 увеличивает не только моно-АДФ-рибозу, но и эту гибридную метку, а также привлечение RNF114 к разрывам. Это наводит на мысль, что нарушенная моно-сигнализация и её взаимодействие с убиквитинированием могут способствовать клеточному стрессу и фенотипам болезни, наблюдаемым при мутациях XRCC1.
Что это значит для понимания и лечения болезней
Для неспециалиста главный вывод таков: то, что раньше воспринималось как один сигнал ремонта ДНК, на самом деле представляет собой две перекрывающиеся волны небольших химических меток, каждая со своим временем появления и последствиями. Создав высокоспецифичные молекулярные инструменты, это исследование разъединяет эти волны и показывает, что потеря XRCC1 усиливает не только известный всплеск длинных цепочек, но и продолжительный подъём одиночных звеньев и связанных с ними убиквитин-маркеров. Эти открытия уточняют наше представление о работе PARP1, помогают объяснить, почему дефекты XRCC1 и родственных ферментов приводят к заболеваниям мозга, и предоставляют набор инструментов, который другие исследователи могут использовать для изучения АДФ-рибозилирования в раке, иммунитете и за их пределами — что потенциально приведёт к более точному использованию препаратов, нацеленных на PARP.
Цитирование: Dauben, H., Mihaljević, M., Kolvenbach, A. et al. Versatile and sensitive detection of mono- and poly(ADP-ribosyl)ation reveals XRCC1-dependent remodelling of PARP1 signalling. Nat Commun 17, 3216 (2026). https://doi.org/10.1038/s41467-026-71311-4
Ключевые слова: АДФ-рибозилирование, репарация повреждений ДНК, сигнализация PARP1, дефицит XRCC1, убиквитинирование