Clear Sky Science · ar
كشف متعدد الاستخدام وحساس لحمض ADP-ريبوز أحادي ومتعدّد يكشف إعادة تشكيل إشارات PARP1 المعتمدة على XRCC1
لماذا تهم العلامات الكيميائية الصغيرة على نظام إصلاح الحمض النووي لدينا
تقوم كل خلية في جسمنا باستمرار بإصلاح الضرر الذي يلحق بالحمض النووي. إذا فشل هذا الإصلاح، فقد يؤدي ذلك إلى السرطان أو التنكس العصبي أو موت الخلايا. لاعب رئيسي في شبكة الإصلاح هذه هو بروتين يدعى PARP1، الذي يزين نفسه والبروتينات المجاورة بعلامات صغيرة شبيهة بالسكَّر مصنوعة من NAD+. تأتي هذه العلامات بأشكال قصيرة وطويلة وتعمل كإشارات تستدعي عوامل إصلاح أخرى. حتى الآن، افتقر العلماء إلى أدوات دقيقة لرؤية وتمييز هذه الأنواع المختلفة من العلامات داخل الخلايا، لا سيما في سياق المرض. تبني هذه الدراسة مثل هذه الأدوات وتستخدمها للكشف عن تغيير غير متوقع في إشارات إصلاح الحمض النووي عند غياب بروتين إصلاح آخر، XRCC1.
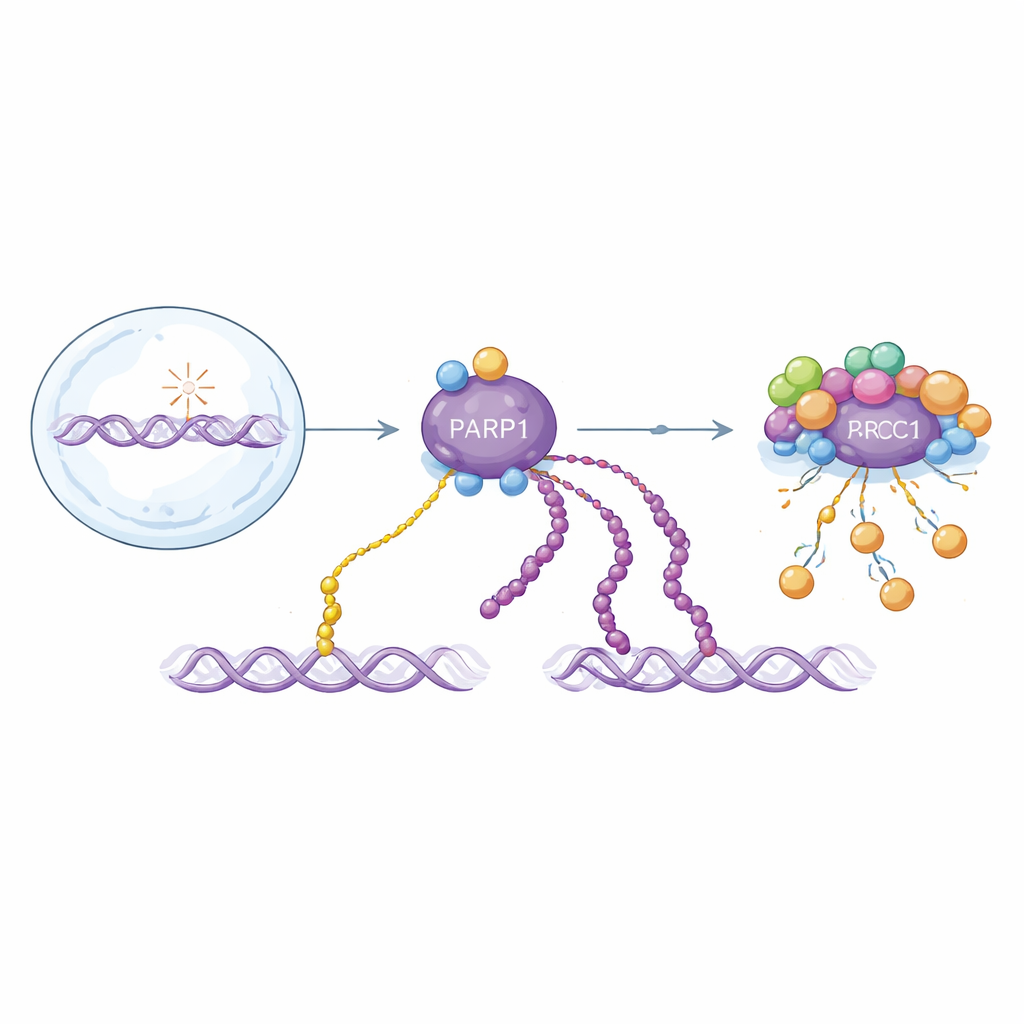
نكهتان لإشارة إصلاح حاسمة للحمض النووي
يستجيب PARP1 لكسور سلاسل الحمض النووي عن طريق ربط وحدات ADP-ريبوز بنفسه وببروتينات أخرى. توجد هذه التعديلات كوحدات مفردة (ADP-ريبوزيلاسيون أحادي) أو كسلاسل طويلة (ADP-ريبوزيلاسيون متعدد). كلا الشكلين يساعدان في تنظيم الإصلاح، لكنهما يتصرفان بشكل مختلف مع الزمن: تظهر السلاسل الطويلة في اندفاع أولي سريع وتُزال بسرعة، بينما تتراكم الوحدات المفردة ببطء أكثر وتستمر لفترة أطول. وبما أن كلا الشكلين مبنيان من نفس الوحدة البنائية، فإن معظم طرق الكشف الحالية تدمج بينهما. هذا يجعل من الصعب فهم مساهمة كلٍ منهما في الصحة والمرض، أو كيفية عمل الأدوية المستهدفة لـ PARP1 على نحو فعلي.
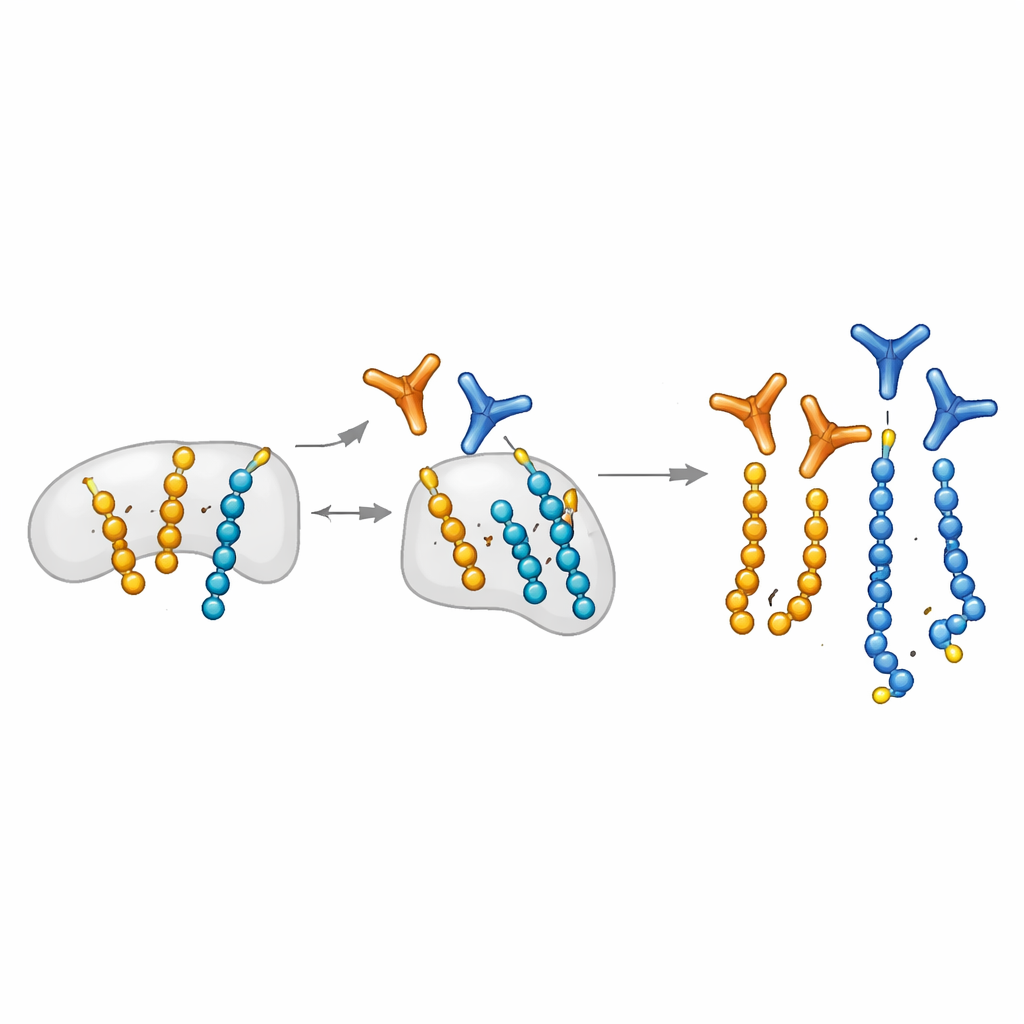
هندسة "عيون" جزيئية انتقائية للغاية
يسّع المؤلفون منصة في الكيمياء الحيوية يمكنها وضع ADP-ريبوز برمجيًا على بقايا سيرين محددة في ببتيدات قصيرة. يستخدمون هذه الببتيدات المصممة كطعم لصيد أجزاء أجسام مضادة من مكتبات عرض كبيرة. والأهم أنهم يدخلون خطوة "حجب أحادي": تُستخدم الببتيدات المعدلة أحاديًا لامتصاص الأجسام المضادة التي تتعرف على الوحدات المفردة، متركين وراءهم المرشحين الذين يفضلون السلاسل الطويلة. تنتج هذه الاستراتيجية أجسامًا مضادة معيارية يمكن، بمجرد تجميعها باستخدام نظام SpyTag/SpyCatcher، تحويلها بسرعة إلى صيغ مختلفة للبلوتات والمجهرية وعمليات السحب. كما يكتشف الفريق نمطًا مميزًا لأيونات شظايا في مطيافية الكتلة يميّز تحديدًا الببتيدات الحاملة لوحدتين من ADP-ريبوز، مما يساعد على تحديد مواقع التعديلات المتعددة على البروتينات بدقة.
رؤية إشارات دقيقة حيث لا يرى الآخرون شيئًا
بأدواتهم الجديدة، يظهر الباحثون أن الأجسام المضادة المتخصصة في المتعدد تكشف سلاسل قصيرة جدًا، وسلاسل طويلة، وحتى بوليمرات ADP-ريبوز الحرة، وتفعل ذلك بحساسية أعلى بكثير من الكواشف التجارية الموجودة. تعمل الأجسام المضادة عبر ارتباطات مختلف الأحماض الأمينية، وليس السيرين فقط، ويمكنها تصور ADP-ريبوز متعدد في الخلايا في ظروف لم ترَ فيها الأدوات السابقة أي إشارة، مثل الخلايا غير المضطربة أو الخلايا التي تنمو في انخفاض الأكسجين. في الوقت نفسه، يقوم الفريق بتحسين ألفة الأجسام المضادة الأحادية والمتخصصة في الموقع لتعزيز حساسيتها مع الحفاظ على انتقائيتها. معًا، تسمح هذه المجموعة بصريًا برصد الإشارتين الأحادية والمتعددة في نفس الخلية، كاشفة أن التعديلات المتعددة تظهر في بؤر نووية موضعية بينما تشكل التعديلات الأحادية موجة أكثر انتشارًا وتستمر لفترة أطول عبر الكروماتين.
كيف يعيد فقدان XRCC1 تشكيل موجات إصلاح الحمض النووي
يعمل XRCC1 عادةً كهيكل داعم يساعد PARP1 على الارتباط ثم الانفصال عن وسائط إصلاح الحمض النووي. عندما يُفقد XRCC1، يصبح PARP1 مفرط النشاط ومن المعروف أنه يفرط في إنتاج سلاسل ADP-ريبوز الطويلة، وهي حالة مرتبطة بالتنكس العصبي. باستخدام مجموعة الأجسام المضادة المحسنة لديهم، يُظهر المؤلفون أن فقدان XRCC1 يفعل أكثر من مجرد زيادة السلاسل الطويلة: فهو يعزز بشكل كبير أيضًا موجة ADP-ريبوزيلاسيون الأحادي. أثناء استمرار تلف الحمض النووي من عوامل مختلفة، تظهر الخلايا التي تفتقر إلى XRCC1 قممًا أعلى وأبكر لكل من التعديلات الطويلة والقصيرة، مع توقيت خاص بنوع الضرر. غالبًا ما تظل التعديلات الأحادية أكثر استقرارًا وموزعة بشكل أكثر تجانسًا من الإشارة المتعددة التي تتقلب بسرعة. وتحدد الدراسة أيضًا الهستون H1 كهدف أحادي ملحوظ قد تحافظ وضعه المستمر على ارتخاء الكروماتين حول الآفات.
من إشارات متغيرة إلى حركة بروتينات متغيرة
يمكن أن يُزين ADP-ريبوز الأحادي على السيرين نفسه بارتباط كيميائي غير عادي إلى اليوبكويتين، مكونًا علامة هجينة تُسمى ADP-ريبوزيلاسيون-يوبيكويتيليشن. يتعرف ليغاز اليوبكويتين RNF114 على هذه الإشارة المركبة وينجذب إلى مواقع تلف الحمض النووي حيث قد يعدّل أو ينقل بروتينات أخرى. باستخدام بروتين قارئ متخصص (ZUD) إلى جانب أجسامهم المضادة، يُظهر المؤلفون أن نقص XRCC1 يزيد ليس فقط ADP-ريبوز الأحادي، بل يزيد أيضًا هذه العلامة الهجينة وتجند RNF114 إلى الكسور. يقترح هذا أن الاختلال في إشارات الأحادي وتداخلها مع نظام اليوبكويتين قد يساهم في الإجهاد الخلوي والظواهر المرضية التي تُرى عندما يتحور XRCC1.
ما يعنيه هذا لفهم المرض ومعالجته
بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن ما بدا في السابق كإشارة إصلاح واحدة للحمض النووي هو في الواقع موجتان متداخلتان من علامات كيميائية صغيرة، لكل منهما توقيته ونتائجه الخاصة. من خلال بناء أدوات جزيئية انتقائية للغاية، تفصل هذه الدراسة تلك الموجات وتظهر أن فقدان XRCC1 يَكثّف ليس فقط الطفرة المعروفة من السلاسل الطويلة ولكن أيضًا اندفاعًا مستمرًا للوحدات المفردة وعلامات اليوبكويتين المرتبطة بها. تصقل هذه الرؤى فهمنا لكيفية عمل PARP1، وتساعد في تفسير سبب تسبب عيوب XRCC1 والإنزيمات المرتبطة بها في أمراض الدماغ، وتوفر صندوق أدوات يمكن للباحثين الآخرين استخدامه لتفكيك ADP-ريبوزيلاسيون في السرطان والمناعة وما وراءهما — مما قد يؤدي إلى استخدام أكثر دقة للأدوية المستهدفة لـ PARP.
الاستشهاد: Dauben, H., Mihaljević, M., Kolvenbach, A. et al. Versatile and sensitive detection of mono- and poly(ADP-ribosyl)ation reveals XRCC1-dependent remodelling of PARP1 signalling. Nat Commun 17, 3216 (2026). https://doi.org/10.1038/s41467-026-71311-4
الكلمات المفتاحية: ADP-ريبوزيلاسيون, إصلاح تلف الحمض النووي, إشارات PARP1, نقص XRCC1, يوبيكويتيليشن