Clear Sky Science · fr
Détection polyvalente et sensible de la mono- et poly(ADP-ribosyl)ation révèle un remodelage dépendant de XRCC1 du signalement PARP1
Pourquoi de petites étiquettes chimiques sur notre système de réparation de l’ADN comptent
Chaque cellule de notre corps répare en permanence les dommages causés à son ADN. Si cette réparation échoue, les conséquences peuvent être le cancer, la neurodégénérescence ou la mort cellulaire. Un acteur clé de ce réseau de réparation est une protéine appelée PARP1, qui se marque elle-même et marque des protéines voisines avec de petites étiquettes ressemblant à des sucres issues du NAD+. Ces étiquettes existent en formes courtes et longues et agissent comme des signaux attirant d’autres facteurs de réparation. Jusqu’à présent, les scientifiques manquaient d’outils précis pour voir et distinguer ces différents types d’étiquettes à l’intérieur des cellules, en particulier en contexte pathologique. Cette étude construit de tels outils et les utilise pour révéler un changement inattendu dans la signalisation de la réparation de l’ADN lorsque une autre protéine de réparation, XRCC1, est absente.
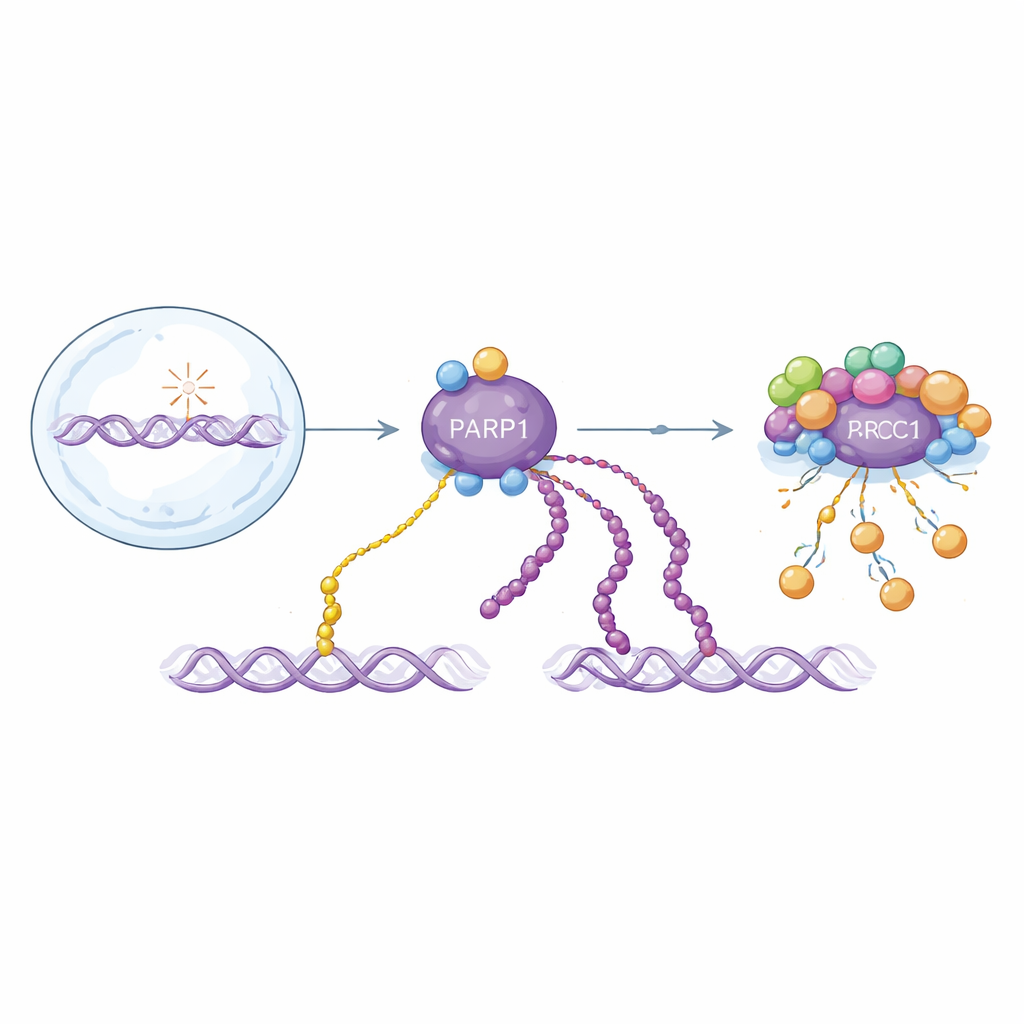
Deux variantes d’un signal critique de réparation de l’ADN
PARP1 répond aux cassures de brin d’ADN en ajoutant des unités d’ADP-ribose sur elle-même et d’autres protéines. Ces modifications existent comme des unités simples (mono-ADP-ribosylation) ou comme de longues chaînes (poly-ADP-ribosylation). Les deux formes aident à organiser la réparation, mais elles se comportent différemment dans le temps : les longues chaînes apparaissent dans une rafale initiale rapide et sont rapidement ôtées, tandis que les unités simples s’accumulent plus lentement et persistent plus longtemps. Parce que les deux formes sont construites à partir du même bloc de base, la plupart des méthodes de détection existantes les confondent. Cela complique la compréhension de la contribution de chacune à la santé et à la maladie, ou de la manière dont les médicaments ciblant PARP1 agissent réellement.
Concevoir des « yeux » moléculaires hautement sélectifs
Les auteurs étendent une plateforme de biologie chimique qui peut placer de façon programmée de l’ADP-ribose sur des résidus sérine spécifiques de courts peptides. Ils utilisent ces peptides sur mesure comme appât pour isoler des fragments d’anticorps à partir de grandes bibliothèques d’affichage. Crucialement, ils introduisent une étape de « blocage mono » : des peptides mono-modifiés sont utilisés pour absorber les anticorps qui reconnaissent les unités simples, laissant des candidats préférant les longues chaînes. Cette stratégie produit des anticorps modulaires qui, une fois assemblés à l’aide d’un système SpyTag/SpyCatcher, peuvent être rapidement convertis en différents formats pour western blot, microscopie et pull-downs. L’équipe découvre également un motif distinctif d’ions fragments en spectrométrie de masse qui marque spécifiquement les peptides portant deux unités d’ADP-ribose, aidant à cartographier correctement où les poly-modifications se produisent sur les protéines.
Voir des signaux subtils là où d’autres ne voient rien
Avec leurs nouveaux outils, les chercheurs montrent que les anticorps poly-spécifiques détectent des chaînes très courtes, des chaînes longues et même des polymères d’ADP-ribose libres, et ce avec une sensibilité bien supérieure aux réactifs commerciaux existants. Les anticorps fonctionnent à travers différents types de liaisons d’acides aminés, pas seulement la sérine, et peuvent visualiser le poly-ADP-ribose dans des cellules dans des conditions où les outils précédents ne détectaient aucun signal, comme dans des cellules non stressées ou en faible oxygénation. Parallèlement, l’équipe améliore par maturation d’affinité des anticorps mono-spécifiques et site-spécifiques antérieurs pour augmenter leur sensibilité tout en conservant leur sélectivité. Ensemble, cette boîte à outils permet l’imagerie simultanée des signaux mono et poly dans la même cellule, révélant que la poly-modification apparaît en foyers nucléaires localisés tandis que la mono-modification forme une onde plus diffuse et plus durable à travers la chromatine.
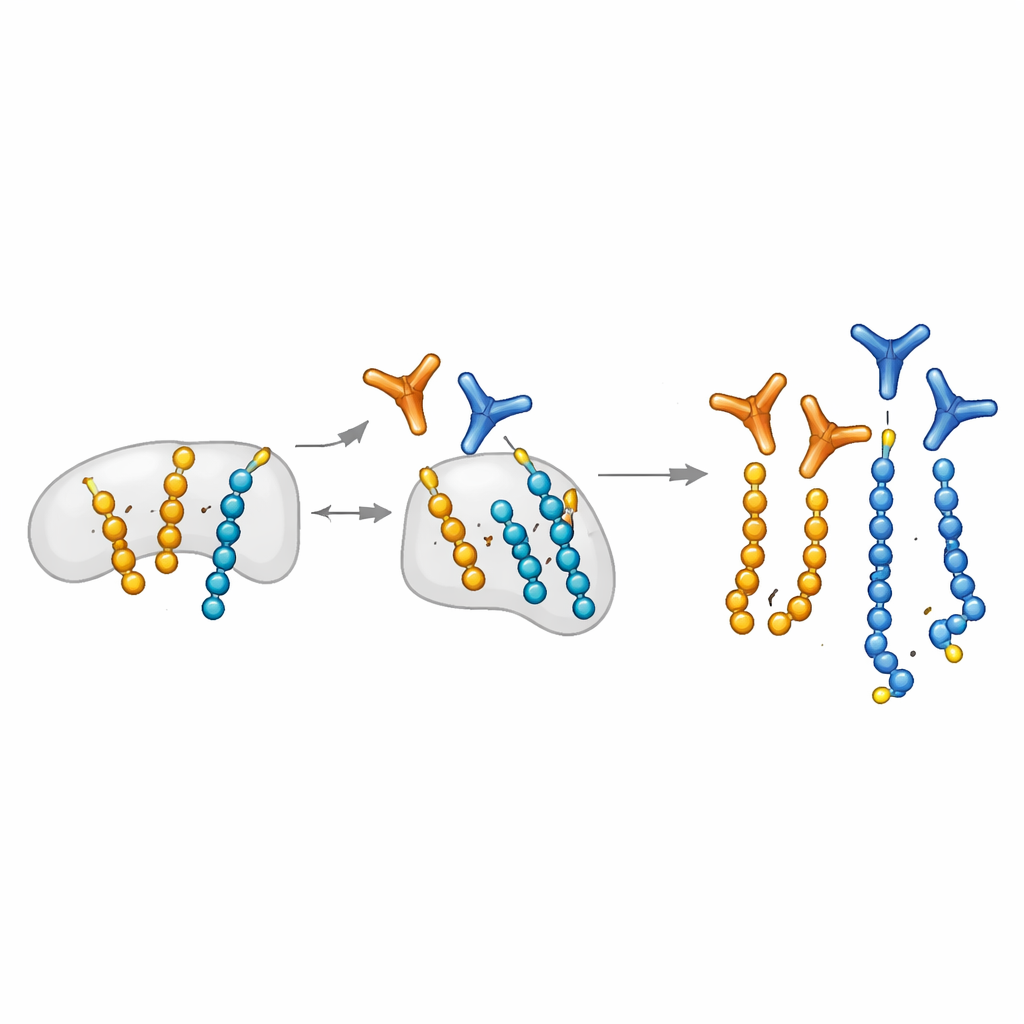
Comment la perte de XRCC1 reconfigure les vagues de réparation de l’ADN
XRCC1 agit normalement comme un échafaudage qui aide PARP1 à s’engager puis à se désengager des intermédiaires de réparation de l’ADN. Lorsque XRCC1 est perdu, PARP1 devient hyperactif et il est connu pour surproduire de longues chaînes d’ADP-ribose, un état associé à la neurodégénérescence. En utilisant leur panel d’anticorps affinés, les auteurs montrent que la perte de XRCC1 ne se contente pas d’augmenter les longues chaînes : elle amplifie de façon spectaculaire la vague de mono-ADP-ribosylation également. Lors de dommages ADN persistants induits par différents agents, les cellules dépourvues de XRCC1 présentent des pics plus élevés et plus précoces des deux modifications, longues et courtes, avec un calendrier dépendant du type de dommage. La mono-modification reste souvent plus stable et plus uniformément distribuée que le signal poly, qui fluctue rapidement. Le travail identifie aussi l’histone H1 comme une cible mono-modifiée proéminente dont l’étiquetage persistant pourrait maintenir la chromatine plus relâchée autour des lésions.
Des signaux altérés au trafic protéique modifié
La mono-ADP-ribose sur sérine peut elle-même être décorée par une liaison chimique singulière à l’ubiquitine, formant une marque hybride appelée ADP-ribosyl-ubiquitylation. La ligase d’ubiquitine RNF114 reconnaît ce signal composite et est attirée vers les sites de dommage ADN où elle peut modifier ou déplacer d’autres protéines. En utilisant une protéine lectrice spécialisée (ZUD) aux côtés de leurs anticorps, les auteurs montrent que la déficience en XRCC1 augmente non seulement la mono-ADP-ribose, mais aussi cette marque hybride et le recrutement de RNF114 aux cassures. Cela suggère que la dérégulation du signal mono et son interconnexion avec l’ubiquitine peuvent contribuer au stress cellulaire et aux phénotypes pathologiques observés lorsque XRCC1 est muté.
Ce que cela implique pour la compréhension et le traitement des maladies
Pour un non-spécialiste, le message clé est que ce qui semblait être un seul signal de réparation de l’ADN est en réalité deux vagues qui se chevauchent d’étiquettes chimiques, chacune avec son propre timing et ses conséquences. En construisant des outils moléculaires hautement sélectifs, cette étude sépare ces vagues et montre que la perte de XRCC1 intensifie non seulement l’explosion bien connue de longues chaînes mais aussi une poussée soutenue d’unités simples et de leurs marques d’ubiquitine associées. Ces conclusions affinent notre compréhension du fonctionnement de PARP1, contribuent à expliquer pourquoi des défauts de XRCC1 et d’enzymes apparentées provoquent des maladies cérébrales, et fournissent une boîte à outils que d’autres chercheurs peuvent utiliser pour disséquer l’ADP-ribosylation en cancérologie, immunologie et au-delà — ouvrant potentiellement la voie à une utilisation plus précise des médicaments ciblant PARP.
Citation: Dauben, H., Mihaljević, M., Kolvenbach, A. et al. Versatile and sensitive detection of mono- and poly(ADP-ribosyl)ation reveals XRCC1-dependent remodelling of PARP1 signalling. Nat Commun 17, 3216 (2026). https://doi.org/10.1038/s41467-026-71311-4
Mots-clés: ADP-ribosylation, Réparation de l'ADN, Signalisation PARP1, Déficit en XRCC1, Ubiquitylation