Clear Sky Science · he
גילוי רב-תכליתי ורגיש של מונו- ופורמל-(ADP-ריבוזילציה) חושף עיצוב מחדש של איתות PARP1 התלוי ב-XRCC1
מדוע תגיות כימיות זעירות במערכת תיקון ה‑DNA שלנו חשובות
כל תא בגופנו מתקן ברציפות נזקים ל‑DNA שלו. כשמערכת התיקון הזו משתבשת, התוצאה עלולה להיות סרטן, ניוון עצבי או מוות תאי. שחקן מרכזי ברשת התיקון הזו הוא החלבון PARP1, שמקשט את עצמו ואת חלבונים סמוכים בתגיות קטנות הדומות לסוכר המיוצרות מ‑NAD+. תגיות אלה מופיעות בצורות קצרות וארוכות ומשמשות אותות שמזמינים גורמי תיקון נוספים. עד היום חסרו למדענים כלים מדויקים לראות ולהבחין בין סוגי התגיות האלה בתוך תאים, במיוחד בהקשר מחלות. העבודה הזו מפתחת כלים כאלה ומשתמשת בהם כדי לחשוף שינוי בלתי צפוי באיתות תיקון ה‑DNA כאשר חלבון תיקון אחר, XRCC1, חסר.
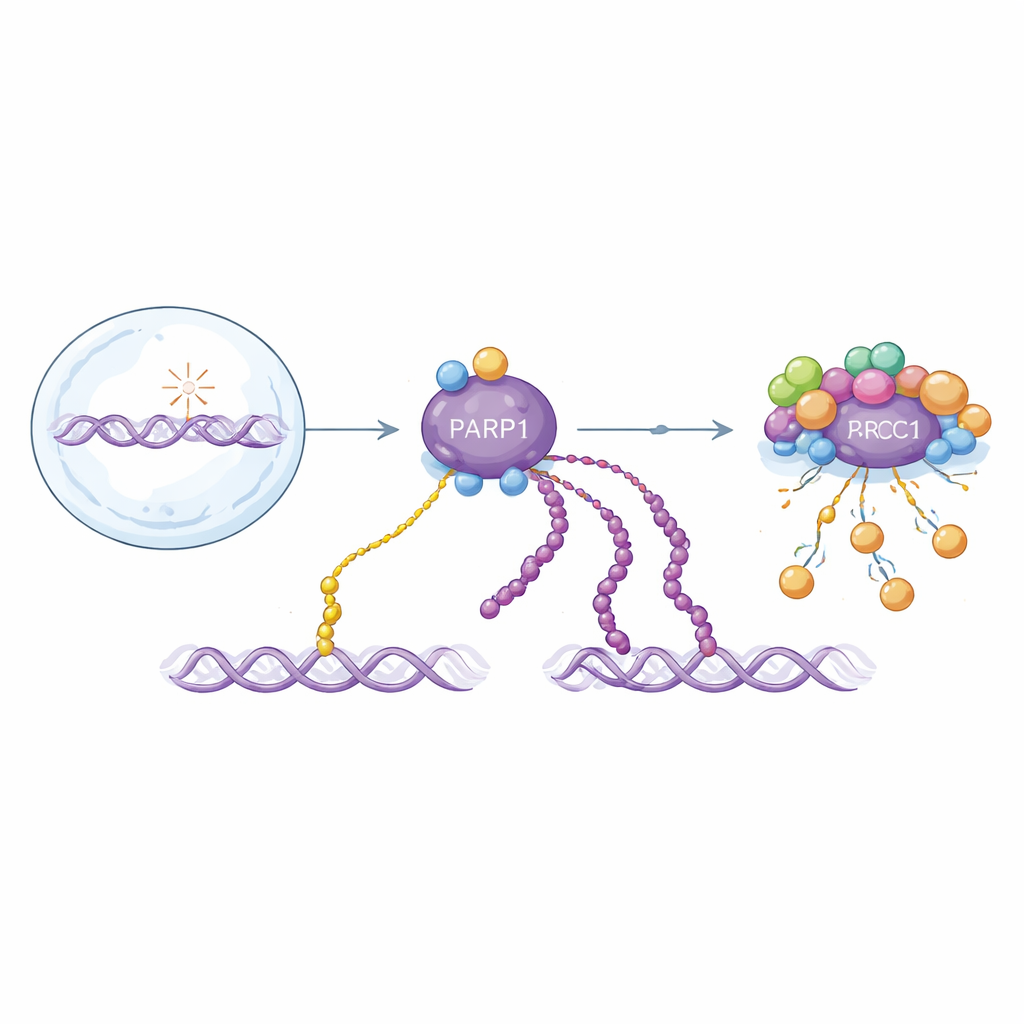
שתי וריאציות של אות קריטי בתיקון DNA
PARP1 מגיב לשברים בגדיל ה‑DNA על ידי חיבור יחידות ADP‑ריבוז לעצמו ולחלבונים אחרים. המודיפיקציות הללו קיימות כיחידות בודדות (מונו‑ADP‑ריבוזילציה) או כשרשראות ארוכות (פוליאדפ‑ריבוזילציה). שתי הצורות מסייעות בארגון התיקון, אך מתנהגות בצורה שונה לאורך זמן: שרשראות ארוכות נוצרות בבועה מהירה בתחילת התגובה ומוסרות במהירות, בעוד יחידות בודדות נצטברות לאט יותר ונשארות לאורך זמן. מאחר ששתי הצורות בנויות מאותו בלוק בסיסי, רוב שיטות הגילוי הקיימות מטשטשות ביניהן. זה מקשה להבין כיצד כל אחת תורמת לבריאות ולמחלה, או כיצד תרופות המכוונות ל‑PARP1 פועלות בפועל.
מהנדסים "עיניים" מולקולריות סלקטיביות במיוחד
המחברים מרחיבים פלטפורמה בכימיה ביולוגית שיכולה לתכנת הצבה של ADP‑ריבוז על שאריות סרין ספציפיות בפפטידים קצרים. הם משתמשים בפפטידים מותאמים אלה כטרף לדיגום פרגמנטים של נוגדנים מספריות תצוגה גדולות. מהותי לגישה הוא צעד של "חסימת מונו": פפטידים במודיפיקציה מונו משמשים כדי לספוח נוגדנים שמזהים יחידות בודדות, ומשאירים מועמדים שמעדיפים שרשראות ארוכות. אסטרטגיה זו מניבה נוגדנים מודולריים שניתן, לאחר הרכבה באמצעות מערכת SpyTag/SpyCatcher, להמיר במהירות לפורמטים שונים לבלאטים, מיקרוסקופיה ומשכי‑חלבון. הצוות גם מגלה דפוס ייחודי של יוני קטעים בספקטרומטריית המסה שמסמן במיוחד פפטידים הנושאים שתי יחידות ADP‑ריבוז, ותורם למיפוי נכון של מקומות הפולימודיפיקציה בחלבונים.
לראות אותות עדינים במקום שאחרים לא ראו כלום
עם הכלים החדשים שלהם, החוקרים מראים שנוגדני הרב‑ספציפיות מזהים שרשראות מאוד קצרות, שרשראות ארוכות ואפילו פולימרים חופשיים של ADP‑ריבוז, והם עושים זאת ברגישות גבוהה בהרבה מאשר תגובות מסחריות קיימות. הנוגדנים פועלים על פני קישורים של חומצות אמינו שונות, לא רק סרין, ויכולים להמחיש פוליאדפ‑ריבוז בתאים בתנאים שבהם כלים קודמים לא ראו אות כלל, כגון בתאים שאינם תחת לחץ או בתאים שגדלים בחמצן נמוך. במקביל, הצוות מבצע שיפור זיקה (affinity‑maturation) לנוגדנים מונו‑ספציפיים וקבועי‑אתר שהיו קיימים קודם כדי להגביר את הרגישות שלהם תוך שמירה על סלקטיביות. יחד, ארגז הכלים הזה מאפשר הדמיה סימולטנית של אותות מונו ופוליאדפ באותו תא, וחושף כי הפולימודיפיקציה מופיעה בכתמים גרעיניים מקומיים בעוד שמונו‑המודיפיקציה יוצרת גל מפוזר ויציב יותר ברחבי הכרומטין.
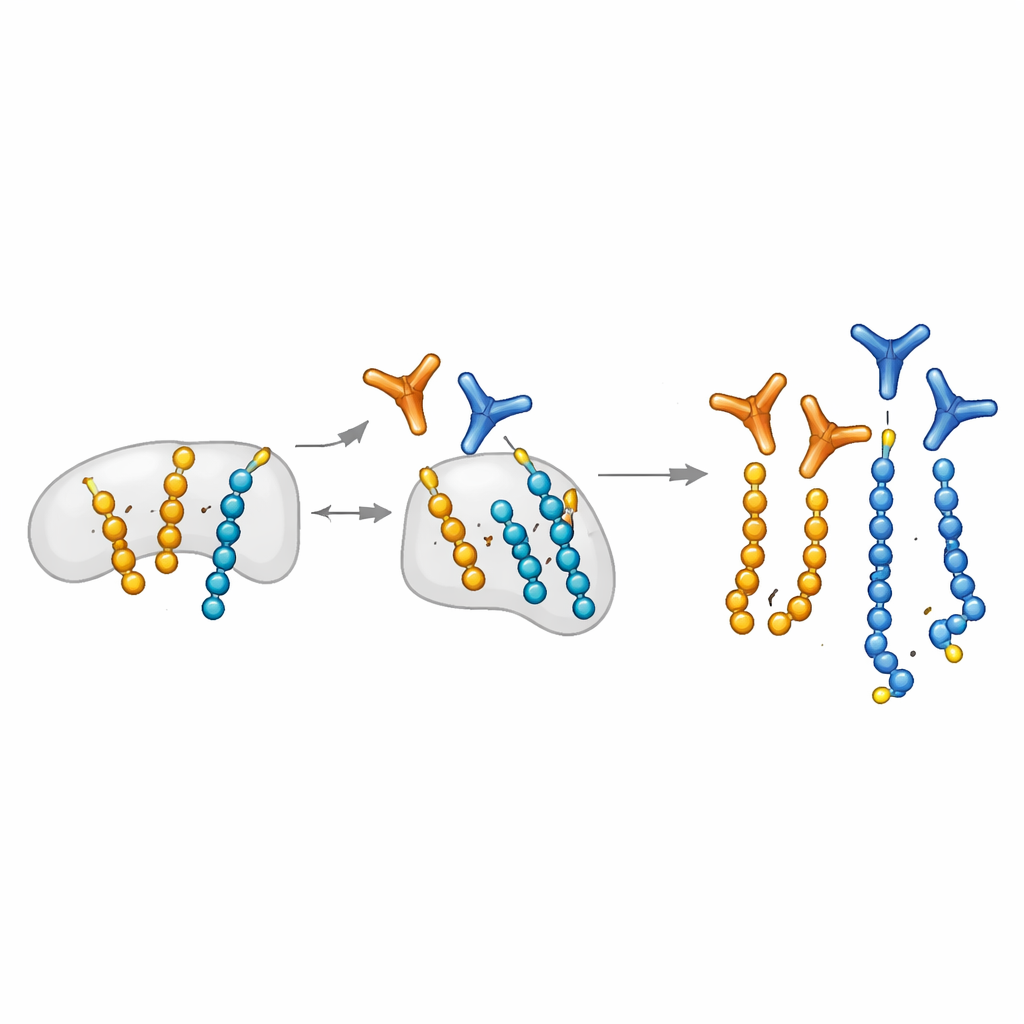
כיצד אובדן XRCC1 משנה את גלי תיקון ה‑DNA
XRCC1 בדרך כלל פועל כשלד המסייע ל‑PARP1 להיכנס ולהתקשר, ואז להשתחרר, מאמצעים בתיקון ה‑DNA. כאשר XRCC1 חסר, PARP1 הופך להיפראקטיבי וידוע שהוא מייצר בקצב יתר שרשראות ADP‑ריבוז ארוכות, מצב שקשור לנוירודגנרציה. בעזרת מערך הנוגדנים המדויק שלהם, המחברים מראים שאובדן XRCC1 עושה יותר מהגברה של השרשראות הארוכות: הוא מגדיל בצורה דרמטית גם את גל המונו‑ADP‑ריבוזילציה. במהלך נזקי DNA מתמשכים שנגרמים על‑ידי סוכנים שונים, תאים החסרים XRCC1 מראים שיאים גבוהים ומוקדמים יותר של שני סוגי המודיפיקציות, עם תזמון התלוי בסוג הנזק. המונו‑מודיפיקציה נשמרת לעתים קרובות יציבה ומפוזרת יותר מאשר האות הפולימרי המתנודד במהירות. העבודה מזהה גם את היסטון H1 כיעד מונו‑מודיפיקציה בולט, שתיוגו המתמשך עשוי לשמור על הכרומטין מרוחק יותר סביב הפגיעות.
מאותות משונים לתנועת חלבונים משונה
מונו‑ADP‑ריבוז על סרין יכול בעצמו להיות מקושט בקשר כימי יוצא דופן לאוביקוויטין, ליצירת סימן היברידי שנקרא ADP‑ריבוזיל‑אוביקוויטינציה. ליגז ה‑ubiquitin RNF114 מזהה את האות המורכב הזה ונמשכת לאתרי נזק ב‑DNA, שם היא עשויה למודיפיקציה או להזיז חלבונים אחרים. באמצעות קורא מיוחד (ZUD) לצד הנוגדנים שלהם, המחברים מראים כי חוסר XRCC1 מעלה לא רק את המונו‑ADP‑ריבוז אלא גם את הסימן ההיברידי הזה ואת גיוס RNF114 לשברים. ממצא זה מרמז כי ויסות לקוי של אותות המונו וצמחוניות האוביקוויטין שלהם עשויים לתרום ללחץ התאי ולפנוטיפים מחלתיים הנצפים כאשר XRCC1 מוטנטי.
מה משמעות הדבר להבנת ומטופלת מחלות
ללא מומחיות עמוקה, המסר המרכזי הוא שמה שנראה בעבר כאות תיקון DNA יחיד הוא למעשה שני גלי־חוצפה חופפים של תגיות כימיות קטנות, לכל אחד זמן וסדר תוצאות משלו. על‑ידי בניית כלים מולקולריים ברירותיים מאוד, עבודה זו מבדילה בין הגלים ומראה שאיבוד XRCC1 מחריף לא רק את ההתפרצות המוכרת של שרשראות ארוכות אלא גם גל ממושך של תגיות יחידיות ושל סימני האוביקוויטין הקשורים אליהן. התובנות הללו מדייקות את ההבנה שלנו לגבי אופן פעולתו של PARP1, מסייעות להבהיר מדוע פגמים ב‑XRCC1 ובאנזימים קשורים גורמים למחלות מוח, ומספקות ארגז כלים שחוקרים אחרים יכולים להשתמש בו לפיענוח ADP‑ריבוזילציה בסרטן, בחיסון ובהקשרים נוספים — דבר שעשוי להוביל לשימוש מדויק יותר בתרופות המכוונות ל‑PARP.
ציטוט: Dauben, H., Mihaljević, M., Kolvenbach, A. et al. Versatile and sensitive detection of mono- and poly(ADP-ribosyl)ation reveals XRCC1-dependent remodelling of PARP1 signalling. Nat Commun 17, 3216 (2026). https://doi.org/10.1038/s41467-026-71311-4
מילות מפתח: ADP-ריבוזילציה, תיקון נזקי DNA, איתות PARP1, חסר XRCC1, אוביקוויטינציה