Clear Sky Science · pl
Wszechstronna i czuła detekcja mono- i poli(ADP-rybozylacji) ujawnia remodelowanie sygnalizacji PARP1 zależne od XRCC1
Dlaczego małe chemiczne znaczniki w naszym systemie naprawy DNA mają znaczenie
Każda komórka w naszym ciele nieustannie naprawia uszkodzenia DNA. Jeśli ten proces idzie źle, może to prowadzić do nowotworów, neurodegeneracji lub śmierci komórki. Kluczowym uczestnikiem tej sieci naprawczej jest białko PARP1, które ozdabia siebie i pobliskie białka małymi, cukropodobnymi znacznikami pochodzącymi z NAD+. Znaczniki te występują w krótkich i długich formach i działają jak sygnały przywołujące inne czynniki naprawcze. Do tej pory naukowcom brakowało precyzyjnych narzędzi do obserwacji i rozróżniania tych różnych typów znaczników w komórkach, zwłaszcza w warunkach chorobowych. W tej pracy zbudowano takie narzędzia i użyto ich do ujawnienia nieoczekiwanej zmiany w sygnalizacji naprawy DNA, gdy brak jest innego białka naprawczego, XRCC1.
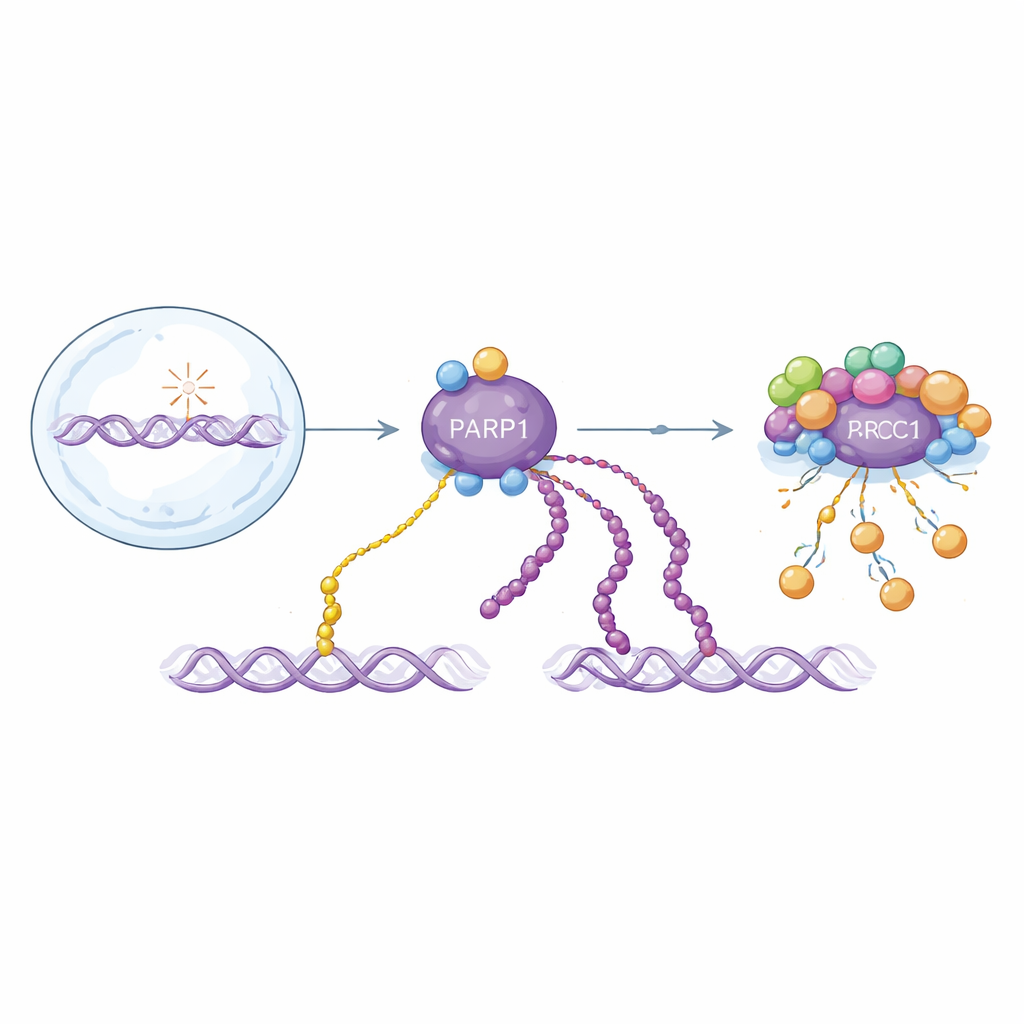
Dwie odmiany kluczowego sygnału naprawy DNA
PARP1 reaguje na złamania nici DNA przez przyłączanie jednostek ADP-rybozy do siebie i innych białek. Modyfikacje te występują jako pojedyncze jednostki (mono-ADP-rybozylacja) lub jako długie łańcuchy (poli-ADP-rybozylacja). Obie formy pomagają zorganizować naprawę, ale zachowują się odmiennie w czasie: długie łańcuchy pojawiają się w szybkim początkowym wybuchu i są szybko usuwane, podczas gdy pojedyncze jednostki kumulują się wolniej i utrzymują dłużej. Ponieważ obie formy budowane są z tego samego elementu, większość istniejących metod detekcji zlewa je w jedną całość. Utrudnia to zrozumienie, jak każda z nich przyczynia się do zdrowia i choroby oraz jak działają leki celujące w PARP1.
Inżynieria wysoce selektywnych „oczu” molekularnych
Autorzy rozbudowują platformę chemii biologicznej, która programowalnie umieszcza ADP-rybozę na określonych resztach serynowych krótkich peptydów. Używają tych niestandardowych peptydów jako przynęty do wyławiania fragmentów przeciwciał z dużych bibliotek display. Kluczowe jest wprowadzenie etapu „blokowania mono”: peptydy zmodyfikowane mono używane są do wyłapania przeciwciał rozpoznających pojedyncze jednostki, pozostawiając kandydatów preferujących długie łańcuchy. Ta strategia daje modułowe przeciwciała, które po zmontowaniu za pomocą systemu SpyTag/SpyCatcher można szybko konwertować na różne formaty do blotów, mikroskopii i pulldownów. Zespół odkrywa również charakterystyczny wzorzec jonów fragmentacyjnych w spektrometrii mas, który specyficznie oznacza peptydy niosące dwie jednostki ADP-rybozy, co pomaga poprawnie mapować miejsca poli-modyfikacji na białkach.
Widzenie subtelnych sygnałów tam, gdzie inni nie widzą nic
Dzięki nowym narzędziom badacze pokazują, że poli-specyficzne przeciwciała wykrywają bardzo krótkie łańcuchy, długie łańcuchy, a nawet wolne polimery ADP-rybozy, i robią to z znacznie większą czułością niż istniejące reagenty komercyjne. Przeciwciała działają w odniesieniu do różnych wiązań aminokwasowych, nie tylko seryny, i potrafią uwidocznić poli-ADP-rybozę w komórkach w warunkach, w których wcześniejsze narzędzia nie wykrywały sygnału, na przykład w komórkach bez stresu lub rosnących przy niskim stężeniu tlenu. Równolegle zespół dojrzewa afinicznie wcześniejsze mono-specyficzne i miejsce-specyficzne przeciwciała, by zwiększyć ich czułość przy zachowaniu selektywności. Razem ten zestaw narzędzi pozwala na jednoczesne obrazowanie zarówno mono-, jak i poli-sygnałów w tej samej komórce, ujawniając, że poli-modyfikacja pojawia się w lokalizowanych ogniskach w jądrze, podczas gdy mono-modyfikacja tworzy bardziej rozproszoną i dłużej utrzymującą się falę w chromatynie.
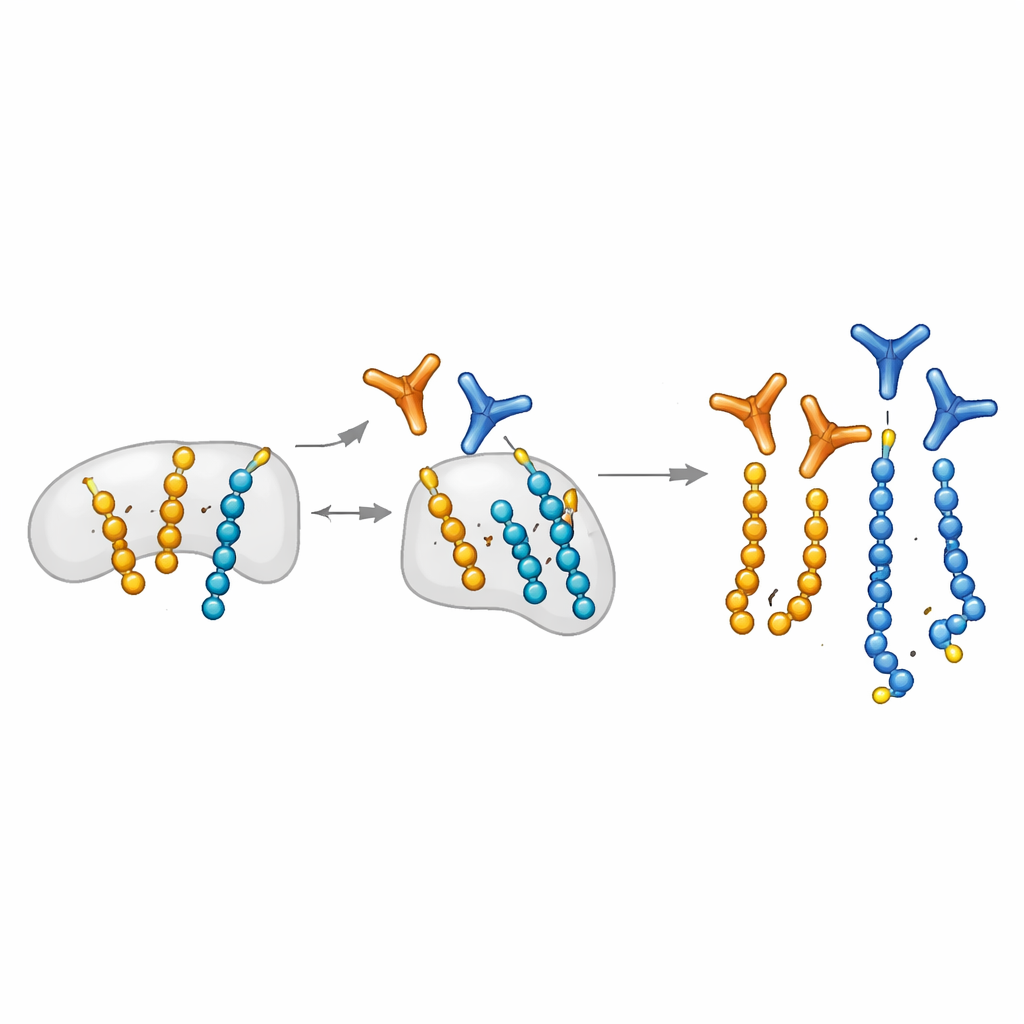
Jak utrata XRCC1 przekształca fale naprawy DNA
XRCC1 zwykle działa jako rusztowanie pomagające PARP1 angażować się i następnie wycofywać z pośredników naprawy DNA. Gdy XRCC1 zostaje utracony, PARP1 staje się hiperaktywny i wiadomo, że produkuje nadmiernie długie łańcuchy ADP-rybozy, stan powiązany z neurodegeneracją. Korzystając z zestawu udoskonalonych przeciwciał, autorzy pokazują, że utrata XRCC1 robi więcej niż tylko zwiększa długie łańcuchy: dramatycznie wzmacnia również falę mono-ADP-rybozylacji. Podczas trwających uszkodzeń DNA wywołanych różnymi czynnikami, komórki pozbawione XRCC1 wykazują wyższe i wcześniejsze szczyty obu modyfikacji, z czasowaniem zależnym od typu uszkodzenia. Mono-modyfikacja często pozostaje bardziej stabilna i jednorodnie rozłożona niż szybko fluktuujący sygnał poli. Praca identyfikuje też histon H1 jako wyraźny cel mono-modyfikacji, którego utrzymujące się oznakowanie może utrzymywać chromatynę bardziej rozluźnioną wokół uszkodzeń.
Z zmienionych sygnałów do zmienionego ruchu białek
Mono-ADP-ryboza na serynie może sama zostać dodatkowo ozdobiona nietypowym wiązaniem z ubikwityną, tworząc hybrydowy znak zwany ADP-rybozyl-ubikwitynacją. Ligaza ubikwitynowa RNF114 rozpoznaje ten złożony sygnał i jest ściągana do miejsc uszkodzeń DNA, gdzie może modyfikować lub przemieszczać inne białka. Używając wyspecjalizowanego białka-czytnika (ZUD) wraz z przeciwciałami, autorzy pokazują, że niedobór XRCC1 zwiększa nie tylko mono-ADP-rybozę, ale także ten hybrydowy znak i rekrutację RNF114 do złamań. To sugeruje, że zaburzona mono-sygnalizacja i jej krzyżowanie z ubikwitynacją mogą przyczyniać się do stresu komórkowego i fenotypów chorobowych obserwowanych przy mutacjach XRCC1.
Co to znaczy dla zrozumienia i leczenia chorób
Dla osoby niebędącej specjalistą kluczowy wniosek jest taki, że to, co wcześniej wyglądało jak pojedynczy sygnał naprawy DNA, to w rzeczywistości dwie nakładające się fale małych chemicznych znaczników, z odrębnym czasowaniem i konsekwencjami. Poprzez zbudowanie wysoce selektywnych narzędzi molekularnych, ta praca rozdziela te fale i pokazuje, że utrata XRCC1 nasila nie tylko dobrze znany wybuch długich łańcuchów, lecz także trwały napływ pojedynczych jednostek i ich powiązanych znaczników ubikwitynowych. Te spostrzeżenia doprecyzowują nasze rozumienie działania PARP1, pomagają wyjaśnić, dlaczego defekty XRCC1 i pokrewnych enzymów powodują choroby mózgu, oraz dostarczają zestawu narzędzi, którego inni badacze mogą użyć do rozpracowania ADP-rybozylacji w kontekście nowotworów, odporności i poza nimi — co może prowadzić do precyzyjniejszego stosowania leków celujących PARP.
Cytowanie: Dauben, H., Mihaljević, M., Kolvenbach, A. et al. Versatile and sensitive detection of mono- and poly(ADP-ribosyl)ation reveals XRCC1-dependent remodelling of PARP1 signalling. Nat Commun 17, 3216 (2026). https://doi.org/10.1038/s41467-026-71311-4
Słowa kluczowe: ADP-rybozylacja, naprawa uszkodzeń DNA, sygnalizacja PARP1, niedobór XRCC1, ubikwitynacja