Clear Sky Science · sv
Mångsidig och känslig detektion av mono- och poly(ADP-ribosylering) avslöjar XRCC1-beroende omformning av PARP1-signalering
Varför små kemiska märken på vårt DNA-reparationssystem spelar roll
Varje cell i vår kropp reparerar ständigt skador i sitt DNA. Om denna reparation går fel kan resultatet bli cancer, neurodegeneration eller celldöd. En nyckelspelare i detta reparationsnätverk är proteinet PARP1, som förser sig själv och närliggande proteiner med små sockerliknande märken byggda av NAD+. Dessa märken förekommer i korta och långa former och fungerar som signaler som rekryterar andra reparationsfaktorer. Hittills har forskare saknat precisa verktyg för att se och skilja dessa olika märkestyper inuti celler, särskilt i sjukdomssammanhang. Denna studie utvecklar sådana verktyg och använder dem för att avslöja en oväntad förändring i DNA-reparationssignalering när ett annat reparationsprotein, XRCC1, saknas.
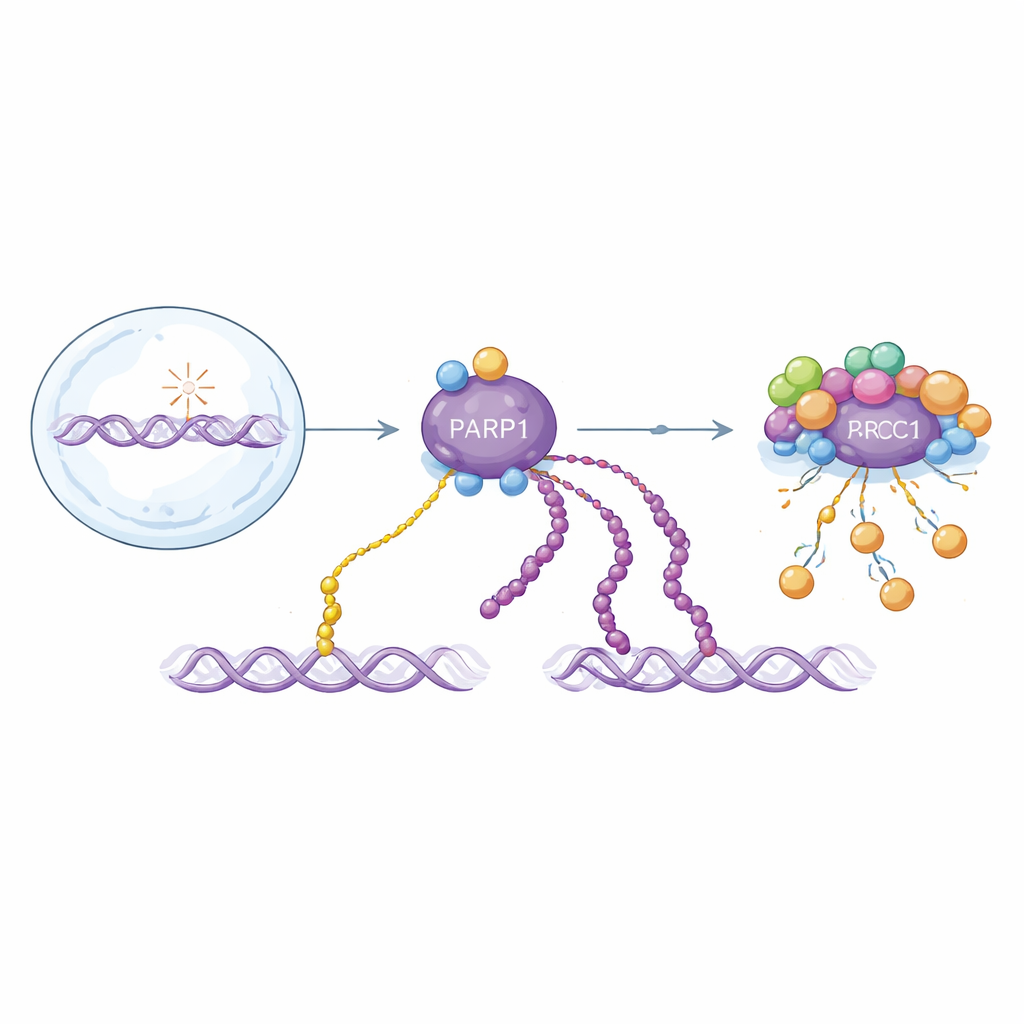
Två varianter av en kritisk DNA-reparationssignal
PARP1 svarar på DNA-strängbrott genom att fästa ADP-ribos-enheter på sig själv och andra proteiner. Dessa modifieringar finns som enskilda enheter (mono-ADP-ribosylering) eller som långa kedjor (poly-ADP-ribosylering). Båda formerna hjälper till att organisera reparationen, men beter sig olika över tid: långa kedjor uppträder i en snabb initial våg och tas snabbt bort, medan enskilda enheter ackumuleras långsammare och består längre. Eftersom båda formerna byggs från samma byggsten suddar de flesta befintliga detektionsmetoder ihop dem. Det försvårar att förstå hur varje form bidrar till hälsa och sjukdom, eller hur läkemedel som riktar sig mot PARP1 egentligen fungerar.
Konstruera högselektiva molekylära ”ögon”
Författarna utökar en kemisk-biologisk plattform som programmässigt kan placera ADP-ribos på specifika serinrester i korta peptider. De använder dessa skräddarsydda peptider som bete för att fiska upp antikroppsfragment från stora visningsbibliotek. Avgörande är att de inför ett ”mono-blockerande” steg: monomodifierade peptider används för att mätta antikroppar som känner igen enskilda enheter, vilket lämnar kvar kandidater som föredrar långa kedjor. Denna strategi ger modulära antikroppar som, när de sammanfogas med ett SpyTag/SpyCatcher-system, snabbt kan konverteras till olika format för blotting, mikroskopi och pull-downs. Teamet upptäcker också ett karaktäristiskt mönster av fragmentjoner i masspektrometri som specifikt markerar peptider som bär två ADP-ribos-enheter, vilket hjälper till att korrekt kartlägga var poly-modifieringar förekommer på proteiner.
Se subtila signaler där andra inte ser något
Med sina nya verktyg visar forskarna att de poly-specifika antikropparna detekterar mycket korta kedjor, långa kedjor och till och med fria ADP-ribospolymerer, och gör det med avsevärt högre känslighet än befintliga kommersiella reagenser. Antikropparna fungerar över olika aminosyralänkningar, inte bara serin, och kan visualisera poly-ADP-ribos i celler under förhållanden där tidigare verktyg inte visade någon signal alls, såsom i ostressade celler eller celler som växer i låg syrehalt. Parallellt affinitetsmognar teamet tidigare mono-specifika och sitespecifika antikroppar för att öka deras känslighet samtidigt som selektiviteten bibehålls. Tillsammans möjliggör denna verktygslåda samtidig avbildning av både mono- och poly-signaler i samma cell, vilket visar att poly-modifiering uppträder i lokaliserade nukleära fokus medan mono-modifiering bildar en mer diffus och långvarig våg över kromatin.
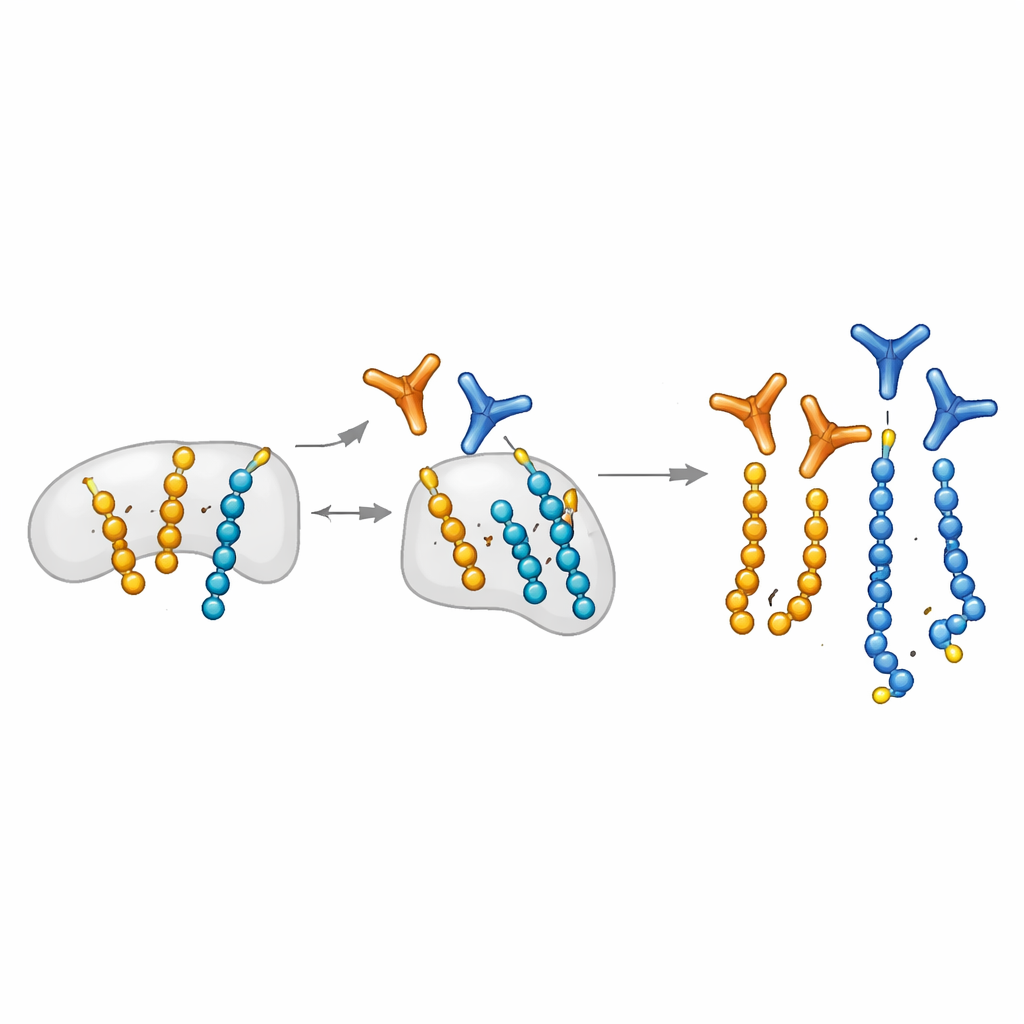
Hur förlust av XRCC1 omformar reparationsvågorna
XRCC1 fungerar normalt som ett skelett som hjälper PARP1 att binda till och sedan släppa från DNA-reparationsintermediärer. När XRCC1 försvinner blir PARP1 hyperaktivt och har tidigare kopplats till överproduktion av långa ADP-riboskedjor, ett tillstånd associerat med neurodegeneration. Med sitt förfinade antikroppssortiment visar författarna att XRCC1-förlust gör mer än att öka långa kedjor: den förstärker dramatiskt även mono-ADP-ribosyleringsvågen. Vid pågående DNA-skada från olika agenter visar celler utan XRCC1 högre och tidigare toppar av både långa och korta modifieringar, med tidpunkter som är specifika för skadetypen. Mono-modifiering förblir ofta mer stabil och jämnt fördelad än den snabbt fluktuerande poly-signalen. Studien identifierar också histon H1 som ett framträdande mono-modifierat mål vars ihållande märkning kan hålla kromatinet mer avspänt runt lesioner.
Från ändrade signaler till ändrad proteintrafik
Mono-ADP-ribos på serin kan själv ytterligare dekoreras genom en ovanlig kemisk koppling till ubikvitin och bilda en hybridmarkör kallad ADP-ribos-ubikvitinering. Ubikvitin-ligaset RNF114 känner igen denna sammansatta signal och dras till DNA-skadeplatser där det kan modifiera eller flytta andra proteiner. Med hjälp av ett specialiserat läsarprotein (ZUD) tillsammans med sina antikroppar visar författarna att XRCC1-brist ökar inte bara mono-ADP-ribos utan även denna hybridmark och rekryteringen av RNF114 till brott. Detta tyder på att felreglerad mono-signalering och dess ubikvitin-korsprat kan bidra till den cellulära stress och de sjukdomsfenotyper som ses när XRCC1 är muterat.
Vad detta betyder för förståelse och behandling av sjukdom
För en icke-specialist är huvudbudskapet att det som tidigare såg ut att vara en enda DNA-reparationssignal egentligen är två överlappande vågor av små kemiska märken, var och en med sin egen timing och konsekvenser. Genom att bygga högselektiva molekylära verktyg separerar denna studie dessa vågor och visar att förlust av XRCC1 inte bara förstärker den välkända utbrottet av långa kedjor utan också en varaktig ökning av enhetsmärkningar och deras kopplade ubikvitin-markörer. Dessa insikter förfinar vår bild av hur PARP1 fungerar, hjälper till att förklara varför defekter i XRCC1 och närliggande enzymer orsakar hjärnsjukdom, och erbjuder en verktygslåda som andra forskare kan använda för att dissekera ADP-ribosylering inom cancer, immunologi och vidare—möjligtvis med sikte på mer precis användning av PARP-riktade läkemedel.
Citering: Dauben, H., Mihaljević, M., Kolvenbach, A. et al. Versatile and sensitive detection of mono- and poly(ADP-ribosyl)ation reveals XRCC1-dependent remodelling of PARP1 signalling. Nat Commun 17, 3216 (2026). https://doi.org/10.1038/s41467-026-71311-4
Nyckelord: ADP-ribosylering, DNA-skadereparation, PARP1-signalering, XRCC1-brist, ubikvitinering