Clear Sky Science · zh
通过人工智能引导的结构景观分析挖掘抗体功能
这项研究为何重要
疫苗和抗体药物是对抗 COVID-19 的核心武器,但我们的免疫系统能产生几乎难以想象的大量抗体,其中大多数我们从未详尽研究。本文展示了人工智能如何读取抗体的基因序列并推断它们如何以及在哪里附着在冠状病毒刺突蛋白上,帮助科学家迅速筛选出那些既能中和病毒又能在病毒变异时保持活性的稀有分子。同样的策略也可能加速针对未来多种病原体的抗体药物开发。
将抗体序列转化为地图
作者将研究重心放在识别 SARS-CoV-2 刺突蛋白受体结合域(RBD)的抗体上,这是病毒用来抓取人类细胞的关键抓手。他们从公开可用的抗体–RBD 复合物结构和绘制病毒变化如何影响抗体结合的深度突变扫描实验中汇集了大量训练集。通过对这些数据进行聚类,研究者定义了 12 个不同的“表位类别”——RBD 上不同抗体反复识别的区域,每一类都与特征性的中和强度和广谱性相关联。
构建指向抗体功能的人工智能指南
在这个结构地图之上,团队构建了名为 RBD-AIM 的人工智能工具。首先,一个专门以抗体序列训练的语言模型分析抗体的重链和轻链的基因编码,并预测其所属的表位类别。随后一个结构预测步骤使用已知的三维模板和现代折叠算法来细化该抗体如何可能位于 RBD 上。由预测的三维比对得出的置信度评分帮助决定何时信任结构模型而不仅仅是基于序列的分类器。总体而言,这种组合方法在推测抗体的结合位点以及其可能阻断病毒的能力方面,优于传统的同源性搜索和若干最先进的结构预测器。
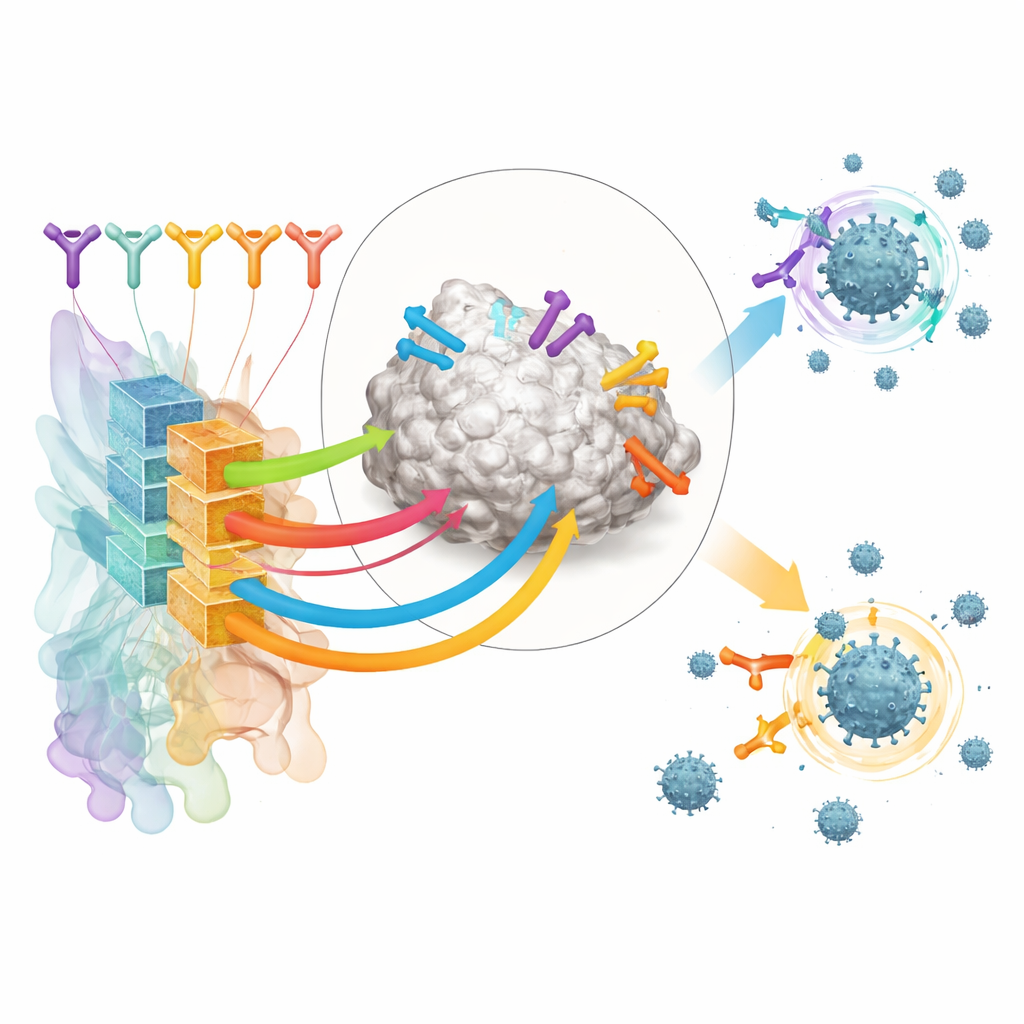
在实验室重建真实免疫反应
为了在真实的抗体集合上测试 RBD-AIM,研究人员重建了接种过 mRNA 疫苗(辉瑞–BioNTech)或腺病毒载体疫苗(Sputnik V)人群的原生 B 细胞库。通过微滴微流控技术,他们从单个 B 细胞捕获了重链和轻链的原始配对,并将所得片段展示在酵母细胞表面。与随机混合链的传统方法相比,这更好地保留了抗体的天然多样性。用荧光标记的 RBD,使他们能够分选出携带高亲和力 RBD 结合子的酵母细胞,其中包括那些直接与人类 ACE2 受体竞争同一刺突位点的抗体。
预测并验证哪些抗体真正有效
研究者将数十个从这些接种者中高度富集的 RBD 结合抗体提交给 RBD-AIM。该工具预测了每个抗体识别的表位类别、是否可能阻断 ACE2 以及对如 Delta 和 Omicron 等变体中发现的刺突突变的耐受性。正如预期,瞄准 ACE2 接触区域的抗体往往效力强但作用范围窄,对 Omicron 失去活性。相比之下,来自较远表位类别的一部分抗体(作者将其命名为 E221)被预测能在多种变体中保持中和活性。实验室结合和病毒中和测试证实了这些模式,晶体结构显示 RBD-AIM 的结构推测在详细接触表面层面常常是准确的。
从预测到动物保护
为检验这些人工智能优先选择的抗体能否作为真实药物,团队挑选了代表性分子:一种经典的阻断 ACE2 的抗体和一种通过更间接机制中和病毒的 E221 类抗体。在使用表达人体 ACE2 的小鼠进行的致死性 SARS-CoV-2 挑战模型中,任一抗体的单次低剂量给药都保护了所有受试动物,这与其预测的中和特征一致。进一步的结构和模拟工作表明,广谱活性的 E221 类抗体通过“冻结”RBD 中那些为高效受体结合所必需的灵活部分来发挥作用,这种机制对 ACE2 接触片段的精确形状不那么敏感。
对未来大流行的意义
从实用角度看,这项研究给出了一套可行的蓝图,将高通量展示技术与人工智能相结合,把原始抗体序列数据转化为功能性见解。研究人员不必再逐一费时表征每种抗体,而是可以快速扫描整个受体库,按效力和广谱性对有前途的候选者进行排序,并理解病毒蛋白的哪些区域最值得针对。尽管 RBD-AIM 是在 SARS-CoV-2 上训练的,作者表明只要有足够的结构和突变数据,同一策略可以扩展到其他病毒,指向一个未来:人工智能引导的“结构景观分析”帮助我们从自身免疫反应中挖掘下一代抗体疗法。
引用: Terekhov, S.S., Ivanisenko, N.V., Zhang, N. et al. Mining antibody functionality via AI-guided structural landscape profiling. Nat Commun 17, 4009 (2026). https://doi.org/10.1038/s41467-026-70553-6
关键词: 抗体发现, 人工智能, SARS-CoV-2 刺突蛋白, 表位绘图, 治疗性抗体