Clear Sky Science · ja
AI誘導型構造ランドスケープ解析による抗体機能の掘り下げ
この研究が重要な理由
ワクチンや抗体薬はCOVID-19に対する主要な武器となってきましたが、私たちの免疫系が生み出す抗体の多様性はほとんど想像を絶するほど広く、その大部分は詳細に研究されていません。本稿は、人工知能が抗体の遺伝配列を読み取り、どこにどのようにしてコロナウイルスのスパイクに結合するかを推定できることを示しています。この能力により、ウイルスを中和し変異に対しても活性を保つ稀な分子を迅速に選び出す手助けができます。同じ戦略は将来の多くの病原体に対する抗体医薬の探索を加速する可能性があります。
抗体配列を地図に変える
著者らは、SARS-CoV-2スパイクタンパクの受容体結合ドメイン(RBD)を認識する抗体に着目しました。RBDはウイルスがヒト細胞を捕らえるための重要な握り手です。彼らは、抗体–RBD複合体の公開された構造データと、ウイルスの変化が抗体結合に与える影響を記録したディープ変異走査(deep mutational scanning)の実験データから大規模な学習セットを構築しました。これらのデータをクラスタリングすることで、12の異なる「エピトープクラス」を定義しました。これらはRBD上の反復して現れる領域であり、各クラスはウイルス中和の強さや広がりという特徴と結びついています。
抗体機能へのAIガイドの構築
この構造マップの上に、研究チームはRBD-AIMと呼ばれるAIツールを構築しました。まず、抗体配列に特化して訓練された言語モデルが、抗体の重鎖と軽鎖の遺伝コードを解析し、どのエピトープクラスに属するかを予測します。次に、構造予測ステップで既知の3Dテンプレートと最新のフォールディングアルゴリズムを用いて、その抗体がRBD上にどのように座るかを精緻化します。予測された3D配置から導かれる信頼度スコアは、構造モデルを信用すべきか、より単純な配列ベースの分類器を優先すべきかの判断に役立ちます。全体として、この統合アプローチは、抗体の結合部位やウイルスをどれほど阻害する可能性があるかを推測する点で、従来のホモロジー検索や複数の最先端の構造予測器よりも優れた性能を示しました。
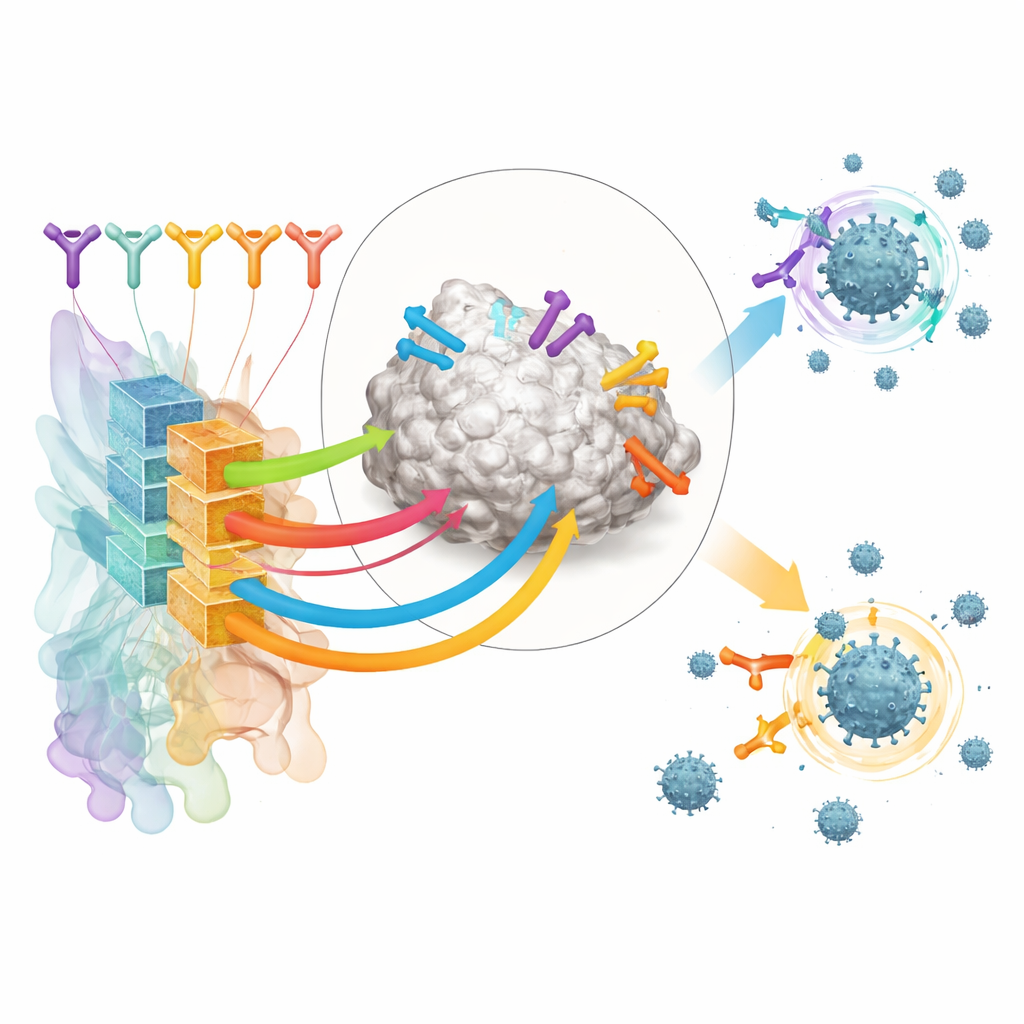
実際の免疫反応を実験室で再現する
現実的な抗体コレクションでRBD-AIMを試すために、研究者らはmRNAワクチン(Pfizer–BioNTech)またはアデノウイルスベクターワクチン(Sputnik V)でワクチン接種を受けた人々からの自然なB細胞レパートリーを再構築しました。ドロップレットマイクロフルイディクスを用いて、単一B細胞から抗体の重鎖と軽鎖の元の組合せを捕まえ、得られた断片を酵母細胞の表面にディスプレイしました。これにより、鎖をランダムに混ぜる従来法よりも自然な抗体多様性がはるかによく保存されました。蛍光標識されたRBDを使って、高親和性のRBD結合体を持つ酵母細胞を選別し、人のACE2受容体と同じスパイク上の部位を直接競合するものも含めて同定しました。
どの抗体が実際に効くかの予測と検証
これらのワクチン接種ドナーから強く富化された数十のRBD結合抗体をRBD-AIMで評価しました。ツールは各抗体がどのエピトープクラスを認識するか、ACE2を阻害する可能性があるか、DeltaやOmicronなどの変異株に含まれるスパイク変異に対してどれだけ耐性があるかを予測しました。予想どおり、ACE2接触領域を標的とする抗体は強力であるものの適用範囲が狭く、Omicronに対しては活性を失う傾向がありました。対照的に、著者らがE221と名付けたより離れた位置のエピトープクラスに属する一部の抗体は、変異株にわたって中和力を保持すると予測されました。実験室での結合試験とウイルス中和試験はこれらの傾向を確認し、結晶構造解析はRBD-AIMの構造予測が接触面の詳細に至るまでしばしば精度が高いことを示しました。
予測から動物での防護へ
これらのAI優先抗体が実際の治療薬になり得るかを確かめるため、研究チームは代表的な分子を選びました:古典的なACE2阻害抗体と、より間接的な機構で中和するE221クラスの抗体を1つずつです。ヒトACE2を発現するように遺伝子改変したマウスを用いる致死的なSARS-CoV-2チャレンジモデルでは、いずれの抗体も単回の低用量投与で処置した動物すべてを保護し、予測された中和プロファイルと一致しました。さらなる構造解析とシミュレーションは、広く作用するE221クラス抗体がRBDの柔軟な部分を「固定」することで効率的な受容体結合に必要な動きを抑え、ACE2接触パッチの厳密な形状に依存しにくい機序で作用している可能性を示唆しました。
将来のパンデミックへの意義
実用的な観点から、この研究は高スループットなディスプレイ技術とAIを組み合わせて、生の抗体配列データを機能的洞察に変える作業手順の動作する設計図を提供します。抗体を一つずつ丹念に特徴付ける代わりに、研究者は全レパートリーを迅速にスキャンし、効力と網羅性で有望な候補をランク付けし、ウイルス蛋白のどの領域を標的にすべきかを理解できます。RBD-AIMはSARS-CoV-2で訓練されましたが、著者らは十分な構造および変異データがあれば同じ戦略を他のウイルスにも拡張できることを示しており、AI誘導の「構造ランドスケープ解析」によって次世代の抗体治療を自らの免疫応答から掘り出す未来を示唆しています。
引用: Terekhov, S.S., Ivanisenko, N.V., Zhang, N. et al. Mining antibody functionality via AI-guided structural landscape profiling. Nat Commun 17, 4009 (2026). https://doi.org/10.1038/s41467-026-70553-6
キーワード: 抗体探索, 人工知能, SARS-CoV-2スパイク, エピトープマッピング, 治療用抗体