Clear Sky Science · he
כריית תפקוד נוגדנים באמצעות מיפוי נופי מבני בהנחיית בינה מלאכותית
מדוע מחקר זה חשוב
חיסונים ותרופות מבוססות נוגדנים היו כלי מרכזי במאבק בקוביד-19, אך מערכת החיסון שלנו מייצרת מגוון כמעט בלתי נתפס של נוגדנים, שרובם לא נחקרים לעומק. מאמר זה ממחיש כיצד בינה מלאכותית יכולה לקרוא רצפי גנים של נוגדנים ולהסיק היכן וכיצד הם נקשרים לחלבון הספייק של הווירוס, ובכך לסייע למדענים במהירות לזהות את המולקולות הנדירות שמנטרלות את הווירוס ועדיין פעילות כשהוא משתנה. אותה אסטרטגיה יכולה גם לזרז את החיפוש אחר תרופות נוגדניות נגד פתוגנים עתידיים רבים.
הפיכת רצפי נוגדנים למפה
המחברים מתמקדים בנוגדנים שמזהים את תחום קשירת הרצפטור (RBD) של חלבון הספייק של SARS-CoV-2, אחיזת מפתח שהווירוס משתמש בה כדי לתפוס תאים אנושיים. הם אספו מערך אימון גדול ממבנים זמינים לציבור של קומפלקסים נוגדן–RBD ומהתנסות סריקה מוטציונית עמוקה שממפה כיצד שינויים בווירוס משפיעים על קשירת הנוגדן. על ידי אשכולת הנתונים הללו הם הגדירו 12 "מחלקות אפיטופ" מובחנות — אזורים חוזרים על עצמם ב-RBD שפותחים את יעד הנוגדנים השונים, כל אחת מקושרת לעוצמה ואבוס (breadth) אופייניים של נטרול הווירוס.
בניית מדריך בינה מלאכותית לתפקוד נוגדנים
על בסיס המפה המבנית בנויה מערכת בינה מלאכותית בשם RBD-AIM. קודם כל, מודל שפה שאומן במיוחד על רצפי נוגדנים מנתח את הקוד הגנטי של השרשרות הכבדות והקלות של הנוגדן ומנבא לאיזו מחלקת אפיטופ הוא שייך. לאחר מכן שלב של חיזוי מבנה משתמש בתבניות תלת־ממד מוכרות ובאלגוריתמים מודרניים לקיפול כדי לחדד כיצד הנוגדן צפוי לשבת על ה-RBD. דירוג ביטחון שמקורו בהתאמה התלת־ממדית החזויה מסייע להחליט מתי לסמוך על המודל המבני מול הממיין הפשוט מבוסס הרצף. בסך הכל הגישה המשולבת הזאת עולה על חיפושי הומולוגיה מסורתיים וכמה מנבאי מבנה מהשורה הראשונה בתחזית היכן נוגדן נקשר וכמה טוב סביר שיחסום את הווירוס.
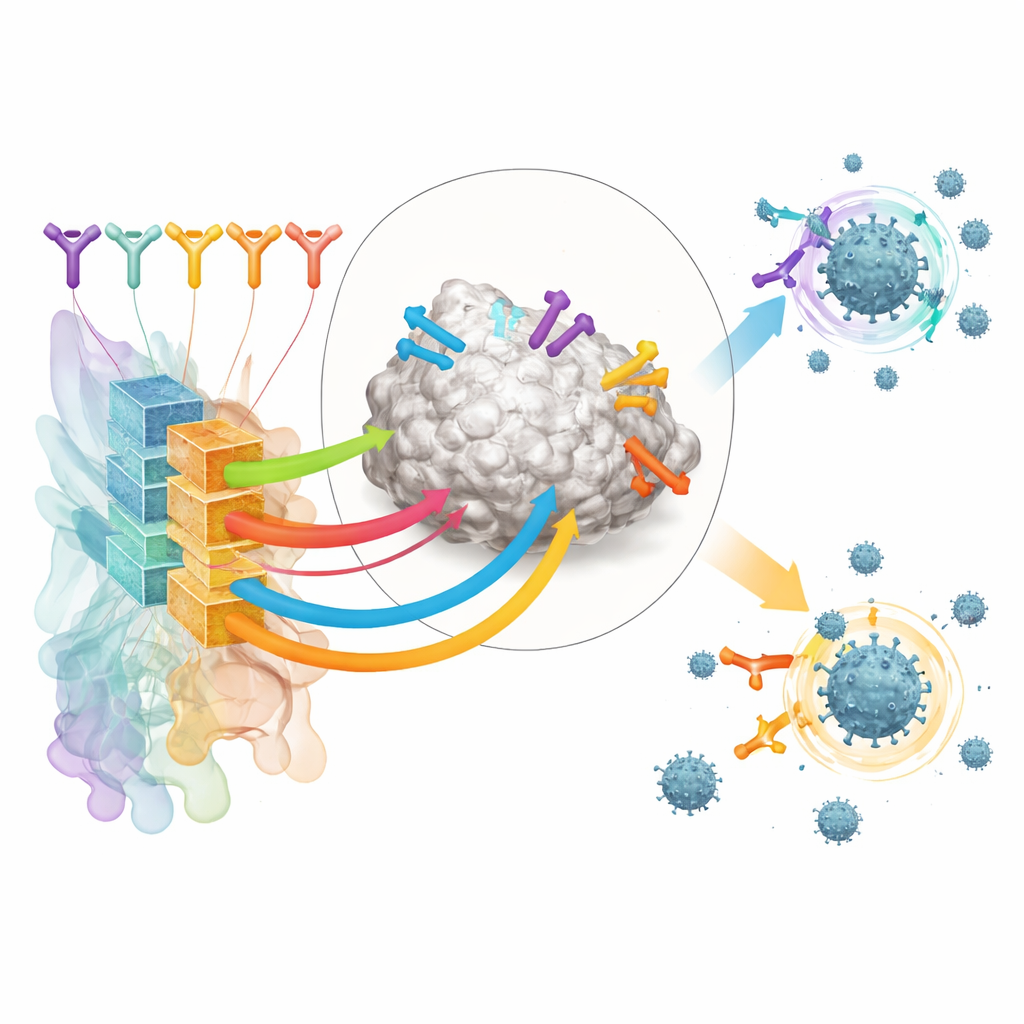
שיחזור תגובות חיסוניות אמיתיות במעבדה
כדי לבדוק את RBD-AIM על אוספים מציאותיים של נוגדנים, החוקרים שיחזרו מערכת B תאית מקומית מאנשים שחוסנו בחיסון mRNA (Pfizer–BioNTech) או בחיסון מבוסס וקטור אדנו-וירלי (Sputnik V). באמצעות מיקרו־פלואידיקה בטיפות תפסו את הצמדים המקוריים של השרשרות הכבדות והקלות מנויטרון B בודד והציגו את הקטעי הנוגדן המתקבלים על פני שטח תאי שמרים. שיטת זו שמרה על המגוון הטבעי של הנוגדנים הרבה יותר טוב משיטות מקובלות שמערבבות שרשרות באקראי. RBD שסומן בפלורסצנציה איפשר להם למיין תאי שמרים הנושאים קושרי RBD בעלי זיקה גבוהה, כולל אלה שמתחרים ישירות עם הרצפטור האנושי ACE2 על אותו אזור בספייק.
חיזוי ואימות אילו נוגדנים באמת עובדים
עשרות נוגדנים עם התעשרות חזקה לקשירת RBD ממנות אלה נבדקו באמצעות RBD-AIM. הכלי חזה לאיזו מחלקת אפיטופ כל נוגדן מזהה, האם סביר שיחסום ACE2 וכמה עמיד הוא עשוי להיות לשינויים בספייק שנמצאים בווריאנטים כגון דלתא ואומיקרון. כצפוי, נוגדנים הפונים לאזור המגע עם ACE2 נטו להיות רבי עוצמה אך מצומצמים בטווח, ואיבדו פעילות נגד אומיקרון. לעומת זאת, תת־קבוצה של נוגדנים ממחלקת אפיטופ מרוחקת יותר (שהמחברים כינו E221) חזו שישמרו על כוח ניטרול מפלח ורחב נגד וריאנטים. בדיקות קשירה ונטרול ויראלי במעבדה אישרו דפוסים אלה, ומבנים גבישים הראו שהשערות המבניות של RBD-AIM היו לעתים קרובות מדויקות אפילו עד פני שטח המגע המפורטות.
מניב חיזוי להגנה בחיות
כדי לבדוק האם הנוגדנים שמדורגים על ידי ה-AI יכולים לשמש כתרופות אמיתיות, הצוות בחר מולקולות מייצגות: נוגדן קלאסי החוסם ACE2 ואחד ממשפחת E221 שמנטרל במנגנון עקיף יותר. במודל אתגר קטלני של SARS-CoV-2 בעכברים מהונדסים לבטא ACE2 אנושי, מנה בודדת נמוכה של כל אחד מהנוגדנים הגנה על כל בעלי החיים המטופלים, בהתאמה לפרופילי הנטרול שחזו להם. עבודות מבניות וסימולציה נוספות הציעו שנוגדן ממשפחת E221, הפעיל לרוחב, פועל על ידי "הקפאת" חלקים גמישים של ה-RBD הדרושים לאינטראקציה יעילה עם הרצפטור — מנגנון הפחות פגיע לצורה המדויקת של אזור מגע ה-ACE2.
מה משמעות הדבר למגפות עתידיות
במונחים מעשיים, המחקר מספק מתווה עובד לשילוב טכנולוגיות תצוגה בקצב גבוה עם בינה מלאכותית כדי להפוך נתוני רצף נוגדנים גולמיים לתובנות פונקציונליות. במקום לאפיין בקפידה נוגדן אחד בכל פעם, חוקרים יכולים כעת לסרוק מהר רגיסטרים שלמים, לדרג מועמדים מבטיחים לפי עוצמה וטווח, ולהבין אילו אזורים בחלבון ויראלי חשובים ביותר לפעולה. אף על פי ש-RBD-AIM אומן על SARS-CoV-2, המחברים מראים שלפני מספקים מבניים ומוטציוניים מתאימים אותה אסטרטגיה יכולה להתרחב לוירוסים אחרים, ומציגה עתיד שבו "מיפוי נופי מבני" בהנחיית AI עוזר לנו לכרות מתוך תגובות החיסון שלנו תרופות נוגדניות בדור הבא.
ציטוט: Terekhov, S.S., Ivanisenko, N.V., Zhang, N. et al. Mining antibody functionality via AI-guided structural landscape profiling. Nat Commun 17, 4009 (2026). https://doi.org/10.1038/s41467-026-70553-6
מילות מפתח: גילוי נוגדנים, בינה מלאכותית, חלבון הספייק של SARS-CoV-2, מיפוי אתר אפיטופי, נוגדנים טיפוליים