Clear Sky Science · de
Antikörperfunktion durch KI-geführte strukturelle Landschaftsprofilierung erkunden
Warum diese Forschung wichtig ist
Impfstoffe und Antikörpertherapien waren zentrale Waffen gegen COVID-19, doch unser Immunsystem erzeugt eine nahezu unvorstellbar große Vielfalt an Antikörpern, von denen die meisten nie im Detail untersucht werden. Dieses Papier zeigt, wie künstliche Intelligenz Antikörper‑Gensequenzen lesen und vorhersagen kann, wo und wie sie am Coronavirus‑Spike andocken. Das hilft Forschenden, schnell die seltenen Moleküle herauszufiltern, die das Virus neutralisieren und zugleich gegen Mutationen robust bleiben. Dieselbe Strategie könnte die Suche nach Antikörpermedikamenten gegen viele zukünftige Erreger beschleunigen.
Antikörpersequenzen in eine Karte verwandeln
Die Autorinnen und Autoren konzentrieren sich auf Antikörper, die die rezeptorbindende Domäne (RBD) des SARS‑CoV‑2‑Spikeproteins erkennen – einen wesentlichen Griff, den das Virus nutzt, um menschliche Zellen zu fassen. Sie stellten einen großen Trainingssatz aus öffentlich verfügbaren Strukturen von Antikörper–RBD‑Komplexen und aus Deep‑Mutational‑Scanning‑Experimenten zusammen, die aufzeichnen, wie Veränderungen im Virus die Antikörperbindung beeinflussen. Durch Clusteranalyse dieser Daten definierten sie 12 unterschiedliche „Epitopklassen“ – wiederkehrende Regionen auf der RBD, die von verschiedenen Antikörpern angezielt werden und jeweils mit charakteristischer Stärke und Reichweite der Virenneutralisation verbunden sind.
Ein KI‑Leitfaden für Antikörperfunktion
Auf dieser strukturellen Karte baut das Team ein KI‑Werkzeug namens RBD‑AIM auf. Zunächst analysiert ein speziell auf Antikörpersequenzen trainiertes Sprachmodell den genetischen Code der schweren und leichten Ketten eines Antikörpers und sagt voraus, zu welcher Epitopklasse er gehört. Anschließend verfeinert ein Strukturvorhersageschritt mithilfe bekannter 3D‑Vorlagen und moderner Faltungsalgorithmen, wie dieser Antikörper wahrscheinlich auf der RBD sitzt. Eine Vertrauensbewertung, abgeleitet aus der vorhergesagten 3D‑Ausrichtung, hilft zu entscheiden, wann dem strukturellen Modell mehr zu trauen ist als dem einfacheren sequenzbasierten Klassifikator. Insgesamt übertrifft dieser kombinierte Ansatz traditionelle Homologiesuchen und mehrere hochmoderne Strukturvorhersager darin, vorherzusagen, wo ein Antikörper bindet und wie gut er das Virus wahrscheinlich blockiert.
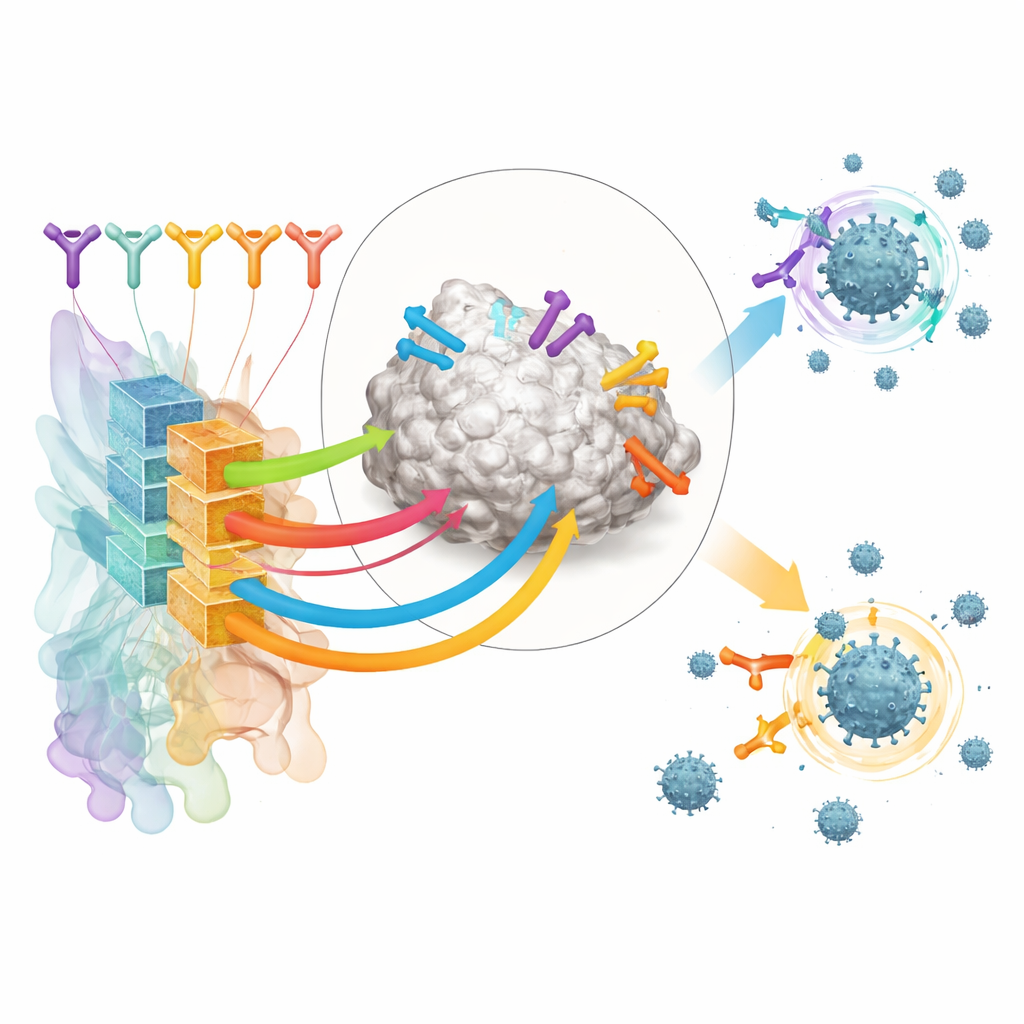
Rekonstruierte Immunantworten im Labor nachbilden
Um RBD‑AIM an realistischen Antikörperkollektionen zu testen, rekonstruierten die Forschenden native B‑Zell‑Repertoires von Personen, die entweder mit einem mRNA‑Impfstoff (Pfizer–BioNTech) oder einem Adenovirusvektorimpfstoff (Sputnik V) geimpft wurden. Mithilfe von Tropfen‑Mikrofluidik erfassten sie die ursprünglichen Paarungen von schweren und leichten Antikörperketten aus einzelnen B‑Zellen und zeigten die resultierenden Fragmente auf der Oberfläche von Hefezellen. Dadurch wurde die natürliche Antikörperdiversität deutlich besser bewahrt als bei konventionellen Methoden, die Ketten zufällig mischen. Fluoreszent markierte RBD ermöglichte es, Hefezellen mit hochaffinen RBD‑Bindern auszusortieren, einschließlich solcher, die direkt mit dem menschlichen ACE2‑Rezeptor um dieselbe Stelle am Spike konkurrieren.
Vorhersagen und Validierung: welche Antikörper wirklich wirken
Dutzende stark angereicherte RBD‑bindende Antikörper aus diesen geimpften Spendern wurden anschließend mit RBD‑AIM analysiert. Das Tool sagte voraus, welche Epitopklasse jeder Antikörper erkannte, ob er wahrscheinlich ACE2 blockiert und wie robust er gegenüber Spike‑Mutationen in Varianten wie Delta und Omikron sein könnte. Wie zu erwarten war, waren Antikörper, die auf den ACE2‑Kontaktbereich zielten, in der Regel potent, aber eng in ihrer Wirksamkeit und verloren gegen Omikron an Aktivität. Im Gegensatz dazu wurde eine Untergruppe von Antikörpern aus einer weiter entfernt liegenden Epitopklasse (von den Autorinnen und Autoren E221 genannt) als wahrscheinlich neutralisierend über Varianten hinweg eingeschätzt. Labortests zur Bindung und Virenneutralisation bestätigten diese Muster, und Kristallstrukturen zeigten, dass RBD‑AIMs strukturelle Vorhersagen oft bis hin zu den detaillierten Kontaktflächen genau waren.
Von der Vorhersage zum Schutz bei Tieren
Um zu prüfen, ob diese von der KI priorisierten Antikörper als echte Medikamente wirken können, wählte das Team repräsentative Moleküle aus: einen klassischen ACE2‑blockierenden Antikörper und einen E221‑Klassen‑Antikörper, der durch einen indirekteren Mechanismus neutralisiert. In einem letalen SARS‑CoV‑2‑Challenge‑Modell mit Mäusen, die so verändert wurden, dass sie menschliches ACE2 exprimieren, schützte eine einzige niedrige Dosis jedes Antikörpers alle behandelten Tiere, entsprechend ihren vorhergesagten neutralisierenden Profilen. Weitere strukturelle und Simulationsarbeiten deuteten darauf hin, dass der breit wirksame E221‑Antikörper dadurch wirkt, dass er flexible Teile der RBD „einfriert“, die für eine effiziente Rezeptorbindung benötigt werden – ein Mechanismus, der weniger anfällig für die genaue Form des ACE2‑Kontaktbereichs ist.
Was das für zukünftige Pandemien bedeutet
Praktisch liefert diese Studie eine funktionsfähige Blaupause dafür, wie Hochdurchsatz‑Anzeigeverfahren mit KI kombiniert werden können, um rohe Antikörpersequenzdaten in funktionelle Einsichten zu verwandeln. Anstatt mühsam einen Antikörper nach dem anderen zu charakterisieren, können Forschende nun ganze Repertoires schnell screenen, vielversprechende Kandidaten nach Potenz und Reichweite priorisieren und verstehen, welche Regionen eines Virusproteins am wichtigsten sind. Obwohl RBD‑AIM auf SARS‑CoV‑2 trainiert wurde, zeigen die Autorinnen und Autoren, dass sich die gleiche Strategie mit ausreichenden strukturellen und mutationalen Daten auf andere Viren übertragen lässt und auf eine Zukunft hindeutet, in der KI‑geführte „strukturelle Landschaftsprofilierung“ uns hilft, unsere eigenen Immunantworten nach Wirkstoffen der nächsten Generation zu durchforsten.
Zitation: Terekhov, S.S., Ivanisenko, N.V., Zhang, N. et al. Mining antibody functionality via AI-guided structural landscape profiling. Nat Commun 17, 4009 (2026). https://doi.org/10.1038/s41467-026-70553-6
Schlüsselwörter: Antikörperentdeckung, Künstliche Intelligenz, SARS-CoV-2-Spike, Epitopkartierung, therapeutische Antikörper