Clear Sky Science · nl
Antistoffunctionaliteit ontdekken via AI-gestuurde structurele landschapsprofilering
Waarom dit onderzoek ertoe doet
Vaccins en antistofgeneesmiddelen waren centrale wapens tegen COVID-19, maar ons immuunsysteem produceert een bijna onvoorstelbaar grote variëteit aan antilichamen, waarvan de meeste nooit in detail worden bestudeerd. Dit artikel laat zien hoe kunstmatige intelligentie antistof-genetische sequenties kan lezen en kan afleiden waar en hoe ze zich aan de coronavirus-spike hechten, zodat wetenschappers snel de zeldzame moleculen kunnen selecteren die het virus neutraliseren en actief blijven naarmate het muteert. Diezelfde strategie kan het zoeken naar antistofgeneesmiddelen tegen veel toekomstige pathogenen versnellen.
Antistofsequenties omzetten in een kaart
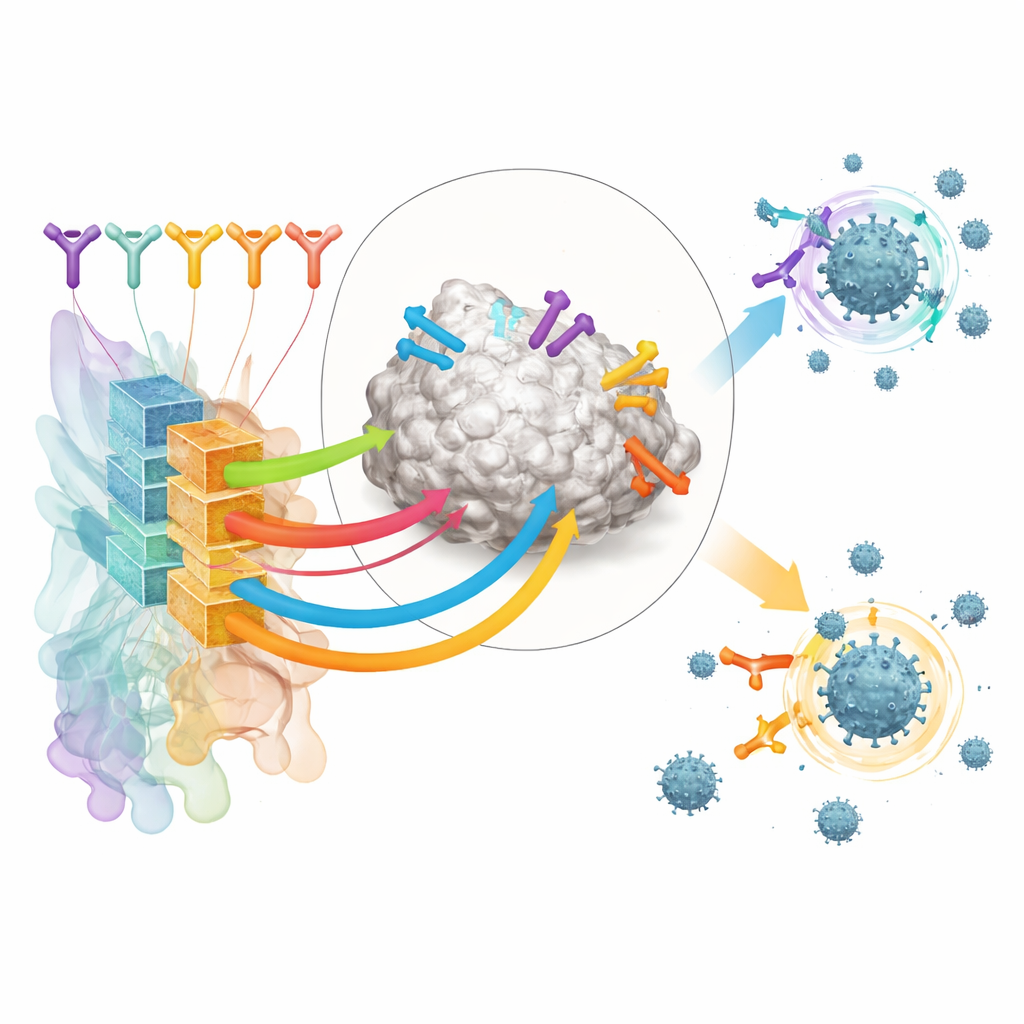
De auteurs richten zich op antilichamen die het receptor-bindende domein (RBD) van het SARS-CoV-2-spike-eiwit herkennen, een belangrijk handvat dat het virus gebruikt om menselijke cellen vast te grijpen. Ze stelden een grote trainingsset samen uit publiek beschikbare structuren van antistof–RBD-complexen en uit deep mutational scanning-experimenten die in kaart brengen hoe veranderingen in het virus de antistoftoewijzing beïnvloeden. Door deze gegevens te clusteren, definieerden ze 12 verschillende “epitoopklassen” – terugkerende regio’s op de RBD die door verschillende antilichamen worden aangetarget, elk geassocieerd met karakteristieke sterkte en breedte van virusneutralisatie.
Een AI-gids bouwen voor antistoffunctie
Bovenop deze structurele kaart bouwde het team een AI-hulpmiddel genaamd RBD-AIM. Eerst analyseert een taalmodel dat specifiek op antistofsequenties is getraind de genetische code van de zware en lichte ketens van een antistof en voorspelt tot welke epitoopklasse het behoort. Vervolgens gebruikt een structuurvoorspellingsstap bekende 3D-templates en moderne vouwalgoritmen om te verfijnen hoe dat antistof waarschijnlijk op de RBD zit. Een confidentiescore, afgeleid van de voorspelde 3D-uitlijning, helpt beslissen wanneer men het structurele model kan vertrouwen versus de eenvoudigere sequentiegebaseerde classifier. Al met al overtreft deze gecombineerde aanpak traditionele homologiezoektochten en verschillende state-of-the-art structuurvoorspellers in het raden waar een antistof bindt en hoe goed het waarschijnlijk het virus blokkeert.
Reconstructie van echte immuunreacties in het laboratorium
Om RBD-AIM op realistische antistofverzamelingen te testen, herbouwden de onderzoekers oorspronkelijke B-celrepertoires van mensen die waren gevaccineerd met ofwel een mRNA-vaccin (Pfizer–BioNTech) of een adenovirale vectorvaccin (Sputnik V). Met behulp van droplet-microfluidica vingen ze de oorspronkelijke koppelingen van zware en lichte antistofketens van individuele B-cellen en toonden de resulterende fragmenten op het oppervlak van gistcellen. Dit behield de natuurlijke diversiteit aan antilichamen veel beter dan conventionele methoden die ketens willekeurig mixen. Fluorescent gelabelde RBD stelde hen in staat gistcellen met hoogaffiene RBD-binders te sorteren, inclusief diegenen die direct concurreren met de menselijke ACE2-receptor voor hetzelfde gebied op de spike.
Voorspellen en valideren welke antilichamen echt werken
Duzenden sterk verrijkte RBD-bindende antilichamen van deze gevaccineerde donors werden vervolgens door RBD-AIM gehaald. Het hulpmiddel voorspelde welke epitoopklasse elk antistof herkende, of het waarschijnlijk ACE2 blokkeerde en hoe robuust het mogelijk zou zijn tegen spike-mutaties die in varianten zoals Delta en Omicron worden aangetroffen. Zoals te verwachten viel, waren antilichamen die zich op het ACE2-contactgebied richtten vaak krachtig maar smal van reikwijdte en verloren ze activiteit tegen Omicron. Daarentegen werd een subset antilichamen uit een meer verwijderd gelegen epitoopklasse (door de auteurs E221 genoemd) voorspeld hun neutraliserende werkzaamheid over varianten heen te behouden. Laboratoriumbinding- en virusneutralisatietesten bevestigden deze patronen, en kristalstructuren toonden dat de structurele schattingen van RBD-AIM vaak nauwkeurig waren tot in de gedetailleerde contactoppervlakken.
Van voorspelling naar bescherming in dieren
Om te onderzoeken of deze door AI-geprioriteerde antilichamen als echte geneesmiddelen konden dienen, selecteerde het team representatieve moleculen: één klassiek ACE2-blokkerend antistof en één E221-klasse antistof die neutraliseert via een indirecter mechanisme. In een dodelijk SARS-CoV-2-uitdagingmodel met muizen die zodanig zijn gemodificeerd dat ze menselijke ACE2 tot expressie brengen, beschermde een enkele lage dosis van elk antistof alle behandelde dieren, wat overeenkomt met hun voorspelde neutralisatieprofielen. Verdere structurele en simulatieanalyses suggereerden dat het breedwerkzame E221-klasse antistof werkt door flexibele delen van de RBD te “bevriezen” die nodig zijn voor efficiënte receptorbinding, een mechanisme dat minder kwetsbaar is voor de precieze vorm van het ACE2-contactgebied.
Wat dit betekent voor toekomstige pandemieën
In praktische zin levert deze studie een werkend stappenplan voor het combineren van hoogdoorvoertechnologieën voor display met AI om ruwe antistofsequentiegegevens in functioneel inzicht om te zetten. In plaats van één antistof tegelijk moeizaam te karakteriseren, kunnen onderzoekers nu hele repertoires snel doorzoeken, veelbelovende kandidaten rangschikken op potentie en breedte, en begrijpen welke regio’s van een viraal eiwit het belangrijkst zijn om te targeten. Hoewel RBD-AIM op SARS-CoV-2 is getraind, tonen de auteurs aan dat bij voldoende structurele en mutationale gegevens dezelfde strategie kan worden uitgebreid naar andere virussen, wat wijst op een toekomst waarin AI-gestuurde “structurele landschapsprofilering” ons helpt onze eigen immuunresponsen te doorzoeken op zoek naar antistoftherapieën van de volgende generatie.
Bronvermelding: Terekhov, S.S., Ivanisenko, N.V., Zhang, N. et al. Mining antibody functionality via AI-guided structural landscape profiling. Nat Commun 17, 4009 (2026). https://doi.org/10.1038/s41467-026-70553-6
Trefwoorden: antistofontdekking, kunstmatige intelligentie, SARS-CoV-2 spike, epitoopmapping, therapeutische antilichamen