Clear Sky Science · ru
Изучение функции антител с помощью ИИ через профилирование структурного ландшафта
Почему это исследование важно
Вакцины и антитела-препараты были ключевыми средствами борьбы с COVID-19, однако наша иммунная система порождает почти невообразимо большое разнообразие антител, большинство из которых мы никогда подробно не исследуем. В этой работе показано, как искусственный интеллект может «читать» генетические последовательности антител и предсказывать, где и как они прикрепляются к шипу коронавируса, помогая учёным быстро отбирать редкие молекулы, которые одновременно нейтрализуют вирус и сохраняют активность при его мутациях. Та же стратегия может ускорить поиск антительных лекарств против многих будущих патогенов.
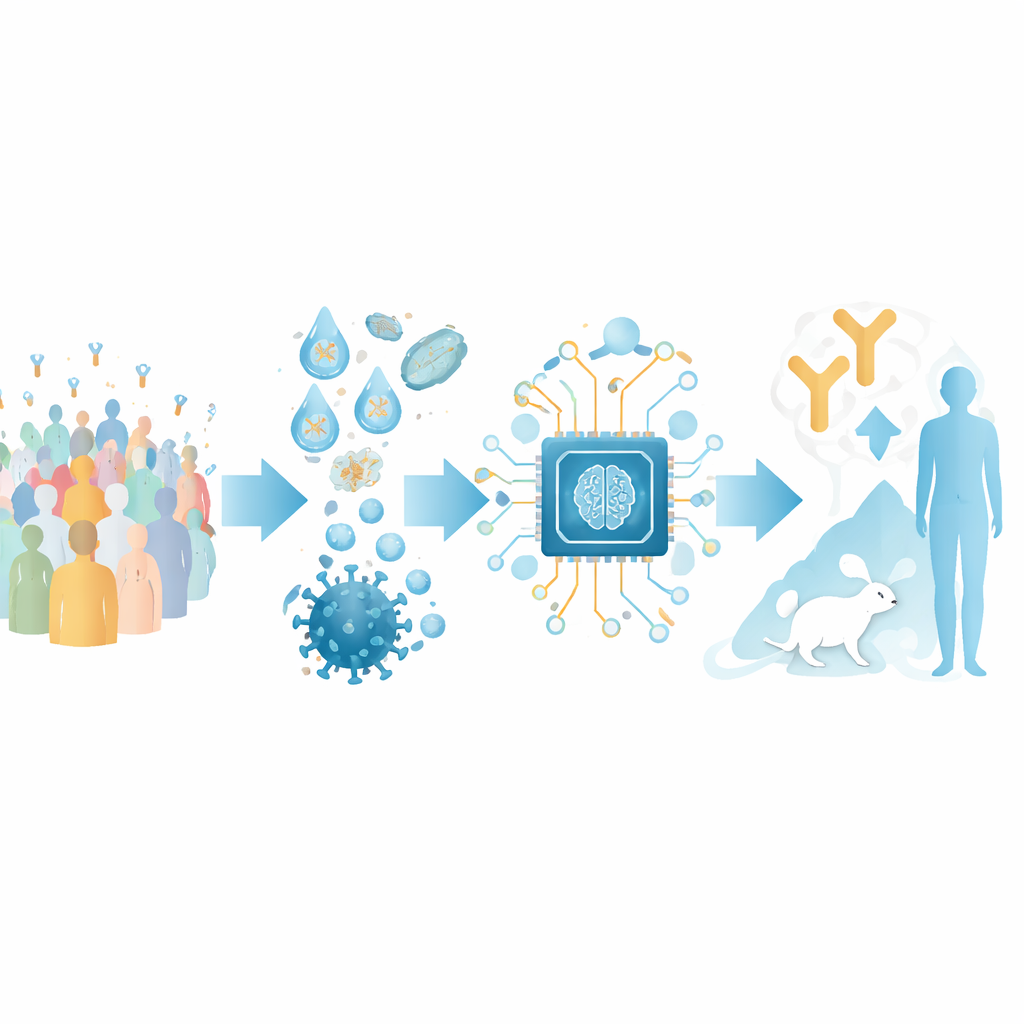
Преобразование последовательностей антител в карту
Авторы сосредоточились на антителах, распознающих домен связывания рецептора (RBD) шипа SARS-CoV-2 — ключевую «ручку», которой вирус захватывает человеческие клетки. Они собрали большую обучающую выборку из общедоступных структур комплексов антитела с RBD и из экспериментов глубокого мутационного сканирования, которые показывают, как изменения в вирусе влияют на связывание антител. Кластеризуя эти данные, они выделили 12 различных «классов эпитопов» — повторяющихся областей на RBD, на которые нацеливаются разные антитела, каждый из которых связан с характерной силой и широтой нейтрализации вируса.
Создание ИИ-направителя для функции антител
На основе этой структурной карты команда создала инструмент ИИ под названием RBD-AIM. Сначала языковая модель, обученная специально на последовательностях антител, анализирует генетический код тяжёлой и лёгкой цепей антитела и предсказывает, к какому классу эпитопа оно относится. Затем шаг предсказания структуры использует известные 3D-шаблоны и современные алгоритмы сворачивания для уточнения того, как это антитело, вероятно, располагается на RBD. Оценка уверенности, выведенная из предсказанного 3D-выравнивания, помогает решить, когда стоит полагаться на структурную модель, а когда — на более простую классификацию по последовательности. В целом этот комбинированный подход превосходит традиционный поиск по гомологии и несколько современных предикторов структуры при угадывании места связывания антитела и того, насколько хорошо оно, вероятно, блокирует вирус.
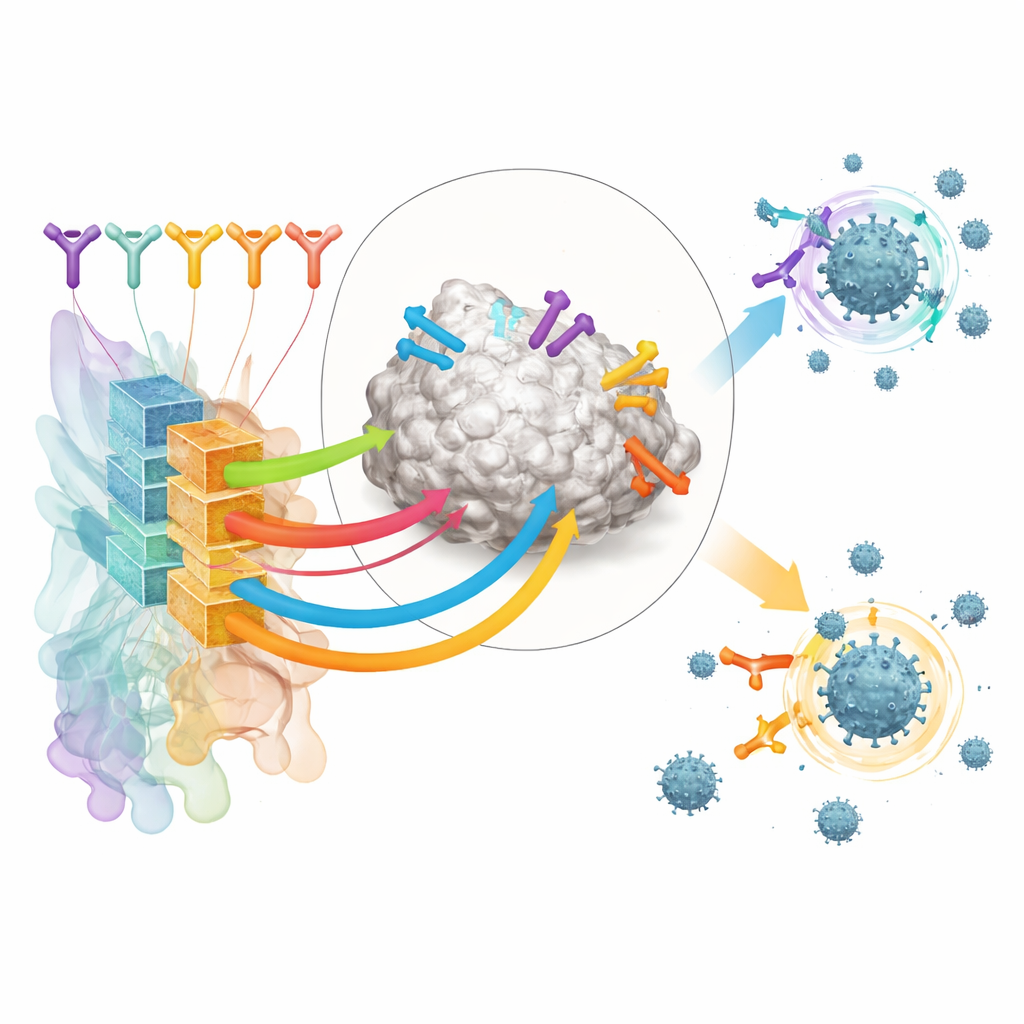
Воссоздание реальных иммунных ответов в лаборатории
Чтобы проверить RBD-AIM на реалистичных коллекциях антител, исследователи реконструировали нативные репертуары B-клеток у людей, вакцинированных либо мРНК-вакциной (Pfizer–BioNTech), либо аденовирусным вектором (Sputnik V). С помощью микрофлюидных капель они захватывали исходные пары тяжёлых и лёгких цепей антител из отдельных B-клеток и экспонировали полученные фрагменты на поверхности дрожжевых клеток. Это лучше сохраняло природное разнообразие антител по сравнению с обычными методами, которые случайно смешивают цепи. Флуоресцентно меченый RBD позволял сортировать дрожжевые клетки, несущие высокоафинные RBD-связывающие антитела, в том числе те, которые напрямую конкурируют с человеческим рецептором ACE2 за ту же область на шипе.
Прогнозирование и валидация действительно работающих антител
Дюжины сильно обогащённых RBD-связывающих антител от этих вакцинированных доноров были затем пропущены через RBD-AIM. Инструмент предсказывал, к какому классу эпитопа принадлежит каждое антитело, блокирует ли оно, вероятно, ACE2 и насколько устойчиво оно может быть к мутациям шипа, встречающимся в вариантах, таких как Дельта и Омикрон. Как и ожидалось, антитела, нацеленные на область контакта с ACE2, как правило, были мощными, но узкими по спектру, теряя активность против Омикрона. Напротив, подмножество антител из более удалённого класса эпитопов (именуемого авторами E221) прогнозировалось как сохраняющее нейтрализующую активность против вариантов. Лабораторные тесты связывания и нейтрализации вируса подтвердили эти закономерности, а кристаллические структуры показали, что структурные предположения RBD-AIM часто были точны вплоть до детализированных контактов поверхности.
От предсказания к защите в животных моделях
Чтобы проверить, могут ли антитела, выбранные ИИ, выступать в роли реальных лекарств, команда отобрала репрезентативные молекулы: одно классическое антитело, блокирующее ACE2, и одно антитело класса E221, нейтрализующее более косвенным механизмом. В летальной модели заражения SARS-CoV-2 у мышей, генетически модифицированных для экспрессии человеческого ACE2, одна низкая доза любого из антител защитила всех обработанных животных, что согласуется с их предсказанными нейтрализующими профилями. Дальнейшие структурные и моделирующие исследования предположили, что широко активное антитело класса E221 действует, «замораживая» гибкие участки RBD, необходимые для эффективного взаимодействия с рецептором — механизм, менее уязвимый к точной форме контактной области с ACE2.
Что это значит для будущих пандемий
Практически эта работа даёт рабочую схему сочетания высокопроизводительных технологий дисплея с ИИ для преобразования сырых данных о последовательностях антител в функциональные инсайты. Вместо того чтобы утомительно характеризовать по одному антителу, исследователи теперь могут быстро сканировать целые репертуары, ранжировать перспективные кандидаты по мощности и широте действия и понимать, какие участки вирусного белка наиболее важно нацеливать. Хотя RBD-AIM был обучен на SARS-CoV-2, авторы показывают, что при достаточном объёме структурных и мутационных данных та же стратегия может быть расширена на другие вирусы, указывая на будущее, в котором ИИ-управляемое «профилирование структурного ландшафта» поможет нам извлекать из собственной иммунной памяти антитела для лекарств следующего поколения.
Цитирование: Terekhov, S.S., Ivanisenko, N.V., Zhang, N. et al. Mining antibody functionality via AI-guided structural landscape profiling. Nat Commun 17, 4009 (2026). https://doi.org/10.1038/s41467-026-70553-6
Ключевые слова: открытие антител, искусственный интеллект, шип белка SARS-CoV-2, картирование эпитопов, терапевтические антитела