Clear Sky Science · pt
Minerando a funcionalidade de anticorpos por meio de perfilamento estrutural guiado por IA
Por que esta pesquisa importa
Vacinas e medicamentos à base de anticorpos têm sido armas centrais contra a COVID-19, mas nossos sistemas imunes geram uma variedade quase inimaginável de anticorpos, a maioria dos quais nunca estudamos em detalhe. Este artigo mostra como a inteligência artificial pode ler sequências genéticas de anticorpos e inferir onde e como eles se prendem à proteína spike do coronavírus, ajudando os cientistas a identificar rapidamente as moléculas raras que tanto neutralizam o vírus quanto permanecem ativas conforme ele muta. A mesma estratégia pode acelerar a busca por medicamentos à base de anticorpos contra muitos patógenos futuros.
Transformando sequências de anticorpos em um mapa
Os autores concentram-se em anticorpos que reconhecem o domínio de ligação ao receptor (RBD) da proteína spike do SARS-CoV-2, uma alça chave que o vírus usa para se conectar às células humanas. Eles montaram um grande conjunto de treinamento a partir de estruturas públicas de complexos anticorpo–RBD e de experimentos de varredura mutacional profunda que mapeiam como alterações no vírus afetam a ligação dos anticorpos. Ao agrupar esses dados, definiram 12 “classes de epítopo” distintas — regiões recorrentes no RBD que diferentes anticorpos miram, cada uma associada a características específicas de força e amplitude de neutralização viral.
Construindo um guia de IA para a função dos anticorpos
Sobre esse mapa estrutural, a equipe construiu uma ferramenta de IA chamada RBD-AIM. Primeiro, um modelo de linguagem treinado especificamente em sequências de anticorpos analisa o código genético das cadeias pesada e leve de um anticorpo e prevê a qual classe de epítopo ele pertence. Em seguida, uma etapa de predição estrutural usa modelos 3D conhecidos e algoritmos modernos de dobramento para refinar como esse anticorpo provavelmente se posiciona no RBD. Uma pontuação de confiança derivada do alinhamento 3D previsto ajuda a decidir quando confiar no modelo estrutural versus no classificador mais simples baseado em sequência. No geral, essa abordagem combinada supera buscas tradicionais por homologia e vários preditores estruturais de ponta ao adivinhar onde um anticorpo se liga e quão bem ele provavelmente bloqueará o vírus.
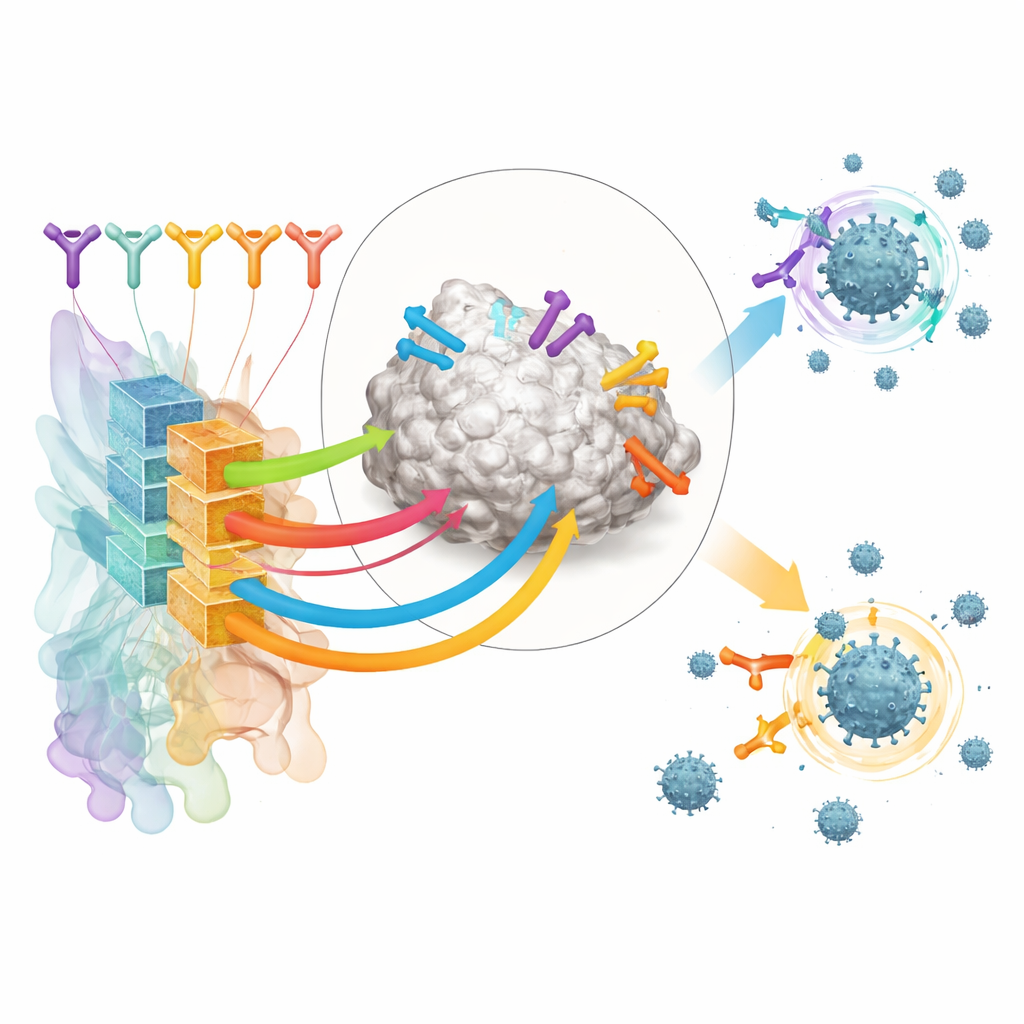
Recriando respostas imunes reais no laboratório
Para testar o RBD-AIM em coleções realistas de anticorpos, os pesquisadores reconstruíram repertórios nativos de células B de pessoas vacinadas com uma vacina de mRNA (Pfizer–BioNTech) ou com uma vacina de vetor adenoviral (Sputnik V). Usando microfluídica de gotículas, capturaram o pareamento original das cadeias pesada e leve de anticorpos de células B únicas e exibiram os fragmentos resultantes na superfície de células de levedura. Isso preservou a diversidade natural de anticorpos muito melhor do que métodos convencionais que misturam cadeias ao acaso. O RBD marcado por fluorescência permitiu separar as células de levedura que exibiam ligantes de RBD de alta afinidade, incluindo aqueles que competem diretamente com o receptor humano ACE2 pelo mesmo local na spike.
Prevendo e validando quais anticorpos realmente funcionam
Dúzias de anticorpos fortemente enriquecidos por ligação ao RBD desses doadores vacinados foram então analisados pelo RBD-AIM. A ferramenta previu qual classe de epítopo cada um reconhecia, se provavelmente bloqueava o ACE2 e quão robusto poderia ser frente a mutações na spike encontradas em variantes como Delta e Ômicron. Como esperado, anticorpos que miram a área de contato com o ACE2 tendiam a ser potentes, porém de escopo estreito, perdendo atividade contra Ômicron. Em contraste, um subconjunto de anticorpos de uma classe de epítopo mais distante (apelidada de E221 pelos autores) foi previsto para manter poder neutralizante através das variantes. Testes laboratoriais de ligação e neutralização viral confirmaram esses padrões, e estruturas cristalinas mostraram que as estimativas estruturais do RBD-AIM frequentemente eram precisas até as superfícies de contato detalhadas.
Da predição à proteção em animais
Para verificar se esses anticorpos priorizados pela IA podiam agir como medicamentos reais, a equipe selecionou moléculas representativas: um anticorpo clássico que bloqueia ACE2 e um anticorpo da classe E221 que neutraliza por um mecanismo mais indireto. Em um modelo letal de desafio por SARS-CoV-2 em camundongos geneticamente modificados para expressar ACE2 humano, uma única dose baixa de qualquer um dos anticorpos protegeu todos os animais tratados, em concordância com seus perfis de neutralização previstos. Trabalho estrutural e de simulação adicional sugeriu que o anticorpo da classe E221, de ampla atividade, atua “congelando” partes flexíveis do RBD necessárias para o engajamento eficiente do receptor, um mecanismo menos vulnerável à forma exata da região de contato com o ACE2.
O que isso significa para pandemias futuras
Em termos práticos, este estudo entrega um roteiro funcional para combinar tecnologias de exibição em alta vazão com IA para transformar dados brutos de sequência de anticorpos em compreensão funcional. Em vez de caracterizar minuciosamente um anticorpo de cada vez, os pesquisadores podem agora vasculhar rapidamente repertórios inteiros, classificar candidatos promissores por potência e amplitude e entender quais regiões de uma proteína viral são mais importantes de visar. Embora o RBD-AIM tenha sido treinado no SARS-CoV-2, os autores mostram que, com dados estruturais e mutacionais suficientes, a mesma estratégia pode se estender a outros vírus, apontando para um futuro em que o “perfilamento do panorama estrutural” guiado por IA nos ajude a minerar nossas próprias respostas imunes em busca de terapias de anticorpos de próxima geração.
Citação: Terekhov, S.S., Ivanisenko, N.V., Zhang, N. et al. Mining antibody functionality via AI-guided structural landscape profiling. Nat Commun 17, 4009 (2026). https://doi.org/10.1038/s41467-026-70553-6
Palavras-chave: descoberta de anticorpos, inteligência artificial, spike do SARS-CoV-2, mapeamento de epítopos, anticorpos terapêuticos