Clear Sky Science · fr
Exploiter la fonctionnalité des anticorps via un profilage du paysage structural guidé par l’IA
Pourquoi cette recherche compte
Les vaccins et les médicaments à base d’anticorps ont été des armes majeures contre la COVID-19, mais nos systèmes immunitaires produisent une diversité d’anticorps presque inimaginable, dont la plupart ne sont jamais étudiés en détail. Cet article montre comment l’intelligence artificielle peut lire les séquences génétiques d’anticorps et déduire où et comment ils s’accrochent à la spicule du coronavirus, aidant les chercheurs à repérer rapidement les molécules rares qui neutralisent le virus tout en restant actives face à ses mutations. La même stratégie pourrait accélérer la recherche d’antibiothérapies par anticorps contre de nombreux agents pathogènes futurs.
Transformer des séquences d’anticorps en carte
Les auteurs se concentrent sur les anticorps reconnaissant le domaine de liaison au récepteur (RBD) de la protéine spicule du SARS-CoV-2, une poignée clé que le virus utilise pour saisir les cellules humaines. Ils ont constitué un large jeu d’entraînement à partir de structures publiques de complexes anticorps–RBD et d’expériences de criblage mutagène profond qui cartographient comment les changements viraux affectent la liaison des anticorps. En clusterisant ces données, ils ont défini 12 « classes d’épitopes » distinctes — des régions récurrentes du RBD ciblées par différents anticorps, chacune associée à des caractéristiques typiques de puissance et d’étendue de neutralisation du virus.
Construire un guide IA de la fonction des anticorps
Par-dessus cette carte structurelle, l’équipe a développé un outil d’IA nommé RBD‑AIM. D’abord, un modèle de langage entraîné spécifiquement sur des séquences d’anticorps analyse le code génétique des chaînes lourdes et légères d’un anticorps et prédit à quelle classe d’épitope il appartient. Ensuite, une étape de prédiction structurelle utilise des modèles 3D connus et des algorithmes modernes de repliement pour affiner la position probable de cet anticorps sur le RBD. Un score de confiance dérivé de l’alignement 3D prédit aide à décider quand faire confiance au modèle structurel plutôt qu’au classifieur basé sur la séquence. Dans l’ensemble, cette approche combinée surpasse les recherches d’homologie traditionnelles et plusieurs prédicteurs structurels de pointe pour estimer où un anticorps se fixe et dans quelle mesure il bloque vraisemblablement le virus.
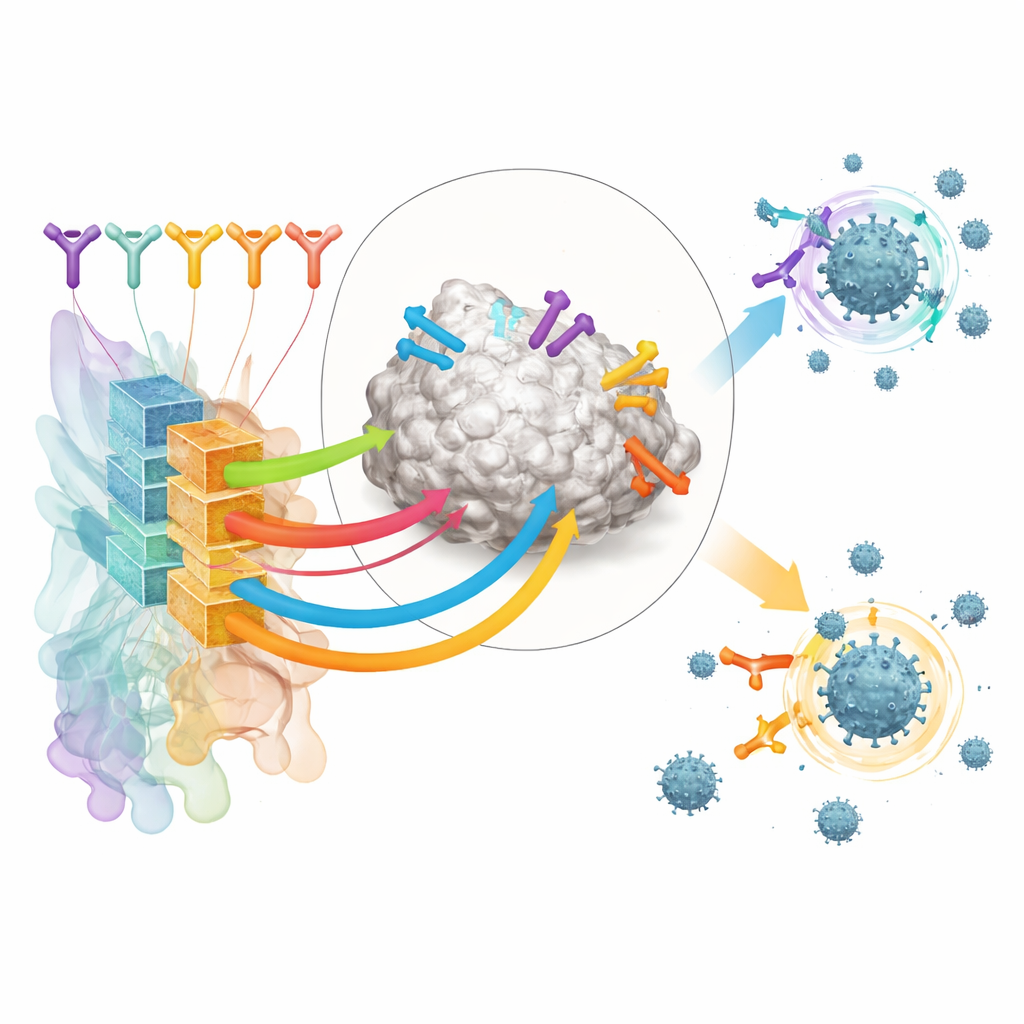
Recréer des réponses immunitaires réelles en laboratoire
Pour tester RBD‑AIM sur des collections d’anticorps réalistes, les chercheurs ont reconstitué des répertoires natifs de cellules B chez des personnes vaccinées soit par un vaccin à ARNm (Pfizer–BioNTech), soit par un vecteur adénoviral (Sputnik V). Grâce à la microfluidique en gouttelettes, ils ont capturé les appariements originaux des chaînes lourdes et légères d’anticorps provenant de cellules B individuelles et affiché les fragments obtenus à la surface de levures. Cela a préservé la diversité naturelle des anticorps bien mieux que les méthodes conventionnelles qui mélangent les chaînes au hasard. Un RBD marqué par fluorescence leur a permis de trier les levures portant des liaisons RBD à haute affinité, y compris celles qui concurrencent directement le récepteur humain ACE2 pour la même zone sur la spicule.
Prédire et valider quels anticorps fonctionnent réellement
Des dizaines d’anticorps fortement enrichis pour la liaison au RBD issus de ces donneurs vaccinés ont ensuite été analysés par RBD‑AIM. L’outil a prédit la classe d’épitope reconnue par chacun, s’il bloquait probablement ACE2, et à quel point il pourrait résister aux mutations de la spicule observées dans des variants comme Delta et Omicron. Comme prévu, les anticorps ciblant la zone de contact avec ACE2 avaient tendance à être puissants mais étroits, perdant de l’activité contre Omicron. En revanche, un sous-ensemble d’anticorps d’une classe d’épitope située plus à distance (nommée E221 par les auteurs) était prédit comme conservant un pouvoir neutralisant à travers les variants. Des tests de liaison et de neutralisation virale en laboratoire ont confirmé ces tendances, et des structures cristallographiques ont montré que les prédictions structurelles de RBD‑AIM étaient souvent exactes jusque dans les surfaces de contact détaillées.
De la prédiction à la protection chez l’animal
Pour vérifier si ces anticorps priorisés par l’IA pouvaient servir de vrais médicaments, l’équipe a sélectionné des molécules représentatives : un anticorps classique bloquant ACE2 et un anticorps de la classe E221 neutralisant par un mécanisme plus indirect. Dans un modèle létal d’infection par SARS‑CoV‑2 chez des souris modifiées pour exprimer l’ACE2 humain, une seule faible dose de l’un ou l’autre anticorps a protégé tous les animaux traités, conforme à leurs profils de neutralisation prédits. Des travaux structurels et de simulation supplémentaires ont suggéré que l’anticorps de la classe E221, d’activité large, agit en « gelant » des parties flexibles du RBD nécessaires à l’engagement efficace du récepteur, un mécanisme moins vulnérable à la forme exacte de la zone de contact ACE2.
Ce que cela signifie pour les pandémies futures
En termes pratiques, cette étude fournit une feuille de route opérationnelle pour combiner des technologies d’affichage à haut débit et l’IA afin de transformer des données brutes de séquences d’anticorps en informations fonctionnelles. Plutôt que de caractériser laborieusement un anticorps à la fois, les chercheurs peuvent désormais scanner rapidement des répertoires entiers, classer les candidats prometteurs par puissance et étendue, et comprendre quelles régions d’une protéine virale sont les plus importantes à cibler. Bien que RBD‑AIM ait été entraîné sur le SARS‑CoV‑2, les auteurs montrent qu’avec des données structurelles et mutationnelles suffisantes, la même stratégie peut s’étendre à d’autres virus, ouvrant la voie à un avenir où le « profilage du paysage structural » guidé par l’IA nous aide à exploiter nos propres réponses immunitaires pour développer des thérapies par anticorps de nouvelle génération.
Citation: Terekhov, S.S., Ivanisenko, N.V., Zhang, N. et al. Mining antibody functionality via AI-guided structural landscape profiling. Nat Commun 17, 4009 (2026). https://doi.org/10.1038/s41467-026-70553-6
Mots-clés: découverte d’anticorps, intelligence artificielle, spicule SARS-CoV-2, cartographie d’épitope, anticorps thérapeutiques