Clear Sky Science · es
Explotando la funcionalidad de los anticuerpos mediante perfilado del paisaje estructural guiado por IA
Por qué importa esta investigación
Las vacunas y los medicamentos basados en anticuerpos han sido armas clave contra la COVID-19, pero nuestros sistemas inmunitarios generan una variedad de anticuerpos casi inimaginablemente grande, la mayoría de los cuales nunca estudiamos en detalle. Este artículo muestra cómo la inteligencia artificial puede leer las secuencias genéticas de los anticuerpos e inferir dónde y cómo se adhieren a la proteína spike del coronavirus, ayudando a los científicos a seleccionar rápidamente las moléculas raras que neutralizan el virus y permanecen activas frente a sus mutaciones. Esa misma estrategia podría acelerar la búsqueda de medicamentos con anticuerpos contra muchos patógenos futuros.
Transformar secuencias de anticuerpos en un mapa
Los autores se centran en anticuerpos que reconocen el dominio de unión al receptor (RBD) de la proteína spike de SARS-CoV-2, un punto de agarre clave que el virus usa para captar las células humanas. Reunieron un gran conjunto de entrenamiento a partir de estructuras públicas de complejos anticuerpo–RBD y de experimentos de escaneo mutacional profundo que cartografían cómo las variaciones del virus afectan la unión de anticuerpos. Mediante el agrupamiento de estos datos, definieron 12 “clases de epítopo” distintas: regiones recurrentes en el RBD que atacan diferentes anticuerpos, cada una asociada a características típicas de potencia y amplitud de neutralización viral.
Construir una guía de IA para la función de anticuerpos
Sobre este mapa estructural, el equipo construyó una herramienta de IA llamada RBD-AIM. Primero, un modelo de lenguaje entrenado específicamente con secuencias de anticuerpos analiza el código genético de las cadenas pesadas y ligeras de un anticuerpo y predice a qué clase de epítopo pertenece. Después, un paso de predicción estructural emplea plantillas 3D conocidas y algoritmos modernos de plegamiento para refinar cómo es probable que ese anticuerpo se coloque sobre el RBD. Una puntuación de confianza derivada del alineamiento 3D predicho ayuda a decidir cuándo confiar en el modelo estructural frente al clasificador más simple basado en secuencia. En conjunto, este enfoque combinado supera a las búsquedas tradicionales por homología y a varios predictores de estructura de última generación al estimar dónde se une un anticuerpo y cuán probable es que bloquee el virus.
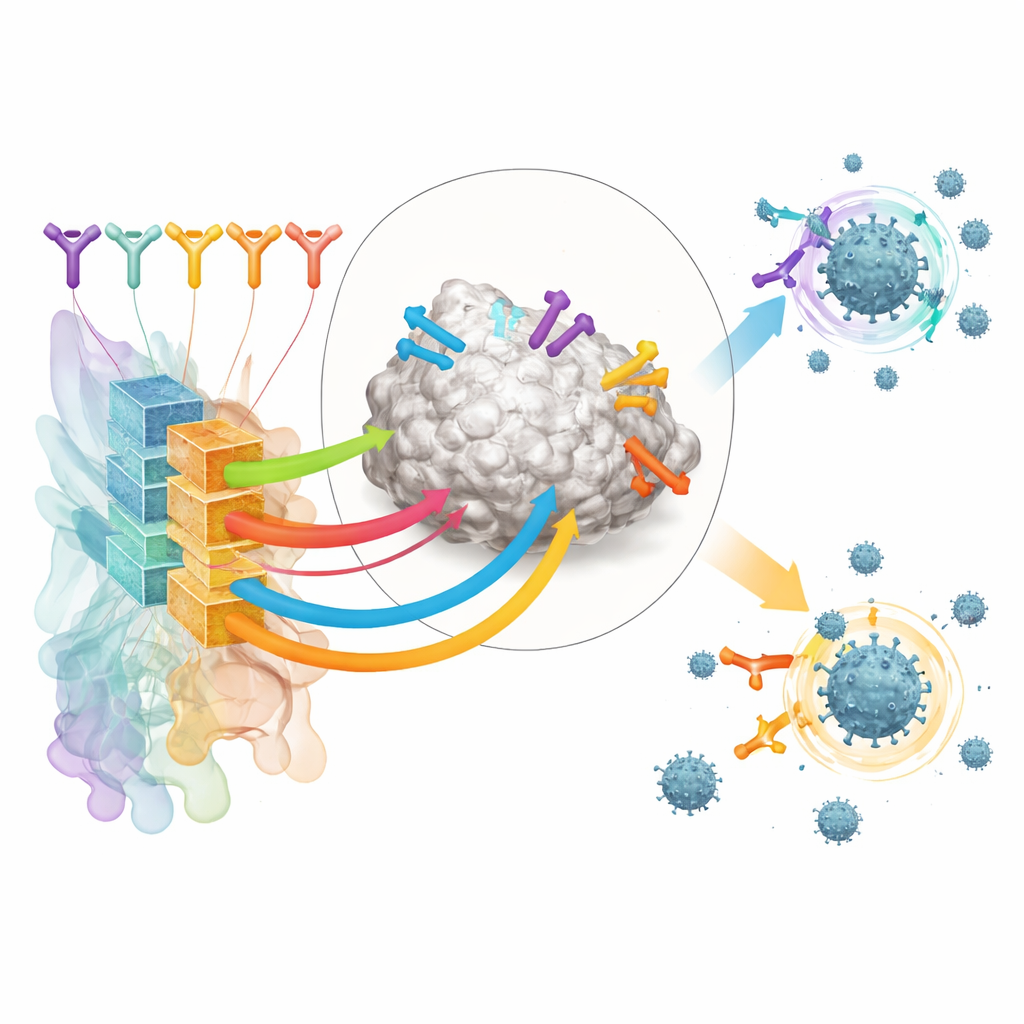
Recrear respuestas inmunitarias reales en el laboratorio
Para probar RBD-AIM con colecciones de anticuerpos realistas, los investigadores reconstruyeron repertorios nativos de células B de personas vacunadas con una vacuna de ARNm (Pfizer–BioNTech) o con una vacuna de vector adenoviral (Sputnik V). Usando microfluidos en gotas, capturaron el apareamiento original de las cadenas pesada y ligera de anticuerpos de células B individuales y mostraron los fragmentos resultantes en la superficie de levaduras. Esto preservó la diversidad natural de los anticuerpos mucho mejor que los métodos convencionales que mezclan las cadenas al azar. Un RBD marcado con fluorescencia les permitió separar las levaduras que exponían ligandos RBD de alta afinidad, incluidos aquellos que compiten directamente con el receptor humano ACE2 por la misma zona del spike.
Predecir y validar qué anticuerpos funcionan realmente
Docenas de anticuerpos con fuerte enriquecimiento en unión al RBD de estos donantes vacunados se sometieron entonces a RBD-AIM. La herramienta predijo a qué clase de epítopo reconocía cada uno, si probablemente bloqueaba ACE2 y cuán robusto podría ser frente a mutaciones del spike presentes en variantes como Delta y Omicron. Como era de esperar, los anticuerpos dirigidos al área de contacto con ACE2 tendían a ser potentes pero de alcance estrecho, perdiendo actividad frente a Omicron. En contraste, un subconjunto de anticuerpos de una clase de epítopo más distante (denominada E221 por los autores) se pronosticó que conservaría poder neutralizante a través de variantes. Pruebas de unión y neutralización viral en laboratorio confirmaron estos patrones, y estructuras cristalinas mostraron que las predicciones estructurales de RBD-AIM eran con frecuencia precisas hasta las superficies de contacto detalladas.
De la predicción a la protección en animales
Para comprobar si estos anticuerpos priorizados por la IA podían actuar como medicamentos reales, el equipo seleccionó moléculas representativas: un anticuerpo clásico que bloquea ACE2 y un anticuerpo de la clase E221 que neutraliza mediante un mecanismo más indirecto. En un modelo letal de desafío con SARS-CoV-2 en ratones modificados para expresar ACE2 humano, una única dosis baja de cualquiera de los dos anticuerpos protegió a todos los animales tratados, en consonancia con sus perfiles de neutralización predichos. Trabajos estructurales y de simulación adicionales sugirieron que el anticuerpo de la clase E221, de amplio espectro, actúa “congelando” partes flexibles del RBD necesarias para un acoplamiento eficiente al receptor, un mecanismo menos vulnerable a la forma exacta del parche de contacto con ACE2.
Qué significa esto para futuras pandemias
En términos prácticos, este estudio ofrece un plan operativo para combinar tecnologías de visualización de alto rendimiento con IA y convertir datos de secuencia cruda de anticuerpos en información funcional. En lugar de caracterizar laboriosamente un anticuerpo a la vez, los investigadores pueden ahora escanear rápidamente repertorios enteros, clasificar candidatos prometedores por potencia y amplitud, y comprender qué regiones de una proteína viral son más importantes de atacar. Aunque RBD-AIM se entrenó con SARS-CoV-2, los autores muestran que con suficientes datos estructurales y mutacionales la misma estrategia puede extenderse a otros virus, apuntando hacia un futuro en el que el “perfilado del paisaje estructural” guiado por IA nos ayude a explotar nuestras propias respuestas inmunitarias para desarrollar terapias de anticuerpos de próxima generación.
Cita: Terekhov, S.S., Ivanisenko, N.V., Zhang, N. et al. Mining antibody functionality via AI-guided structural landscape profiling. Nat Commun 17, 4009 (2026). https://doi.org/10.1038/s41467-026-70553-6
Palabras clave: descubrimiento de anticuerpos, inteligencia artificial, spike de SARS-CoV-2, mapeo de epítopos, anticuerpos terapéuticos