Clear Sky Science · sv
Utforska antikroppsfunktion via AI-styrd kartläggning av den strukturella landskapen
Varför denna forskning är viktig
Vacciner och antikroppsbaserade läkemedel har varit centrala vapen mot COVID-19, men vårt immunsystem skapar en nästan ofattbart stor variation av antikroppar, varav de flesta aldrig studeras i detalj. Denna artikel visar hur artificiell intelligens kan läsa antikroppars genetiska sekvenser och härleda var och hur de fäster vid koronavirusets spike, vilket hjälper forskare att snabbt plocka ut de sällsynta molekyler som både neutraliserar viruset och behåller aktiviteten när det muterar. Samma strategi skulle kunna påskynda sökandet efter antikroppsläkemedel mot många framtida patogener.
Att omvandla antikroppssekvenser till en karta
Författarna fokuserar på antikroppar som känner igen receptorbindande domänen (RBD) av SARS-CoV-2:s spikeprotein, ett viktigt grepp viruset använder för att få fäste vid människoceller. De sammanställde ett stort träningsset från offentligt tillgängliga strukturer av antikropp–RBD-komplex och från deep mutational scanning-experiment som kartlägger hur förändringar i viruset påverkar antikroppsfäste. Genom att klustra dessa data definierade de 12 distinkta ”epitopklasser” – återkommande regioner på RBD som olika antikroppar riktar sig mot, vardera associerad med karakteristisk styrka och bredd i virusneutralisering.
Bygga en AI-vägvisare för antikroppsfunktion
Ovanpå denna strukturella karta byggde teamet ett AI-verktyg kallat RBD-AIM. Först analyserar en språkmodell som är särskilt tränad på antikroppssekvenser den genetiska koden för en antikropps tunga och lätta kedjor och förutspår vilken epitopklass den tillhör. Därefter använder ett struktur-prediktionssteg kända 3D-mallar och moderna foldningsalgoritmer för att förfina hur den antikroppen sannolikt sitter på RBD. En konfidenspoäng härledd från den förutsagda 3D-justeringen hjälper till att avgöra när man ska lita på den strukturella modellen kontra den enklare sekvensbaserade klassificeraren. Sammantaget överträffar detta kombinerade angreppssätt traditionella homologisökningar och flera toppmoderna strukturprediktorer när det gäller att gissa var en antikropp binder och hur väl den sannolikt blockerar viruset.
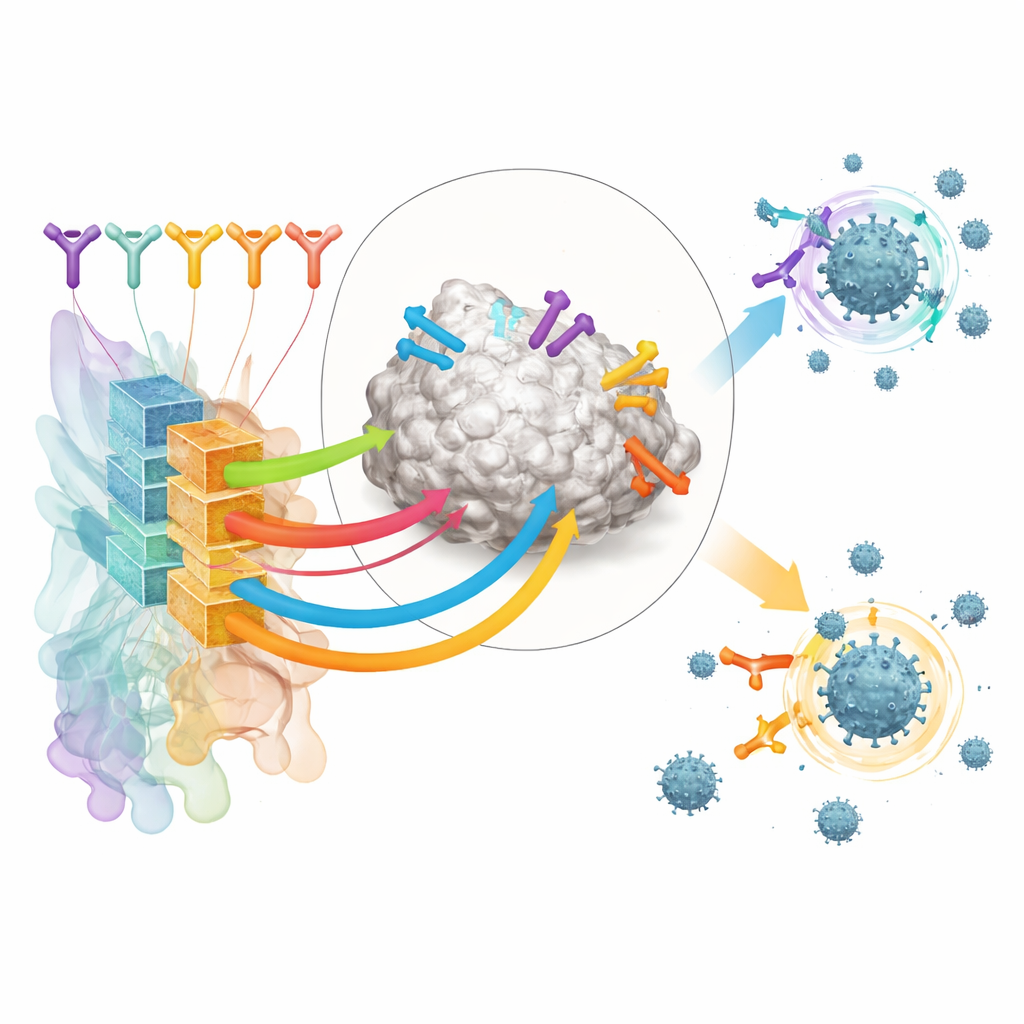
Återskapa verkliga immunsvar i laboratoriet
För att testa RBD-AIM på realistiska antikroppsuppsättningar rekonstruerade forskarna naturna B-cellsrepertoarer från personer som vaccinerats med antingen ett mRNA-vaccin (Pfizer–BioNTech) eller ett adenoviral vektorvaccin (Sputnik V). Med droppmikrofluidik fångade de de ursprungliga parningarna av tunga och lätta antikroppskedjor från enskilda B-celler och visade de resulterande fragmenten på ytan av jästceller. Detta bevarade antikropparnas naturliga mångfald betydligt bättre än konventionella metoder som slumpmässigt blandar kedjor. Fluorescerande märkt RBD gjorde det möjligt att sortera ut jästceller som bar högaffinitets-RBD-bindare, inklusive sådana som konkurrerar direkt med den mänskliga ACE2-receptorn om samma yta på spiken.
Förutsäga och validera vilka antikroppar som verkligen fungerar
Flera dussin starkt berikade RBD-bindande antikroppar från dessa vaccinerade donatorer kördes sedan genom RBD-AIM. Verktyget förutspådde vilken epitopklass var och en kände igen, om de sannolikt blockerade ACE2, och hur robusta de skulle kunna vara mot spikmutationer som återfinns i varianter som Delta och Omicron. Som väntat tenderade antikroppar som riktar sig mot ACE2-kontaktytan att vara potenta men snäva i räckvidd och förlora aktivitet mot Omicron. I kontrast förutspåddes en undergrupp antikroppar från en mer avlägsen epitopklass (döpt E221 av författarna) behålla neutraliserande förmåga över varianter. Laboratorietester av bindning och virusneutralisering bekräftade dessa mönster, och kristallstrukturer visade att RBD-AIM:s strukturella gissningar ofta var korrekta ner på detaljerade kontaktytor.
Från förutsägelse till skydd i djur
För att se om dessa AI-prioriterade antikroppar kunde fungera som verkliga läkemedel valde teamet representativa molekyler: en klassisk ACE2-blockerande antikropp och en E221-klassantkropp som neutraliserar via en mer indirekt mekanism. I en dödlig SARS-CoV-2-utmaningsmodell med möss som modifierats att uttrycka mänsklig ACE2 skyddade en enda låg dos av båda antikropparna alla behandlade djur, i linje med deras förutsagda neutraliseringsprofiler. Ytterligare strukturellt och simuleringsarbete antydde att den bredaktivt E221-klassade antikroppen verkar genom att ”frysa” flexibla delar av RBD som behövs för effektiv receptorbindning, en mekanism som är mindre sårbar för den exakta formen av ACE2-kontaktytan.
Vad detta betyder för framtida pandemier
I praktiska termer levererar denna studie en fungerande blåkopi för att kombinera höggenomströmmande displayteknologier med AI för att förvandla rå antikroppssekvensdata till funktionell insikt. Istället för att mödosamt karaktärisera en antikropp i taget kan forskare nu snabbt skanna hela repertoarer, rangordna lovande kandidater efter potens och bredd, och förstå vilka regioner av ett virusprotein som är viktigast att rikta in sig mot. Även om RBD-AIM tränades på SARS-CoV-2 visar författarna att med tillräckliga strukturella och mutagena data kan samma strategi utsträckas till andra virus, och pekar mot en framtid där AI-styrd ”strukturell landskapsprofilering” hjälper oss att bryta nytta av våra egna immunsvar för nästa generations antikroppsterapier.
Citering: Terekhov, S.S., Ivanisenko, N.V., Zhang, N. et al. Mining antibody functionality via AI-guided structural landscape profiling. Nat Commun 17, 4009 (2026). https://doi.org/10.1038/s41467-026-70553-6
Nyckelord: antikroppsupptäckt, artificiell intelligens, SARS-CoV-2-spike, epitopkartläggning, terapeutiska antikroppar