Clear Sky Science · zh
mGlu6 的冷冻电镜结构捕捉到受体在与 G 蛋白偶联前的激活状态
我们的眼睛如何在黑暗中继续工作
在微光中看清事物依赖于视网膜内一个从不休眠的微小分子机器。这个机器是名为 mGlu6 的受体,位于杆状光感受器与将信号传递到大脑的神经细胞之间的连接处。mGlu6 功能失常会导致先天性恒定性夜盲——患者在弱光下无法正常看见,尽管眼睛外观通常正常。该研究揭示了 mGlu6 的近原子级三维结构,并解释了其运动如何实现夜视,以及遗传突变如何破坏这一过程。
视觉第一个突触处的繁忙守门人
在黑暗中,视网膜的杆细胞持续释放神经递质谷氨酸。表面上的 mGlu6 在 ON 双极细胞上接收这一信号,这些细胞充当杆驱动视觉的第一道中继。活化的 mGlu6 打开细胞内的开关——一种名为 Gαo 的 G 蛋白——该开关使离子通道(TRPM1)保持关闭状态,从而使双极细胞静默。当光照射到杆细胞时,谷氨酸释放瞬间降低,mGlu6 信号关闭,通道打开,双极细胞被激活,传递光的存在。由于该切换必须在一生中快速而持续地工作,mGlu6 的结构既需要稳定又要高度精密调节。
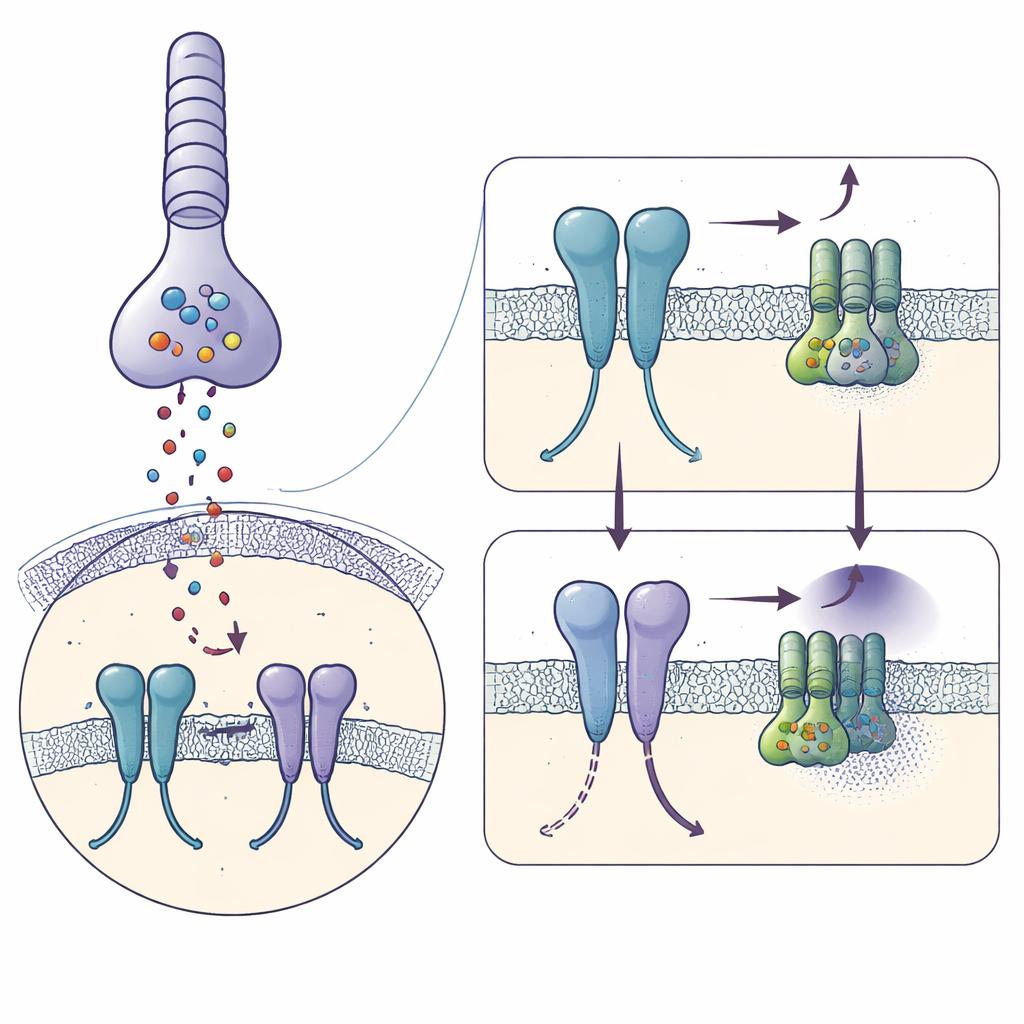
在受体发出信号前的捕捉
作者使用冷冻电子显微镜,将纯化的人源 mGlu6 与一种强效激动剂 L‑丝氨酸 O‑磷酸化合物一同速冻,并重建出 3.2 埃分辨率下的形态。每个 mGlu6 分子以二聚体形式存在,由三层堆叠的区域构成:位于细胞外的大“贝壳”夹层用于捕捉谷氨酸;富含二硫键的柔性中段;以及横跨膜的七螺旋束——G 蛋白结合位点。激动剂将外部结构夹持在一个闭合、类激活构象,并使中间段靠拢,同时膜内螺旋发生位移,使一对关键的 TM6 螺旋相互紧密接触——这些都是受体准备与 G 蛋白结合的特征。
内建的不对称:一侧先行,另一侧随动
一个显著发现是 mGlu6 二聚体的两半并未表现出完全相同的构象,尽管两侧都结合相同的激动剂。一个亚基弯曲更明显,其膜内螺旋稍微向细胞外升高,产生了两侧 TM6 螺旋会合处的不对称界面。这种构型与在相关受体中观察到的 G 蛋白结合态非常相似,表明 mGlu6 在一侧已处于“预准备”耦合的状态。对大量粒子图像的分析显示,二聚体取样的弯曲角度呈连续分布,从近乎对称到强烈不对称不等,暗示受体在不同构象间动态摆动,而且不对称性在 G 蛋白到来之前就已出现。
加速信号传导的隐藏支撑支架
研究还发现了中间富半胱氨酸区与膜外一段环之间的一种不同寻常的接触面。在 mGlu6 中,该环比相关受体更长,形成由盐桥、氢键和疏水相互作用组成的网络,将中段与膜区牢固连接。当该界面中的关键残基被突变时,受体仍能到达细胞表面并激活 G 蛋白,但其速度变慢,即便受体表达量充足。这提示这些额外的接触像机械支架一样,有效地将外部“贝壳”受谷氨酸诱导的运动传递到膜螺旋,从而实现实时视觉所需的快速反应。
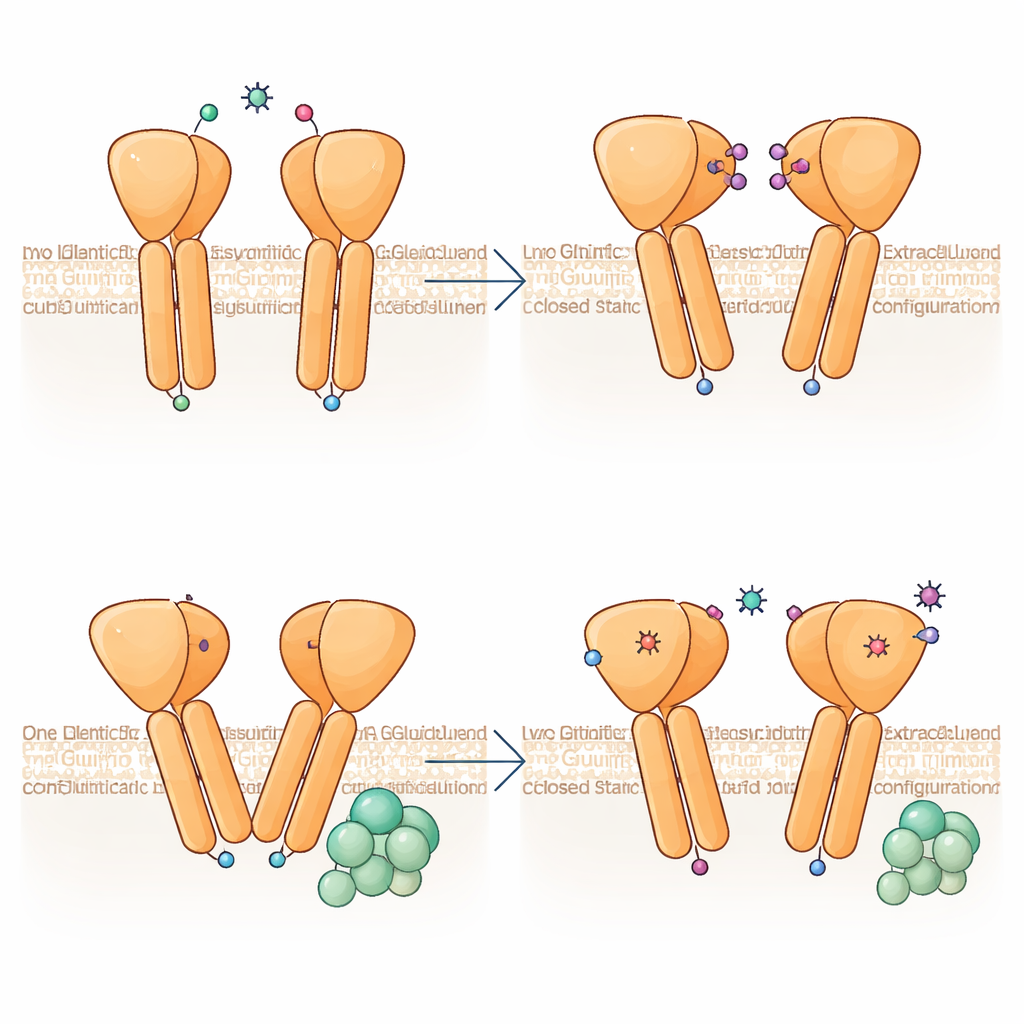
通过结构解释夜盲
作者将所有已知的先天性恒定性夜盲患者突变映射到新结构上,展示了多种改变如何削弱 mGlu6。部分突变扭曲了谷氨酸结合口袋或破坏了埋藏的疏水核心,致使外部结构不稳定;另一些则破坏维持中段与膜区连接的关键二硫键或盐桥,导致受体错误折叠、无法到达细胞表面。许多变体降低了 G 蛋白激活的效率或速度。有趣的是,两种突变在表达量标准化后实际上增强了信号传导能力,但仍可能导致疾病,因为这些受体运输不足或在突触处定位异常。总体而言,这些发现将具体的结构缺陷与受损信号传导联系起来,为理解并最终治疗遗传性夜视障碍提供了分子蓝图。
引用: Lee, S.Y., Chang, CT., Yun, Y. et al. CryoEM structure of mGlu6 captures receptor activation prior to G protein coupling. Nat Commun 17, 3681 (2026). https://doi.org/10.1038/s41467-026-70436-w
关键词: 夜盲, 视网膜信号传导, G 蛋白偶联受体, 代谢型谷氨酸受体, 冷冻电子显微镜