Clear Sky Science · tr
mGlu6'nın CryoEM yapısı, G proteini bağlanmasından önce reseptör aktivasyonunu yakalıyor
Gözlerimizin Karanlıkta Çalışmaya Devam Etmesini Sağlayan Mekanizma
Loş ışıkta görme, retina içinde hiçbir zaman uyumayan küçük bir moleküler makineye dayanır. Bu makine, mGlu6 adlı bir reseptör, rod fotoreseptörleri ile beyne sinyal ileten sinir hücreleri arasındaki kavşakta yer alır. mGlu6 işlevini yitirdiğinde insanlar doğuştan durağan gece körlüğü adı verilen bir durumla doğarlar—düşük ışıkta düzgün göremezler, oysa gözleri başka açıdan normal görünür. Bu çalışma, mGlu6'nın üç boyutlu yapısını atomlara yakın ayrıntıda ortaya koyuyor ve hareketinin gece görmesini nasıl mümkün kıldığını ve kalıtsal mutasyonların bu süreci nasıl bozduğunu açıklıyor.
Görmenin İlk Sinapsindeki Yoğun İşlek Kapı Bekçisi
Karanlıkta, retinadaki rod hücreleri sürekli olarak kimyasal haberci glutamat salar. Bu sinyal, rod kaynaklı görmenin ilk rölesi olarak görev yapan ON‑bipolar hücrelerin yüzeyindeki mGlu6 tarafından algılanır. Aktif mGlu6, hücre içinde Gαo adlı bir G proteininin açılmasını sağlayan bir anahtarı çalıştırır; bu, bir iyon kanalını (TRPM1) kapalı tutar ve böylece bipolar hücre sessiz kalır. Işık rodları vurduğunda, glutamat salımı aniden düşer, mGlu6 sinyali kapanır, kanal açılır ve bipolar hücre aktif hale gelerek ışığın varlığını duyurur. Bu geçişin hızla ve yaşam boyu sürekli olarak çalışması gerektiğinden, mGlu6 yapısının hem sağlam hem de son derece hassas ayarlanmış olması gerekir.
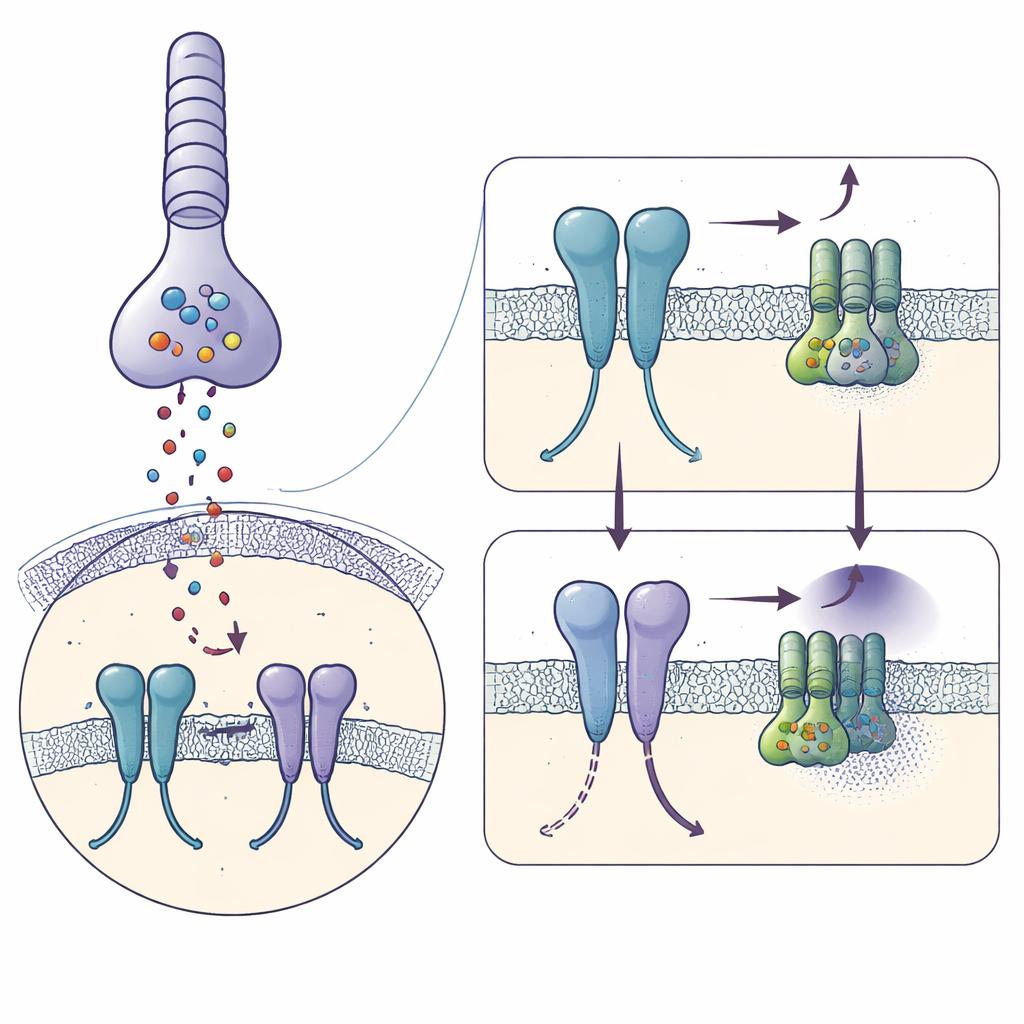
Reseptör Sinyal Vermeden Hemen Önceyi Yakalamak
Kriyoyalın elektron mikroskobisi kullanarak, yazarlar saflaştırılmış insan mGlu6'yı güçlü bir aktive edici olan L‑serin O‑fosfata bağlı halde dondurdular ve şeklini 3.2‑ångström çözünürlükte yeniden yapılandırdılar. Her mGlu6 molekülü, üç katmanlı bölgeden oluşan bir çift (dimer) oluşturur: glutamatı yakalayan hücre dışında büyük bir "midye kabuğu" (clamshell), disülfit bağlarca zengin esnek bir orta segment ve G proteinlerinin bağlandığı membranı geçen yedi heliksli bir demet. Aktivatör, dış bölgeleri kapalı, aktif benzeri bir duruma sıkıştırır ve orta segmentleri birbirine yaklaştırırken, membran heliksleri de öyle bir kayma gösterir ki anahtar bir heliks çifti (TM6) yakın temas kurar—G proteinine bağlanmaya hazır bir reseptörün ayırt edici özellikleri bunlardır.
İçsel Asimetri: Bir Partner Önde, Diğeri Ardından Geliyor
Çarpıcı bir keşif, mGlu6 dimerinin iki yarısının aynı şekli almadığıdır; her ikisi de aynı aktivatörü bağlasa bile. Bir altünite daha keskin biçimde bükülür ve membran heliksleri hücre dışına doğru biraz daha yükselir; bu da iki TM6 heliksinin buluştuğu asimetrik bir ara yüz oluşturur. Bu konfigürasyon, ilişkili reseptörlerde görülen G proteini bağlanmış duruma çok benzer; bu da mGlu6'nın bir tarafta bağlanmaya "ön‑hazır" olduğunu düşündürür. Çok sayıda partikül görüntüsünün analizleri, dimerin hemen hemen simetrik olandan güçlü asimetrik olana kadar bir bükülme açısı continuum'u örneklediğini gösterir; bu da reseptörün durumlar arasında dinamik olarak sallandığını ve asimetrinin G proteini gelmeden önce bile ortaya çıktığını ima eder.
Sinyali Hızlandıran Gizli Bir Destek İskeleti
Araştırma ayrıca orta sistein‑zengin bölge ile membranın dış tarafındaki bir döngü arasında alışılmadık bir temas yüzeyini ortaya çıkarır. mGlu6'da bu döngü, ilişkili reseptörlerden daha uzundur ve orta ile membran bölgelerini birbirine kilitleyen bir tuz köprüleri, hidrojen bağları ve hidrofobik temas ağı oluşturur. Bu arayüzdeki kritik kalıntılar değiştirildiğinde, reseptör hâlâ hücre yüzeyine ulaşır ve G proteinlerini aktive edebilir, ancak bol miktarda reseptör olsa bile bunu daha yavaş yapar. Bu bulgu, fazladan temasların dış "midye kabuğu"nun glutamat kaynaklı hareketini membran helikslerine verimli biçimde ileten mekanik bir takoz işlevi gördüğünü ve gerçek zamanlı görme için gereken hızlı yanıtları mümkün kıldığını gösterir.
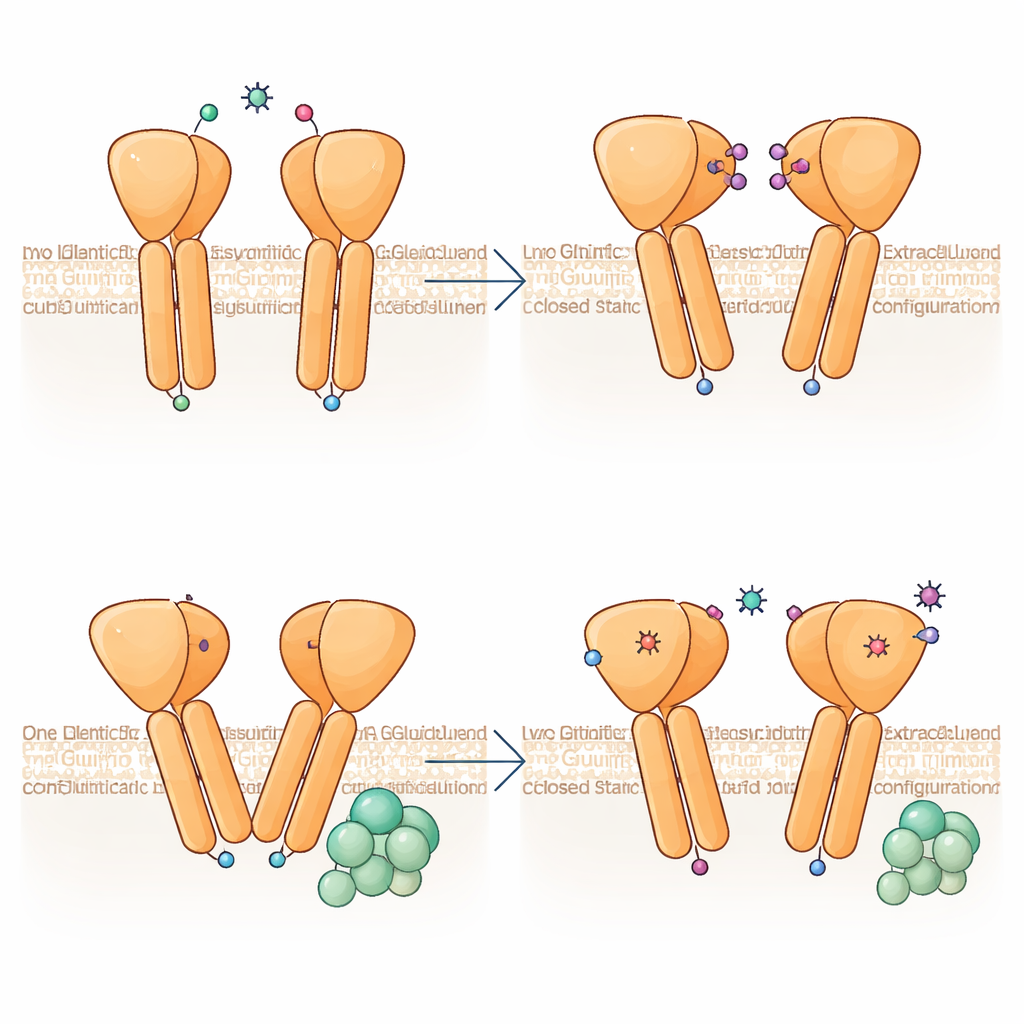
Yapı Üzerinden Gece Körlüğünü Açıklamak
Doğuştan durağan gece körlüğü için bilinen her hasta mutasyonunu yeni yapıya eşleyerek yazarlar, çeşitli değişikliklerin mGlu6'yı nasıl sakat bırakabileceğini gösteriyor. Bazı mutasyonlar glutamat bağlama ceplerini bozar veya gömülü hidrofobik çekirdekleri dağıtarak dış alanı kararsızlaştırır; diğerleri ise orta ve membran bölgelerini bir arada tutan kritik disülfit bağlarını veya tuz köprülerini kırar, bunun sonucunda reseptör hatalı katlanır ve hücre yüzeyine ulaşamaz. Birçok varyant, G proteini aktivasyonunun verimliliğini veya hızını azaltır. İlginç bir şekilde, iki mutasyon ifadenin normalize edilmesinin ardından aslında sinyal kapasitesini artırıyor gibi görünür, ancak muhtemelen reseptörlerin kötü trafikte olması veya sinapslarda yanlış konumlanması nedeniyle yine de hastalığa yol açarlar. Birlikte bu bulgular, belirli yapısal kusurları bozulmuş sinyallemeye bağlayarak kalıtsal gece görüş bozukluklarını anlamak ve nihayetinde tedavi etmek için moleküler bir yol haritası sunar.
Atıf: Lee, S.Y., Chang, CT., Yun, Y. et al. CryoEM structure of mGlu6 captures receptor activation prior to G protein coupling. Nat Commun 17, 3681 (2026). https://doi.org/10.1038/s41467-026-70436-w
Anahtar kelimeler: gece körlüğü, retinal sinyal iletimi, G proteini–bağlı reseptörler, metabotropik glutamat reseptörü, kriyoyalın elektron mikroskobu