Clear Sky Science · ru
Крио-ЭМ структура mGlu6 фиксирует активацию рецептора перед связыванием с G-белком
Как наши глаза продолжают работать в темноте
Видение при слабом освещении зависит от крошечного молекулярного механизма в сетчатке, который никогда не спит. Эта машина — рецептор под названием mGlu6 — расположена на стыке между палочками и нервными клетками, передающими сигналы в мозг. При нарушении функции mGlu6 люди рождаются с состоянием, известным как врождённая неподвижная ночная слепота: они плохо видят в условиях низкой освещённости, хотя внешне глаза выглядят нормально. В этом исследовании показана трёхмерная структура mGlu6 с близкой к атомной детализацией и объяснено, как движение рецептора обеспечивает ночное зрение и как наследственные мутации нарушают этот процесс.
Занятый сторож на первом синапсе зрительной системы
В темноте палочки сетчатки постоянно выделяют химический посредник — глутамат. Этот сигнал улавливает mGlu6 на поверхности ON‑биполярных клеток, которые выступают первым звеном для зрительных сигналов от палочек. Активный mGlu6 включает внутренний переключатель — G‑белок Gαo — который удерживает ионный канал (TRPM1) в закрытом состоянии, так что биполярная клетка остаётся тихой. Когда свет попадает на палочки, выделение глутамата резко снижается, сигнал от mGlu6 выключается, канал открывается, и биполярная клетка активируется, сообщая о наличии света. Поскольку этот переключатель должен работать быстро и непрерывно в течение всей жизни, структура mGlu6 должна быть одновременно стабильной и тонко настроенной.
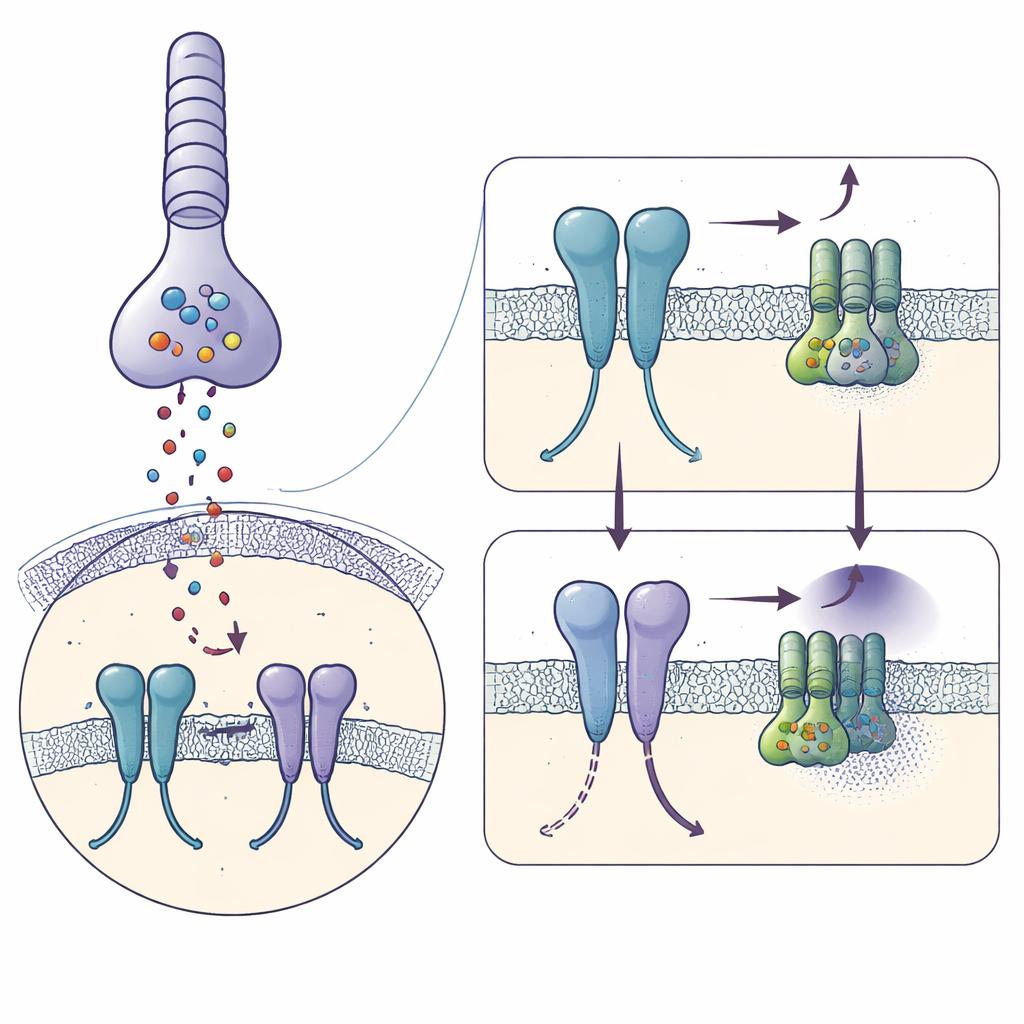
Поймать рецептор непосредственно перед сигнализацией
С помощью криоэлектронной микроскопии авторы заморозили очищенный человеческий mGlu6, связанный с сильным активатором L‑серином O‑фосфатом, и восстановили его форму с разрешением 3,2 ангстрёма. Каждая молекула mGlu6 образует пару, или димер, состоящий из трёх наслаивающихся областей: большой «раковиноподобной» внешней части вне клетки, улавливающей глутамат; гибкого среднего сегмента, богатого дисульфидными связями; и семи спирального пучка, проходящего через мембрану, где связываются G‑белки. Активатор зажимает внешние домены в закрытой, похожей на активную, конформации и сближает средние сегменты, в то время как мембранные спирали смещаются так, что ключевая пара спиралей (называемая TM6) оказывается в тесном контакте — признаки рецептора, готового взаимодействовать с G‑белком.
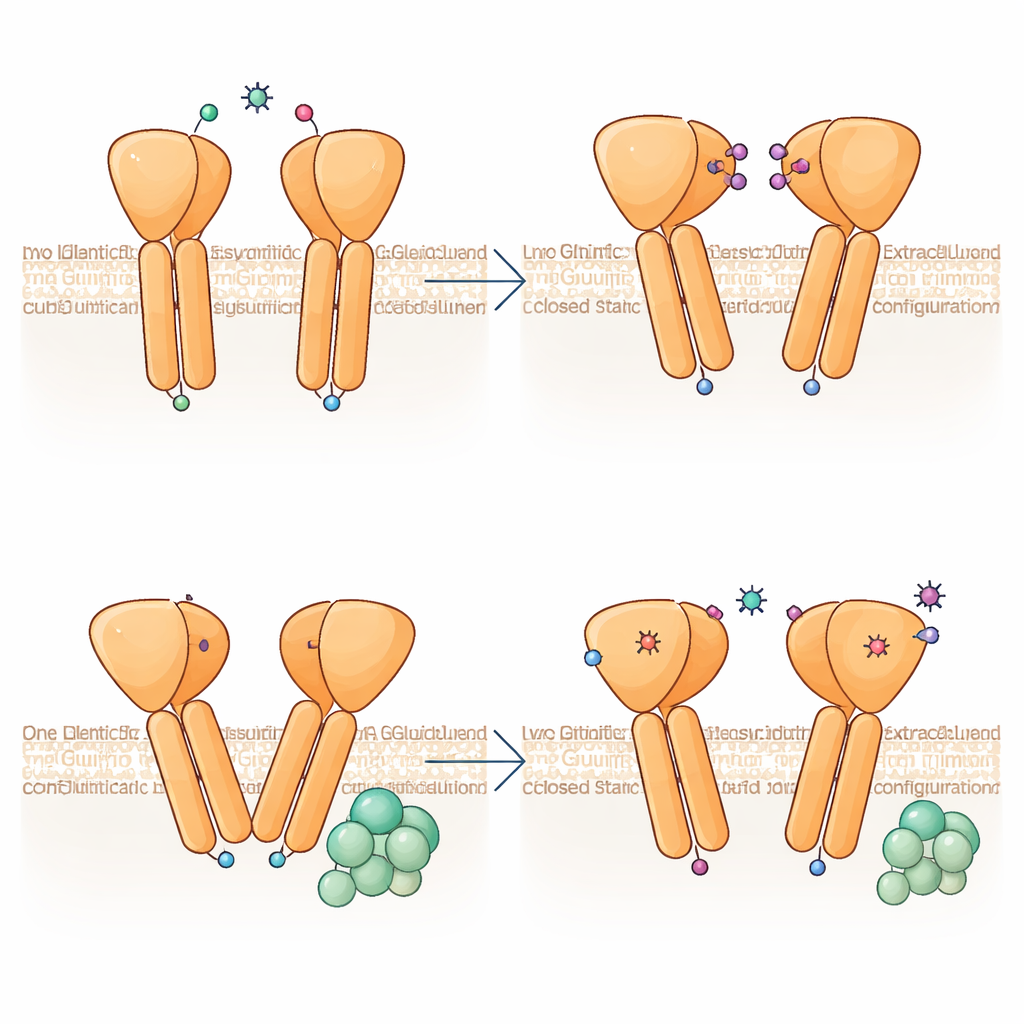
Встроенная асимметрия: один партнёр ведёт, другой следует
Поразительное открытие заключается в том, что две половины димера mGlu6 не принимают идентичные формы, хотя обе связывают один и тот же активатор. Одна субъединица изгибается сильнее, и её мембранные спирали поднимаются чуть выше к внешней стороне клетки, создавая асимметричный интерфейс там, где сходятся две TM6. Эта конфигурация сильно напоминает состояние связывания с G‑белком, наблюдаемое у родственных рецепторов, что наводит на мысль, что mGlu6 «предварительно подготовлен» к сопряжению на одной стороне. Анализ множества частиц показывает, что димер проходит через континуум углов изгиба — от почти симметричного до сильно асимметричного, — что подразумевает динамическое качание рецептора между состояниями и появление асимметрии ещё до прихода G‑белка.
Скрытый опорный каркас, ускоряющий передачу сигнала
Работа также выявляет необычную контактную поверхность между средней богатой цистеином областью и петлёй с внешней стороны мембраны. У mGlu6 эта петля длиннее, чем у родственных рецепторов, и образует сеть ионных мостов, водородных связей и гидрофобных контактов, которая фиксирует среднюю и мембранную области вместе. При замене ключевых остатков в этом интерфейсе рецептор всё ещё достигает поверхности клетки и способен активировать G‑белки, но делает это медленнее, даже если рецепторов достаточно. Это указывает на то, что дополнительные контакты действуют как механическое подкрепление, эффективно передающее движение внешней «раковины», вызванное глутаматом, вниз к мембранным спиралям, обеспечивая быстрые ответы, необходимые для своевременного зрения.
Объяснение ночной слепоты через структуру
Нанесши все известные мутации пациентов с врождённой неподвижной ночной слепотой на новую структуру, авторы показывают, как разнообразные изменения могут выводить mGlu6 из строя. Некоторые мутации деформируют карман связывания глутамата или разрушают погружённые гидрофобные ядра, дестабилизируя внешнюю область; другие разрывают критические дисульфидные связи или ионные мосты, удерживающие вместе средние и мембранные участки, что приводит к неправильной сворачиваемости рецептора и его неспособности достигнуть поверхности клетки. Многие варианты уменьшают эффективность или скорость активации G‑белка. Любопытно, что две мутации действительно усиливают сигнальную способность при нормализованном экспрессии, но всё равно, вероятно, вызывают заболевание, поскольку рецепторы плохо транспортируются или неправильно локализуются на синапсах. В целом эти данные связывают конкретные структурные дефекты с нарушением передачи сигналов, предлагая молекулярную схему для понимания и, в перспективе, лечения наследственных нарушений ночного зрения.
Цитирование: Lee, S.Y., Chang, CT., Yun, Y. et al. CryoEM structure of mGlu6 captures receptor activation prior to G protein coupling. Nat Commun 17, 3681 (2026). https://doi.org/10.1038/s41467-026-70436-w
Ключевые слова: ночная слепота, сетчаточная передача сигналов, рецепторы, сопряжённые с G-белками, метаботропный глутаматный рецептор, криоэлектронная микроскопия