Clear Sky Science · he
מכשיר CryoEM של mGlu6 תופס את הפעלת הקולטן לפני קישור לחלבון G
כיצד העיניים שלנו נשארות פעילות בחושך
היכולת לראות באור עמום תלויה במכונה מולקולרית זעירה ברשתית שאינה נחה. המכונה הזו, קולטן בשם mGlu6, יושבת בצומת בין התאים הפוטורצפטוריים מסוג Rod לבין תאי העצב המתווכים את האותות למוח. כאשר mGlu6 לא מתפקד, נולדים אנשים עם מצב הנקרא עיוורון לילי קונגניטלי סטציונרי — הם אינם רואים כראוי באור חלש, למרות שהעיניים נראות תקינות. המחקר הזה חושף את המבנה התלת־ממדי של mGlu6 ברזולוציה קרובה לאטומית ומסביר כיצד תנועתו מאפשרת ראיית לילה וכיצד מוטציות תורשתיות משבשות תהליך זה.
שומר שער פעיל בצומת הוויזואלי הראשון
בחשיכה, תאי ה‑rod ברשתית משחררים באופן מתמיד את השליח הכימי גלוטמט. האות הזה נקלט על ידי mGlu6 על פני תאי ה‑ON‑bipolar, המהווים את הזרוע הראשונה של העברת האות המושפע על ידי rods. mGlu6 פעיל מדליק מתג פנימי — חלבון G בשם Gαo — ששומר על תעלת יונים (TRPM1) סגורה כך שהתא ה‑bipolar נשאר שקט. כאשר אור פוגע ב‑rods, שחרור הגלוטמט יורד בפתאומיות, האיתות של mGlu6 כבה, התעלה נפתחת והתא הביפולרי נעשה פעיל ומודיע על נוכחות האור. מאחר שהמצב הזה חייב לפעול במהירות ובאופן רציף לאורך חיים, המבנה של mGlu6 צריך להיות גם יציב וגם מכויל בדייקנות מרבית.
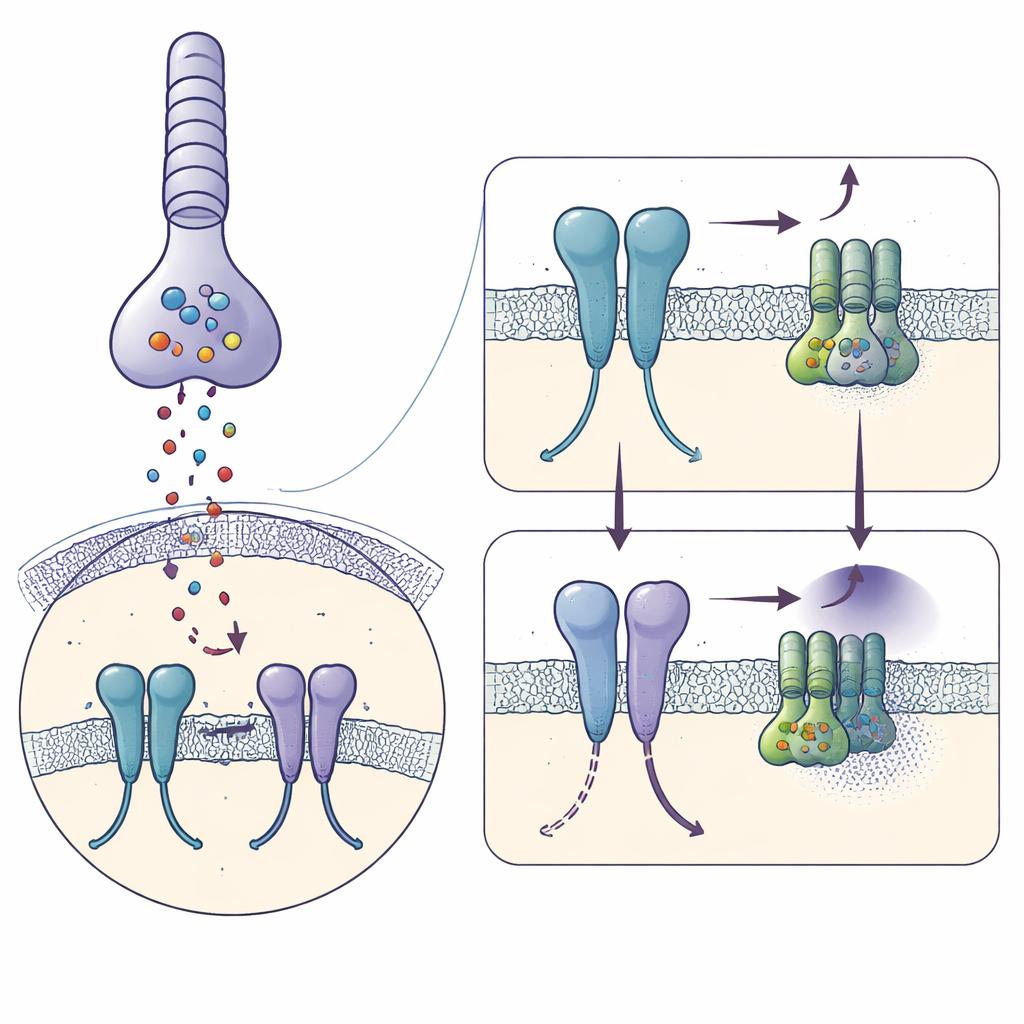
לתפוס את הקולטן ממש לפני שהוא משדר
בעזרת קריו־אלקטרון מיקרוסקופיה, החוקרים הקפיאו mGlu6 אנושי מזוקק קשור למפעיל חזק, L‑סרין O‑פוספט, ושחזרו את צורתו ברזולוציה של 3.2 אנגסטרם. כל מולקולת mGlu6 יוצרת זוג, או דימר, המורכב משלוש שכבות מוצלבות: "קונכיה" חיצונית גדולה שתפוסת גלוטמט, מקטע אמצעי גמיש עשיר בקשרי די־סולפיד, וחבילת שבעה סלילים החוצה את הממברנה שבהן נקשרים חלבוני G. המפעיל מהדק את הדומיינים החיצוניים בתנוחה סגורה הדומה לפעילה ומקרב את המקטעים האמצעיים זה לזה, בעוד הסלילים הממברנליים משנים מיקום כך שזוג סלילים מרכזי (נקראים TM6) מתקרבים זה לזה — סימנים אופייניים של קולטן שמוכן לקשור חלבון G.
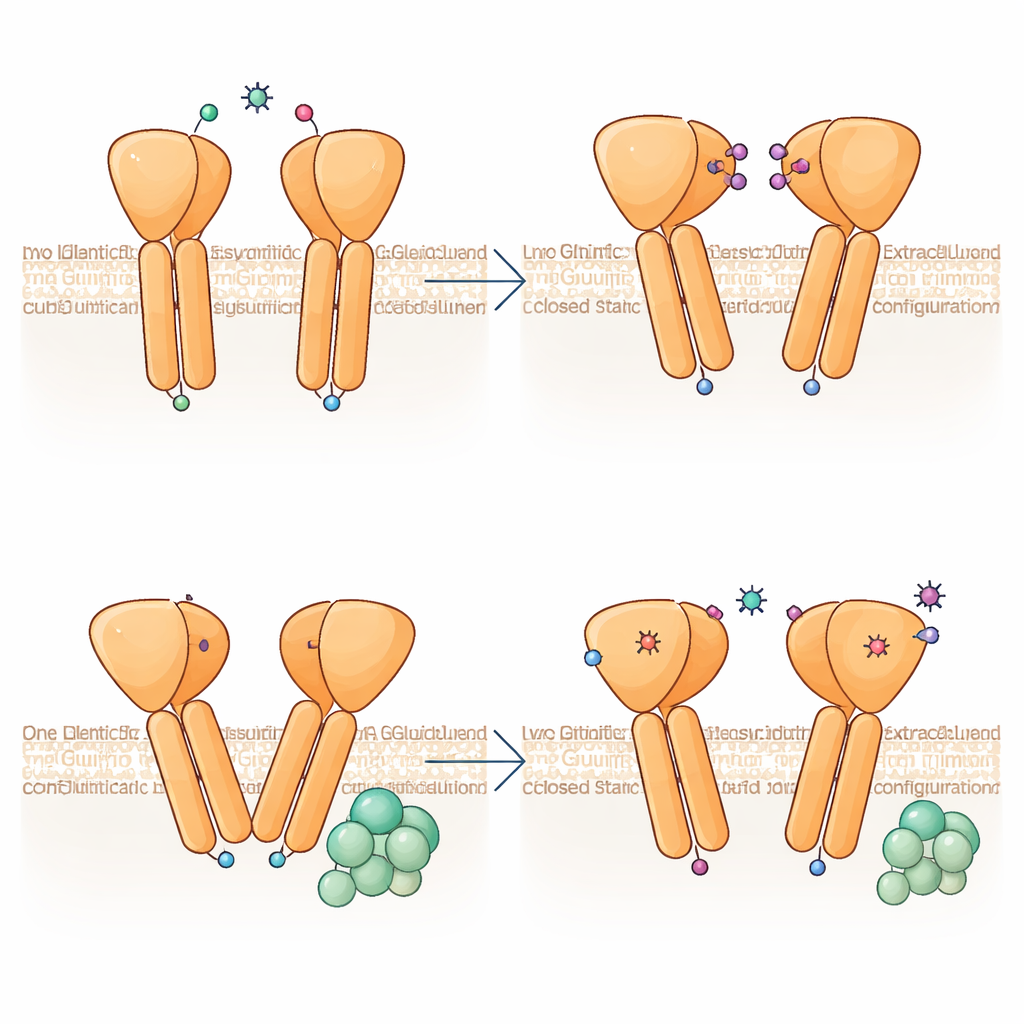
אי־סימטריה מובנית: צד אחד מוביל, השני עוקב
ממצא בולט הוא ששתי החצאים של דימר ה‑mGlu6 אינן מאמצות צורות זהות, אף על פי ששתיהן קושרות את המפעיל. סובוניט אחד מתקפל בהטיה חדה יותר, וסליליו הממברנליים עולים מעט גבוה יותר כלפי חוץ התא, ויוצרים ממשק אסימטרי שבו נפגשים שני סלילי TM6. תצורה זו דומה במידה רבה למצב של קישור חלבון G כפי שנצפה בקולטנים קרובים, ומה שמרמז ש‑mGlu6 "מוכנה מראש" לקישור בצד אחד. ניתוח של תמונות רבות מראה שהדימר מדגם רצף של זוויות קיפול, החל מכמעט סימטרי ועד אסימטרי חזק, מה שרומז שהקולטן מתנדנד בדינמיקה בין מצבים, כשהאי־סימטריה מתפתחת כבר לפני הגעת חלבון G.
תמך מוסתר שמאיץ את האיתות
העבודה מעלה גם מפגש יוצא דופן בין אזור האמצע העשיר בציסטאינים ולולאה על צידו החיצוני של הממברנה. ב‑mGlu6, הלולאה הזו ארוכה יותר מבקולטנים קשורים ויוצרת רשת של גשרים יוניים, קשרי מימן ומגעים הידרופוביים שמנעולים את האזורים האמצעיים והממברנליים יחד. כאשר שיירים חשובים בממשק זה משתנים במוטציה, הקולטן עדיין מגיע לפני שטח התא ויכול להפעיל חלבוני G, אבל הוא עושה זאת לאט יותר, אפילו כאשר יש שפע של קולטנים. הממצא מרמז שהמגעים הנוספים פועלים כמעין חיזוק מכני שמעביר ביעילות את תנועת הקונכיה החיצונית המושרת על ידי גלוטמט אל הסלילים הממברנליים, ומאפשר תגובות מהירות הנדרשות לראייה בזמן אמת.
להסביר עיוורון לילי דרך המבנה
על‑ידי מיפוי כל המוטציות הידועות של חולי עיוורון לילי קונגניטלי סטציונרי על המבנה החדש, המחברים מראים כיצד שינויים מגוונים יכולים לשתק את mGlu6. חלק מהמוטציות מעוותות את כיס קשירת הגלוטמט או משבשות ליבות הידרופוביות קבויות, מה שמרעיד את הדומיין החיצוני; אחרות שוברות קשרי די־סולפיד קריטיים או גשרים יוניים שמחזיקים יחד את האזורים האמצעיים והממברנליים, וגורמות לקולטן להתקמט ולכשל בהגעה לפני שטח התא. וריאנטים רבים מקטינים את היעילות או את המהירות של הפעלת חלבון G. מעניין ששתי מוטציות דווקא מגדילות את יכולת האיתות לאחר נרמול הביטוי, אך סביר שהן עדיין גורמות למחלה מפני שהקולטנים מסוכסנים בתנועה או מונחים בצורה לקויה בסינפסות. יחד, הממצאים מקשרים פגמים מבניים ספציפיים לאיתות לקוי ומספקים מפת דרכה מולקולרית להבנה ולבסוף לטיפול בהפרעות ראיית לילה תורשתיות.
ציטוט: Lee, S.Y., Chang, CT., Yun, Y. et al. CryoEM structure of mGlu6 captures receptor activation prior to G protein coupling. Nat Commun 17, 3681 (2026). https://doi.org/10.1038/s41467-026-70436-w
מילות מפתח: עיוורון לילי, אותות ברשתית, קולטנים מחוברי חלבון G, קולטן גלוטמט מטבוטרופי, קריו אלקטרון מיקרוסקופיה