Clear Sky Science · sv
CryoEM‑struktur av mGlu6 fångar receptoraktivering före G‑proteinkoppling
Hur våra ögon fungerar i mörker
Att se i svagt ljus beror på en liten molekylär maskin i näthinnan som aldrig vilar. Denna maskin, en receptor kallad mGlu6, sitter vid skarven mellan stavfotoreceptorer och de nervceller som för vidare signaler till hjärnan. När mGlu6 sviktar föds människor med en sjukdom som kallas kongenital stationär nattblindhet — de kan inte se korrekt i svagt ljus, trots att ögonen i övrigt ser normala ut. Denna studie avslöjar mGlu6:s tredimensionella struktur i nästan atomär detalj och förklarar hur dess rörelse möjliggör mörkerseende och hur ärftliga mutationer stör den processen.
En upptagen grindvakt vid synens första synaps
I mörker frisätter stavceller i näthinnan ständigt budbäraren glutamat. Denna signal fångas upp av mGlu6 på ytan av ON‑bipolära celler, som fungerar som första relä för stavdriven syn. Aktiv mGlu6 slår på en intern strömbrytare — ett G‑protein kallat Gαo — som håller en jonkanal (TRPM1) stängd så att bipolärcellen förblir tyst. När ljus träffar stavarna faller glutamatfrisättningen plötsligt, mGlu6‑signaleringen stängs av, kanalen öppnas och bipolärcellen aktiveras och meddelar att ljus föreligger. Eftersom denna växling måste fungera snabbt och kontinuerligt under en livstid behöver mGlu6:s struktur vara både stabil och ytterst finjusterad.
Fångar receptorn precis innan den signalerar
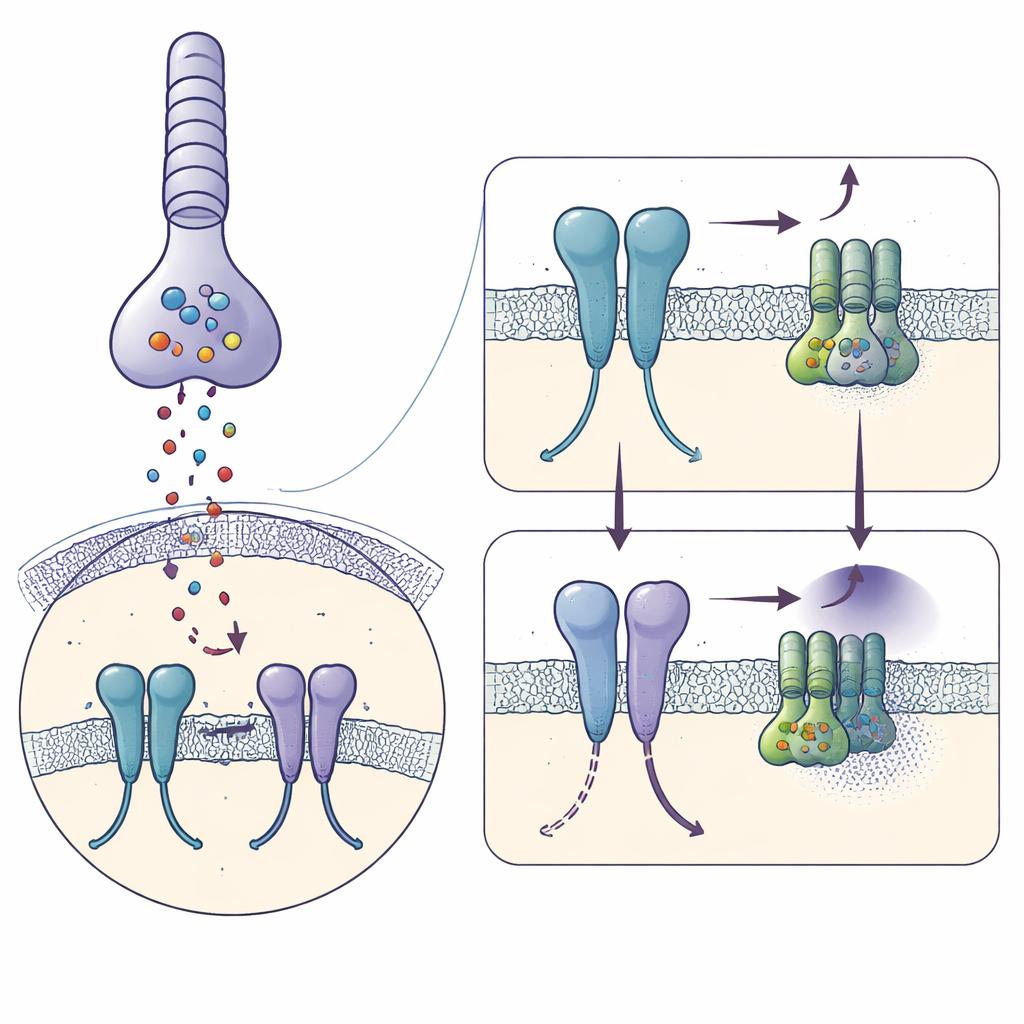
Med kryoelektronmikroskopi frös forskarna renat humant mGlu6 bundet till en stark aktivator, L‑serin O‑fosfat, och rekonstruerade dess form vid 3,2 ångström upplösning. Varje mGlu6‑molekyl bildar ett par, eller dimer, bestående av tre staplade regioner: ett stort ”klappskal” utanför cellen som fångar glutamat, en flexibel mellandel rik på disulfidbindningar, och en sju‑helix‑bunt som spänner över membranet där G‑proteiner binder. Aktivatorn klämmer ihop de yttre domänerna i en sluten, aktivliknande position och för mellandelarna nära varandra, medan membranhelixarna förskjuts så att ett nyckelpar av helixar (kallade TM6) kommer i nära kontakt — kännetecken för en receptor redo att ansluta till ett G‑protein.
Inbyggd asymmetri: ena parten leder, den andra följer
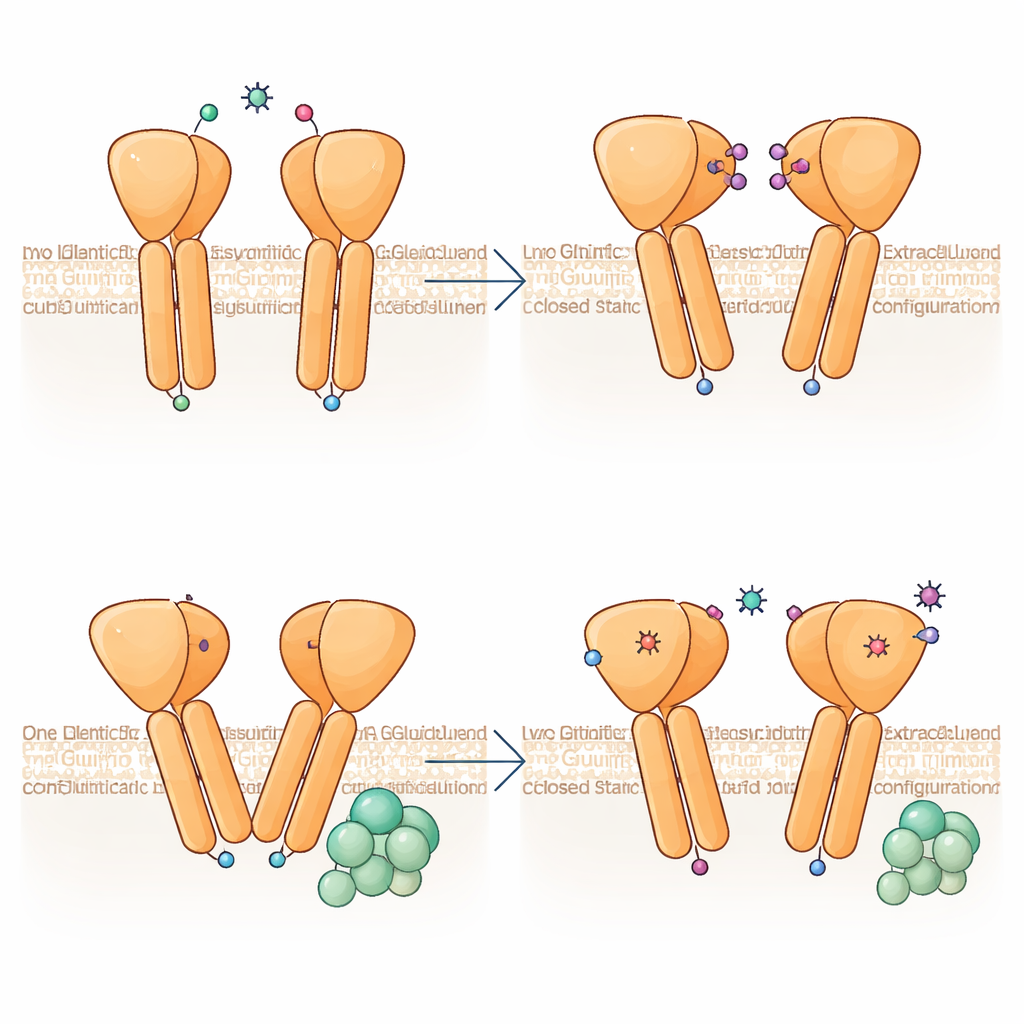
En slående upptäckt är att de två halvorna av mGlu6‑dimeren inte antar identiska former, trots att båda binder samma aktivator. En subenhet böjer sig mer markant och dess membranhelixar stiger något högre mot cellens utsida, vilket skapar en asymmetrisk gränsyta där de två TM6‑helixarna möts. Denna konfiguration liknar starkt det G‑protein‑anslutna tillstånd som observerats i närbesläktade receptorer, vilket tyder på att mGlu6 är ”för‑primad” för koppling på ena sidan. Analys av många partikelbilder visar att dimeren provar en kontinuerlig serie böjvinklar, från nästan symmetrisk till starkt asymmetrisk, vilket antyder att receptorn dynamiskt gungar mellan tillstånd och att asymmetrin uppstår redan innan ett G‑protein anländer.
En dold stödkonstruktion som snabbar upp signaleringen
Arbetet avslöjar också en ovanlig kontaktyta mellan den mellersta cysteinfattiga regionen och en slinga på membranets yttre sida. I mGlu6 är denna slinga längre än i närbesläktade receptorer och bildar ett nätverk av saltbryggor, vätebindningar och hydrofoba kontakter som låser ihop mellan‑ och membrandomänerna. När nyckelaminosyror i detta gränssnitt muteras når receptorn fortfarande cellytan och kan aktivera G‑proteiner, men den gör det långsammare, även när rikligt med receptorer finns. Detta tyder på att de extra kontakterna fungerar som en mekanisk förstärkning som effektivt överför glutamatinducerad rörelse i det yttre ”klappskalet” ner till membranhelixarna, vilket möjliggör snabba svar som krävs för realtidsseende.
Förklarar nattblindhet genom struktur
Genom att kartlägga alla kända patientmutationer för kongenital stationär nattblindhet på den nya strukturen visar författarna hur skiftande förändringar kan förlama mGlu6. Vissa mutationer förvränger glutamatbindande fickan eller stör inbäddade hydrofoba kärnor och destabliserar den yttre domänen; andra bryter viktiga disulfidbindningar eller saltbryggor som håller samman mellan‑ och membrandomänerna, vilket får receptorn att felvikta och misslyckas med att nå cellytan. Många varianter minskar effektiviteten eller hastigheten i G‑proteinaktiveringen. Intressant nog ökar två mutationer faktiskt signaleringen när uttrycket normaliseras, men orsakar ändå sannolikt sjukdom eftersom receptorerna transporteras dåligt eller hamnar felaktigt vid synapser. Tillsammans knyter dessa fynd specifika strukturella defekter till nedsatt signalering och erbjuder en molekylär ritning för att förstå och så småningom behandla ärftliga störningar i mörkerseendet.
Citering: Lee, S.Y., Chang, CT., Yun, Y. et al. CryoEM structure of mGlu6 captures receptor activation prior to G protein coupling. Nat Commun 17, 3681 (2026). https://doi.org/10.1038/s41467-026-70436-w
Nyckelord: nattblindhet, retinal signalering, G‑protein‑kopplade receptorer, metabotrop glutamatreceptor, kryoelektronmikroskopi