Clear Sky Science · fr
Structure CryoEM de mGlu6 révélant l’activation du récepteur avant le couplage au G-protéine
Comment nos yeux continuent de fonctionner dans l’obscurité
La vision en faible luminosité dépend d’une minuscule machine moléculaire dans la rétine qui ne s’arrête jamais. Cette machine, un récepteur appelé mGlu6, se trouve à la jonction entre les photorécepteurs en bâtonnets et les cellules nerveuses qui relayent les signaux vers le cerveau. Quand mGlu6 est défaillant, les patients naissent avec une affection connue sous le nom de cécité nyctémérale congénitale stationnaire : ils ne voient pas correctement en faible luminosité, alors que leurs yeux paraissent par ailleurs normaux. Cette étude révèle la structure tridimensionnelle de mGlu6 à une résolution proche de l’atomique et explique comment ses mouvements permettent la vision nocturne et comment des mutations héréditaires perturbent ce processus.
Un gardien très occupé à la première synapse de la vision
Dans l’obscurité, les cellules en bâtonnets de la rétine libèrent en continu le messager chimique glutamate. Ce signal est détecté par mGlu6 à la surface des cellules bipolaires ON, qui assurent le premier relais de la vision portée par les bâtonnets. Le mGlu6 actif active un interrupteur interne — une protéine G appelée Gαo — qui maintient un canal ionique (TRPM1) fermé, gardant la cellule bipolaire au repos. Lorsque la lumière atteint les bâtonnets, la libération de glutamate chute brusquement, la signalisation mGlu6 s’éteint, le canal s’ouvre et la cellule bipolaire s’active, signalant la présence de lumière. Parce que ce basculement doit fonctionner rapidement et en continu tout au long de la vie, la structure de mGlu6 doit être à la fois stable et finement réglée.
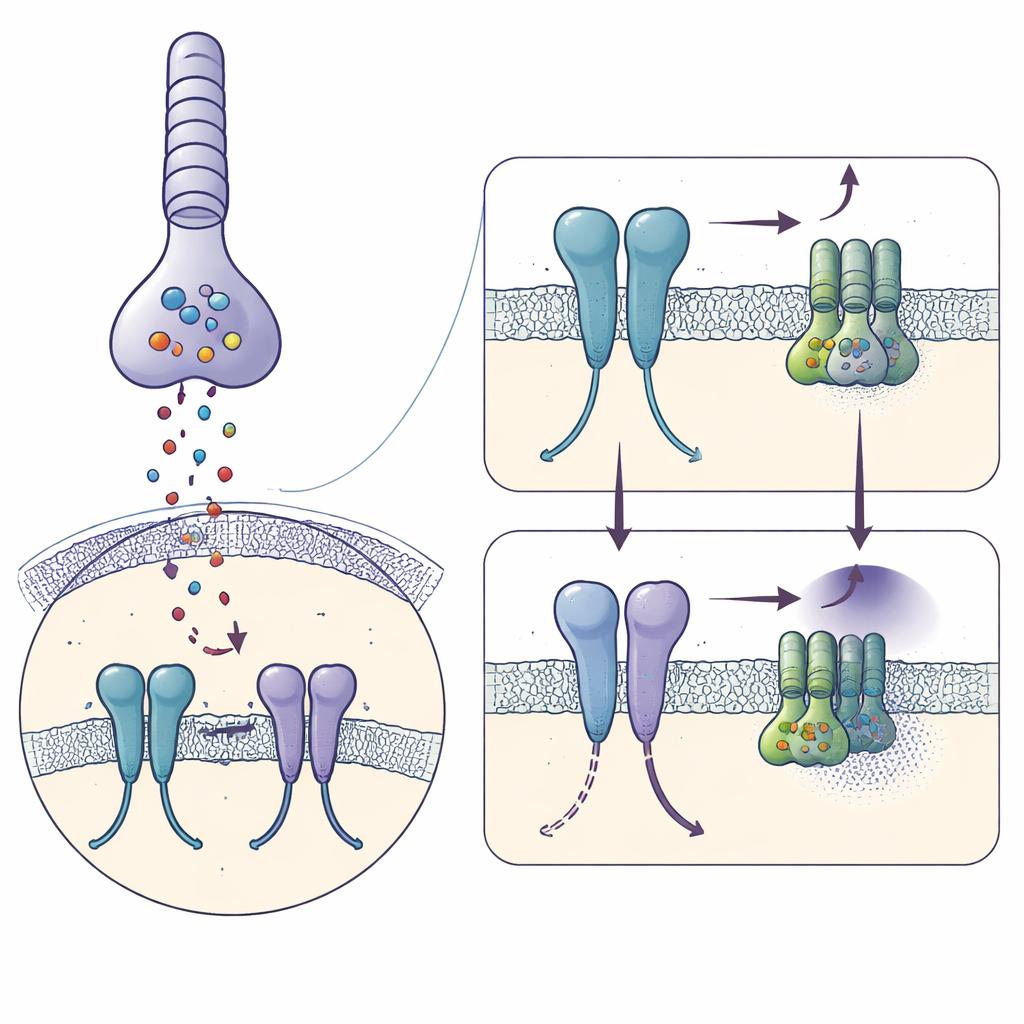
Capturer le récepteur juste avant qu’il ne signale
À l’aide de cryo‑microscopie électronique, les auteurs ont figé du mGlu6 humain purifié lié à un puissant activateur, la L‑sérine O‑phosphate, et reconstruit sa forme à une résolution de 3,2 Å. Chaque molécule de mGlu6 forme une paire, ou dimère, composée de trois régions empilées : une large « coquille » externe captant le glutamate, un segment intermédiaire flexible riche en ponts disulfure, et un faisceau de sept hélices traversant la membrane où se lient les protéines G. L’activateur maintient les domaines externes dans une pose fermée, proche de l’état actif, et rapproche les segments intermédiaires, tandis que les hélices transmembranaires se déplacent de sorte qu’une paire clé d’hélices (appelée TM6) entre en contact étroit — des caractéristiques d’un récepteur prêt à engager une protéine G.
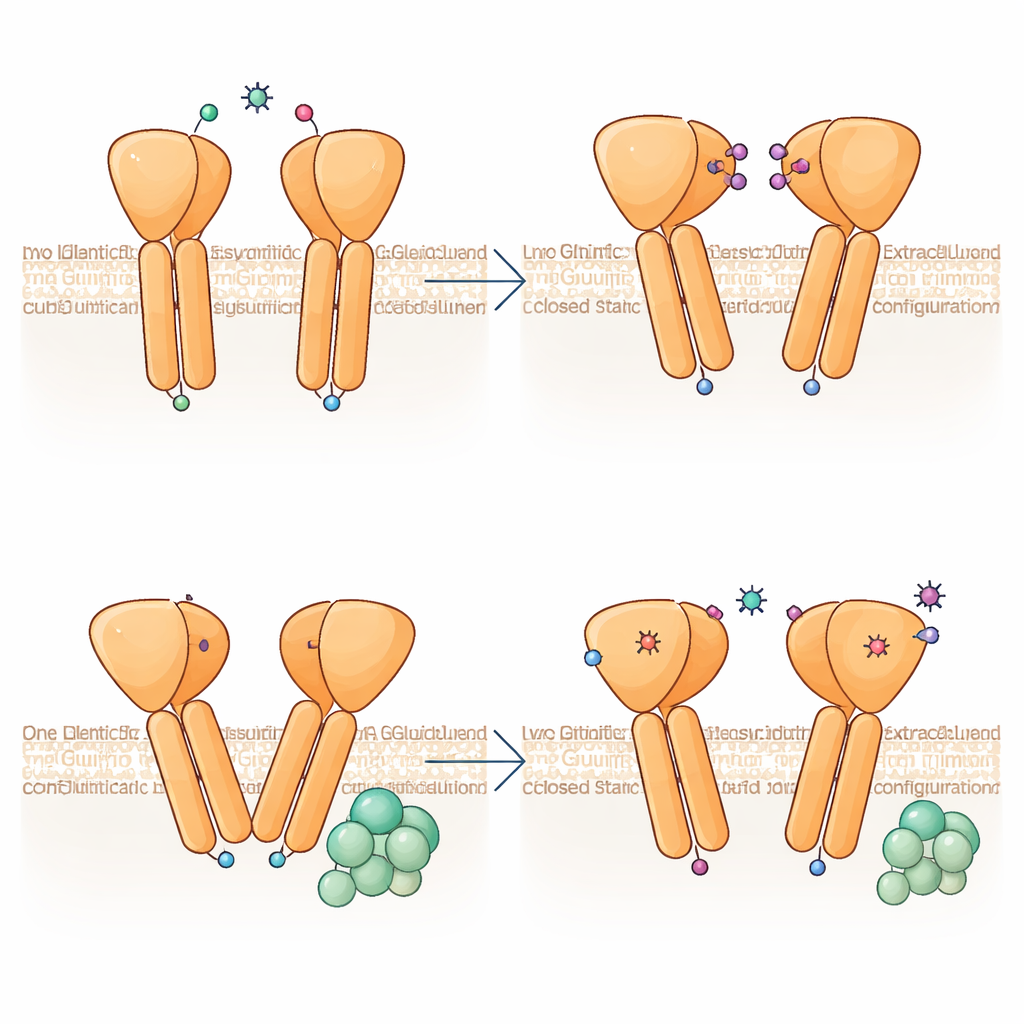
Asymétrie intégrée : un partenaire mène, l’autre suit
Une découverte marquante est que les deux moitiés du dimère mGlu6 n’adoptent pas des formes identiques, même si les deux lient le même activateur. Une sous‑unité se plie plus fortement et ses hélices membranaires s’élèvent légèrement vers l’extérieur de la cellule, produisant une interface asymétrique où les deux TM6 se rencontrent. Cette configuration ressemble étroitement à l’état de liaison à la protéine G observé chez des récepteurs apparentés, ce qui suggère que mGlu6 est « pré‑amorçé » pour le couplage d’un côté. Des analyses de nombreuses images de particules montrent que le dimère explore un continuum d’angles de pliure, allant d’un quasi‑symétrique à un fortement asymétrique, ce qui implique que le récepteur oscille dynamiquement entre états, l’asymétrie apparaissant déjà avant l’arrivée d’une protéine G.
Un support dissimulé qui accélère la signalisation
Le travail met aussi au jour une surface de contact inhabituelle entre la région intermédiaire riche en cystéines et une boucle du côté externe de la membrane. Chez mGlu6, cette boucle est plus longue que chez des récepteurs apparentés et forme un réseau de liaisons salines, de liaisons hydrogène et d’interactions hydrophobes qui verrouillent les régions intermédiaire et membranaire ensemble. Lorsque des résidus clés de cette interface sont mutés, le récepteur atteint toujours la surface cellulaire et peut activer des protéines G, mais il le fait plus lentement, même en présence d’un grand nombre de récepteurs. Cela suggère que ces contacts supplémentaires servent de renfort mécanique qui transmet efficacement le mouvement induit par le glutamate de la « coquille » externe jusqu’aux hélices membranaires, permettant des réponses rapides nécessaires à la vision en temps réel.
Expliquer la cécité nyctémérale par la structure
En cartographiant chaque mutation connue chez des patients atteints de cécité nyctémérale congénitale stationnaire sur la nouvelle structure, les auteurs montrent comment des altérations diverses peuvent neutraliser mGlu6. Certaines mutations déforment la poche de liaison du glutamate ou perturbent des cœurs hydrophobes enfouis, déstabilisant le domaine externe ; d’autres rompent des ponts disulfure ou des liaisons salines cruciales qui maintiennent ensemble les régions intermédiaire et membranaire, provoquant un mauvais repliement du récepteur et son incapacité à atteindre la surface cellulaire. De nombreux variants réduisent l’efficacité ou la vitesse d’activation des protéines G. Fait intrigant, deux mutations augmentent en réalité la capacité de signalisation une fois l’expression normalisée, mais provoquent probablement quand même la maladie parce que les récepteurs sont mal transportés ou mal positionnés aux synapses. Ensemble, ces résultats relient des défauts structuraux précis à une signalisation altérée, offrant une feuille de route moléculaire pour comprendre et, éventuellement, traiter les troubles héréditaires de la vision nocturne.
Citation: Lee, S.Y., Chang, CT., Yun, Y. et al. CryoEM structure of mGlu6 captures receptor activation prior to G protein coupling. Nat Commun 17, 3681 (2026). https://doi.org/10.1038/s41467-026-70436-w
Mots-clés: cécité nyctémérale, signalisation rétinienne, récepteurs couplés aux protéines G, récepteur métabotropique du glutamate, cryo‑microscopie électronique