Clear Sky Science · pl
Struktura mGlu6 uzyskana metodą kriomikroskopii pokazuje aktywację receptora tuż przed sprzężeniem z białkiem G
Jak nasze oczy działają w ciemności
Widzenie przy słabym świetle zależy od maleńkiej molekularnej maszyny w siatkówce, która nigdy nie odpoczywa. Ta maszyna — receptor o nazwie mGlu6 — znajduje się na styku między pręcikami a komórkami nerwowymi przekazującymi sygnały do mózgu. Gdy mGlu6 zawodzi, ludzie rodzą się z zespołem wrodzonej stacjonarnej ślepoty nocnej — nie widzą prawidłowo przy słabym oświetleniu, mimo że ich oczy wyglądają na zdrowe. Badanie ujawnia trójwymiarową strukturę mGlu6 z niemal atomową rozdzielczością i wyjaśnia, jak jego ruchy umożliwiają widzenie w nocy oraz jak dziedziczne mutacje zakłócają ten proces.
Zajęty strażnik w pierwszym synapsie wzroku
W ciemności komórki pręcikowe siatkówki stale uwalniają przekaźnik chemiczny — glutaminian. Ten sygnał odbiera mGlu6 na powierzchni komórek ON‑bipolarnych, które pełnią pierwszą rolę przekaźnikową w widzeniu napędzanym przez pręciki. Aktywne mGlu6 załącza wewnętrzny przełącznik — białko G zwane Gαo — które utrzymuje zamknięty kanał jonowy (TRPM1), powodując, że komórka bipolarną pozostaje w stanie spoczynku. Gdy dociera światło, uwalnianie glutaminianu gwałtownie spada, sygnalizacja mGlu6 wyłącza się, kanał otwiera, a komórka bipolarna staje się aktywna, sygnalizując obecność światła. Ponieważ ten przełącznik musi działać szybko i ciągle przez całe życie, struktura mGlu6 musi być jednocześnie stabilna i bardzo precyzyjnie dostrojona.
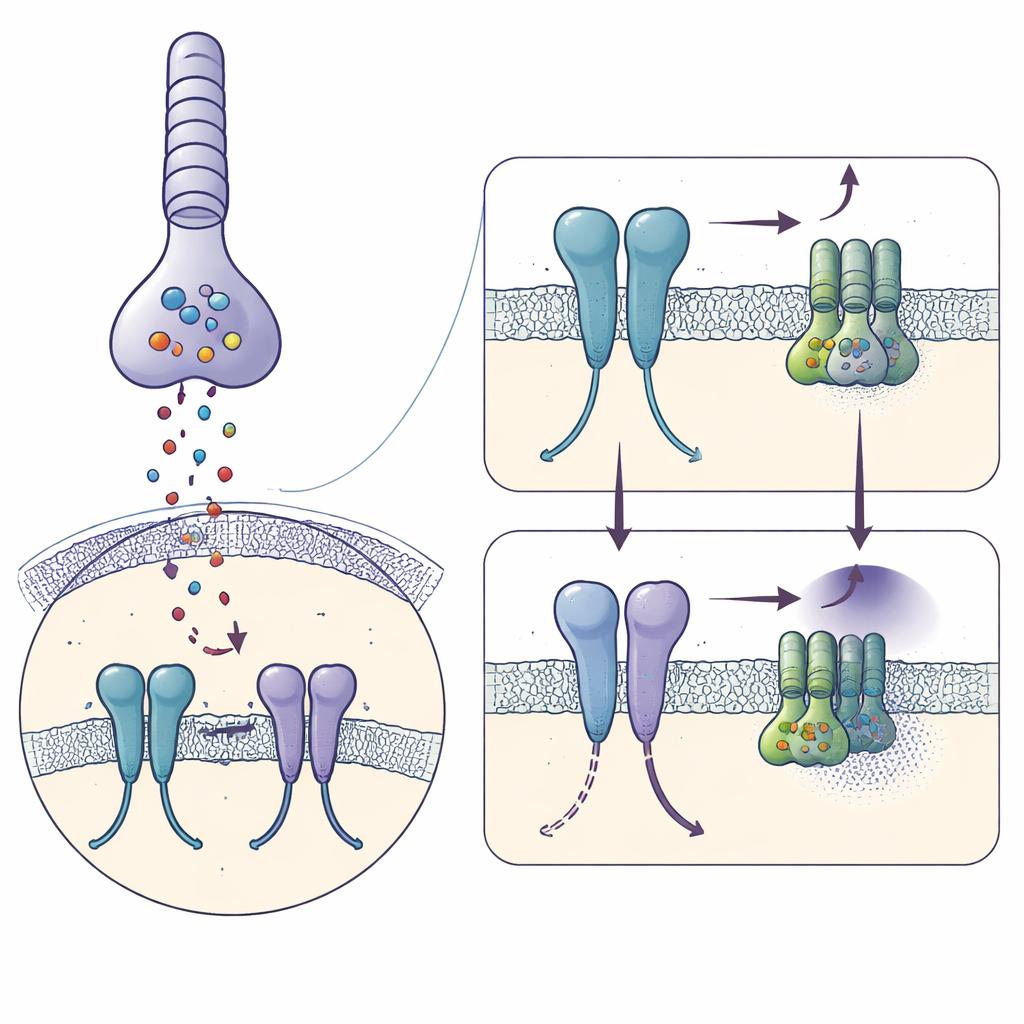
Uchwycenie receptora tuż przed wysłaniem sygnału
Przy użyciu kriomikroskopii elektronowej autorzy zamrozili oczyszczony ludzki mGlu6 związany z silnym aktywatorem, L‑seryną O‑fosforanem, i odtworzyli jego kształt w rozdzielczości 3,2 ångströma. Każda cząsteczka mGlu6 tworzy parę — dimer — złożony z trzech ułożonych na sobie regionów: dużej zewnętrznej „muszli” wychwytującej glutaminian, elastycznego środkowego odcinka bogatego w mostki disiarczkowe oraz siedmiowęglowej wiązki helis przenikającej błonę, gdzie wiążą się białka G. Aktywator zaciska zewnętrzne domeny w zamkniętej, aktywnej konfiguracji i zbliża środkowe segmenty, podczas gdy helisy błonowe przesuwają się tak, że para kluczowych helis (zwanych TM6) dochodzi do bliskiego kontaktu — cechy charakterystyczne receptora gotowego do związania z białkiem G.
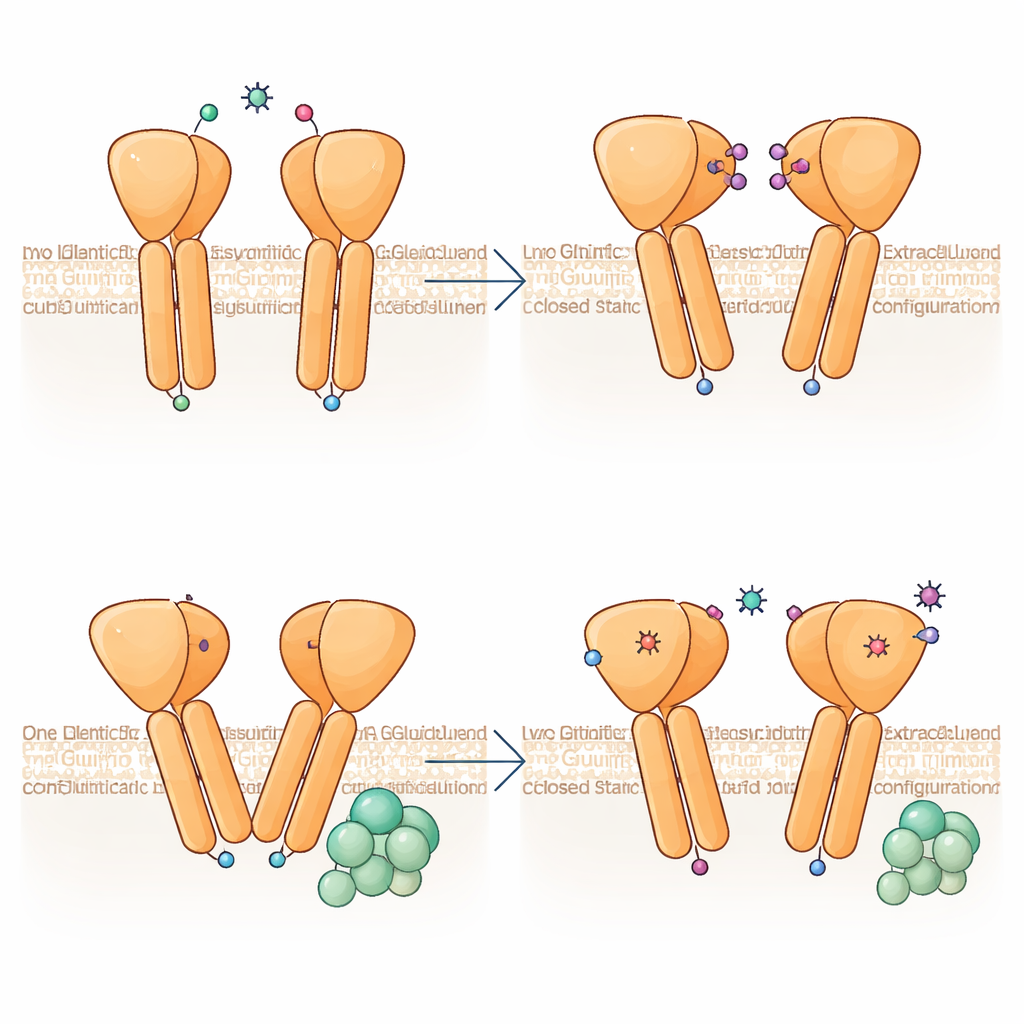
Wbudowana asymetria: Jeden partner prowadzi, drugi podąża
Uderzające odkrycie polega na tym, że dwie połowy dimerycznego mGlu6 nie przyjmują identycznych kształtów, mimo że obie wiążą ten sam aktywator. Jeden podjednostka zgina się bardziej ostro, a jej helisy błonowe unoszą się nieco wyżej w kierunku zewnętrznej strony komórki, tworząc asymetryczne miejsce styku, gdzie spotykają się obie helisy TM6. Ta konfiguracja przypomina stan zaangażowania białka G obserwowany w pokrewnych receptorach, co sugeruje, że mGlu6 jest „wstępnie przygotowany” do sprzężenia po jednej stronie. Analiza wielu obrazów cząstek pokazuje, że dimer próbuje ciągłości kątów zgięcia, od niemal symetrycznych do silnie asymetrycznych, co wskazuje, że receptor dynamicznie kołysze się między stanami, a asymetria pojawia się już przed nadejściem białka G.
Ukryty stelaż wspierający, który przyspiesza sygnalizację
Praca ujawnia również nietypową powierzchnię kontaktu między środkowym regionem bogatym w cysteiny a pętlą po zewnętrznej stronie błony. W mGlu6 ta pętla jest dłuższa niż w pokrewnych receptorach i tworzy sieć mostków solnych, wiązań wodorowych oraz kontaktów hydrofobowych, które zespalają razem regiony środkowy i błonowy. Gdy kluczowe reszty w tym interfejsie są zmutowane, receptor wciąż dociera do powierzchni komórki i potrafi aktywować białka G, lecz robi to wolniej, nawet przy obfitej liczbie receptorów. Sugeruje to, że dodatkowe kontakty działają jak mechaniczna rozpórka, efektywnie przekazująca ruch zewnętrznej „muszli” wywołany przez glutaminian do helis błonowych, umożliwiając szybkie odpowiedzi potrzebne do widzenia w czasie rzeczywistym.
Wyjaśnienie ślepoty nocnej przez strukturę
Mapując każdą znaną mutację pacjentów z wrodzoną stacjonarną ślepotą nocną na nowej strukturze, autorzy pokazują, jak różnorodne zmiany mogą unieruchomić mGlu6. Niektóre mutacje zniekształcają kieszeń wiążącą glutaminian lub zakłócają zatopione hydrofobowe rdzenie, destabilizując domenę zewnętrzną; inne łamią kluczowe mostki disiarczkowe lub mostki solne trzymające razem regiony środkowy i błonowy, powodując nieprawidłowe fałdowanie receptora i jego brak dojścia do powierzchni komórki. Wiele wariantów zmniejsza wydajność lub szybkość aktywacji białka G. Co ciekawe, dwie mutacje faktycznie zwiększają zdolność sygnalizowania po normalizacji ekspresji, lecz wciąż prawdopodobnie powodują chorobę, ponieważ receptory są słabo transportowane lub niewłaściwie zlokalizowane w synapsach. Razem te odkrycia łączą konkretne defekty strukturalne z upośledzoną sygnalizacją, oferując molekularny szkic do zrozumienia i w końcu leczenia dziedzicznych zaburzeń widzenia w nocy.
Cytowanie: Lee, S.Y., Chang, CT., Yun, Y. et al. CryoEM structure of mGlu6 captures receptor activation prior to G protein coupling. Nat Commun 17, 3681 (2026). https://doi.org/10.1038/s41467-026-70436-w
Słowa kluczowe: ślepotą nocna, sygnalizacja siatkówkowa, receptory sprzężone z białkami G, metabotropowy receptor glutaminianowy, kriomikroskopia elektronowa