Clear Sky Science · es
Estructura por CryoEM de mGlu6 capta la activación del receptor antes del acoplamiento con la proteína G
Cómo nuestros ojos siguen funcionando en la oscuridad
Ver con poca luz depende de una diminuta máquina molecular en la retina que nunca descansa. Esta máquina, un receptor llamado mGlu6, se sitúa en la unión entre los fotorreceptores en bastón y las neuronas que transmiten las señales al cerebro. Cuando mGlu6 falla, las personas nacen con una afección conocida como ceguera nocturna estacionaria congénita: no pueden ver correctamente con poca luz, aunque sus ojos en general parecen normales. Este estudio revela la estructura tridimensional de mGlu6 con detalle cercano al atómico y explica cómo su movimiento permite la visión nocturna y cómo las mutaciones heredadas alteran ese proceso.
Un guardián ocupado en la primera sinapsis de la visión
En la oscuridad, las células en bastón de la retina liberan constantemente el mensajero químico glutamato. Esta señal la capta mGlu6 en la superficie de las células bipolares ON, que actúan como el primer relevo para la visión impulsada por bastones. mGlu6 activo enciende un interruptor interno: una proteína G llamada Gαo, que mantiene cerrado un canal iónico (TRPM1) para que la célula bipolar permanezca en reposo. Cuando la luz incide sobre los bastones, la liberación de glutamato cae de forma abrupta, la señalización de mGlu6 se apaga, el canal se abre y la célula bipolar se activa, anunciando la presencia de luz. Dado que este conmutador debe funcionar de manera rápida y continua durante toda la vida, la estructura de mGlu6 debe ser a la vez estable y extraordinariamente precisa.
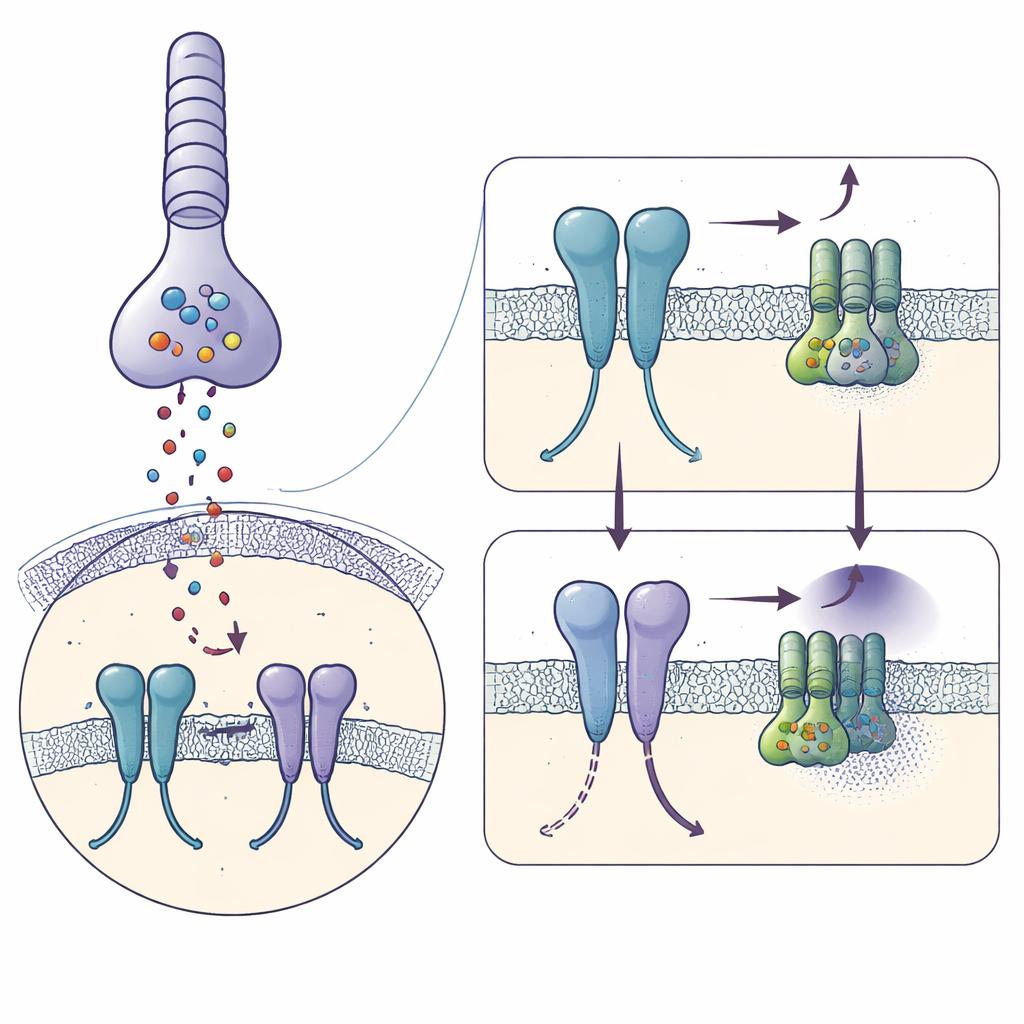
Capturando el receptor justo antes de que señalice
Usando crio‑microscopía electrónica, los autores congelaron mGlu6 humano purificado unido a un activador potente, la L‑serina O‑fosfato, y reconstruyeron su forma a 3,2 Å de resolución. Cada molécula de mGlu6 forma un par, o dímero, compuesto por tres regiones apiladas: una gran “concha” exterior que capta el glutamato, un segmento medio flexible rico en enlaces disulfuro y un paquete de siete hélices que atraviesa la membrana donde se unen las proteínas G. El activador sujeta los dominios externos en una pose cerrada, similar a la activa, y acerca los segmentos medios, mientras que las hélices de la membrana se desplazan de modo que un par clave de hélices (llamadas TM6) entra en contacto cercano, señales características de un receptor preparado para enganchar una proteína G.
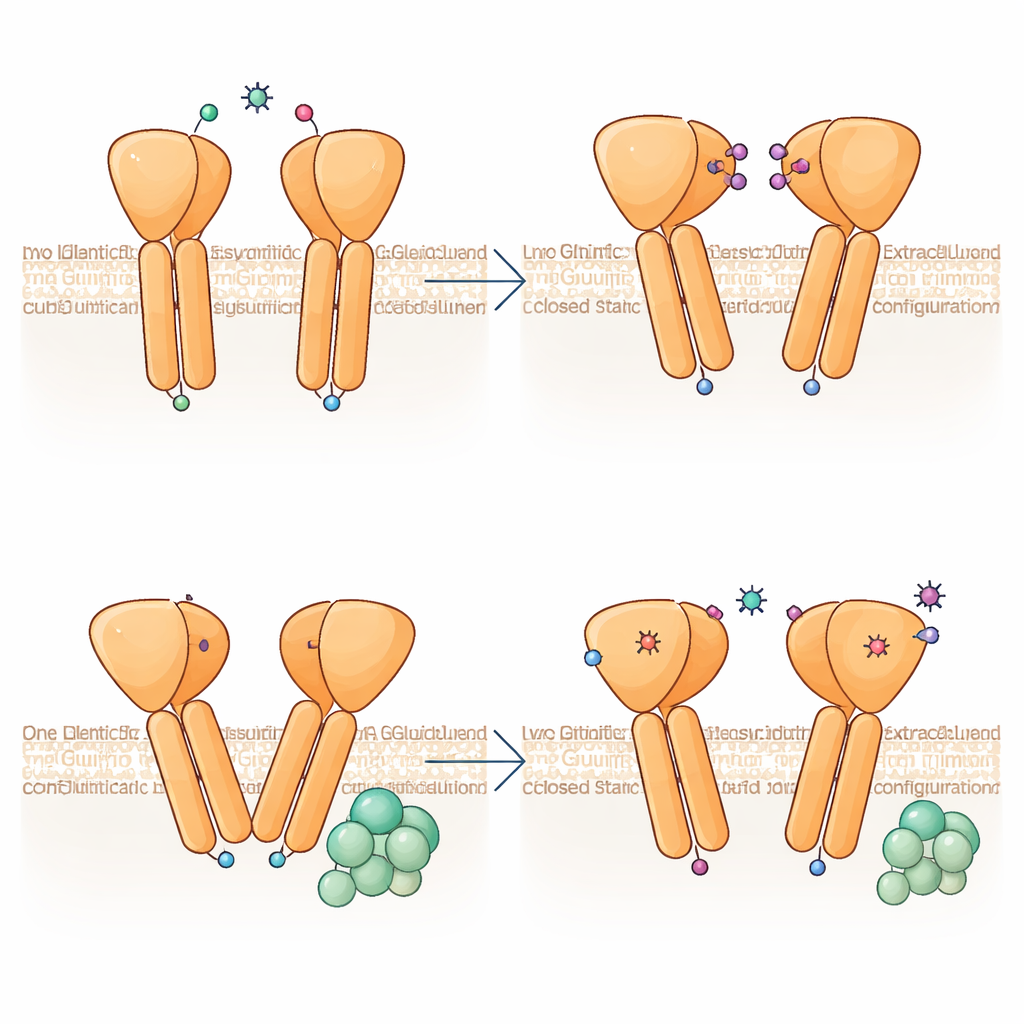
Asimetría incorporada: un socio lidera y el otro sigue
Un hallazgo llamativo es que las dos mitades del dímero mGlu6 no adoptan formas idénticas, aunque ambas se unan al mismo activador. Una subunidad se dobla con mayor brusquedad y sus hélices de membrana se elevan ligeramente hacia el exterior celular, produciendo una interfaz asimétrica donde se encuentran las dos TM6. Esta configuración se asemeja mucho al estado de acoplamiento con proteína G visto en receptores relacionados, lo que sugiere que mGlu6 está “preparado” para el acoplamiento por un lado. Análisis de muchas imágenes de partículas muestran que el dímero explora un continuo de ángulos de flexión, desde casi simétrico hasta fuertemente asimétrico, lo que implica que el receptor oscila dinámicamente entre estados, con la asimetría emergiendo ya antes de la llegada de la proteína G.
Un andamiaje oculto que acelera la señalización
El trabajo también descubre una superficie de contacto inusual entre la región media rica en cisteína y una hebra (loop) en el lado externo de la membrana. En mGlu6, esta hebra es más larga que en receptores relacionados y forma una red de puentes salinos, enlaces de hidrógeno y contactos hidrofóbicos que bloquean las regiones media y de membrana entre sí. Cuando residuos clave en esta interfaz se mutan, el receptor aún llega a la superficie celular y puede activar proteínas G, pero lo hace más lentamente, incluso cuando hay abundancia de receptores. Esto sugiere que los contactos adicionales actúan como un refuerzo mecánico que transmite de forma eficiente el movimiento inducido por el glutamato de la “concha” externa hacia las hélices de la membrana, permitiendo respuestas rápidas necesarias para la visión en tiempo real.
Explicando la ceguera nocturna a través de la estructura
Al mapear cada mutación conocida de pacientes con ceguera nocturna estacionaria congénita sobre la nueva estructura, los autores muestran cómo cambios diversos pueden incapacitar a mGlu6. Algunas mutaciones deforman el bolsillo de unión al glutamato o interrumpen núcleos hidrofóbicos enterrados, desestabilizando el dominio externo; otras rompen enlaces disulfuro cruciales o puentes salinos que mantienen unidas las regiones media y de membrana, causando que el receptor se pliegue mal y no llegue a la superficie celular. Muchas variantes reducen la eficiencia o la velocidad de activación de la proteína G. De manera intrigante, dos mutaciones aumentan en realidad la capacidad de señalización una vez normalizada la expresión, pero aun así probablemente causan la enfermedad porque los receptores se transportan mal o se ubican incorrectamente en las sinapsis. En conjunto, estos hallazgos relacionan defectos estructurales específicos con la señalización deteriorada, ofreciendo un plano molecular para comprender y, eventualmente, tratar los trastornos hereditarios de la visión nocturna.
Cita: Lee, S.Y., Chang, CT., Yun, Y. et al. CryoEM structure of mGlu6 captures receptor activation prior to G protein coupling. Nat Commun 17, 3681 (2026). https://doi.org/10.1038/s41467-026-70436-w
Palabras clave: ceguera nocturna, señalización retiniana, receptores acoplados a proteínas G, receptor metabotrópico de glutamato, crioelectrón microscopía