Clear Sky Science · pt
Estrutura por CryoEM de mGlu6 captura a ativação do receptor antes do acoplamento à proteína G
Como nossos olhos continuam funcionando no escuro
Ver em luz fraca depende de uma pequena máquina molecular na retina que nunca dorme. Essa máquina, um receptor chamado mGlu6, fica na junção entre os fotorreceptores bastonetes e as células nervosas que transmitem sinais ao cérebro. Quando o mGlu6 falha, as pessoas nascem com uma condição conhecida como cegueira noturna estacionária congênita — elas não enxergam bem em pouca luz, embora os olhos pareçam normais por fora. Este estudo revela a estrutura tridimensional do mGlu6 em detalhe quase atômico e explica como seu movimento permite a visão noturna e como mutações herdadas alteram esse processo.
Um porteiro atarefado na primeira sinapse da visão
No escuro, as células bastonete na retina liberam constantemente o mensageiro químico glutamato. Esse sinal é detectado pelo mGlu6 na superfície das células bipolares ON, que atuam como o primeiro relé da visão conduzida pelos bastonetes. O mGlu6 ativo liga um interruptor interno — uma proteína G chamada Gαo — que mantém um canal iônico (TRPM1) fechado, deixando a célula bipolar silenciosa. Quando a luz atinge os bastonetes, a liberação de glutamato cai abruptamente, a sinalização do mGlu6 desliga, o canal se abre e a célula bipolar fica ativa, anunciando a presença de luz. Como esse comutador precisa operar rápida e continuamente ao longo da vida, a estrutura do mGlu6 precisa ser ao mesmo tempo estável e finamente ajustada.
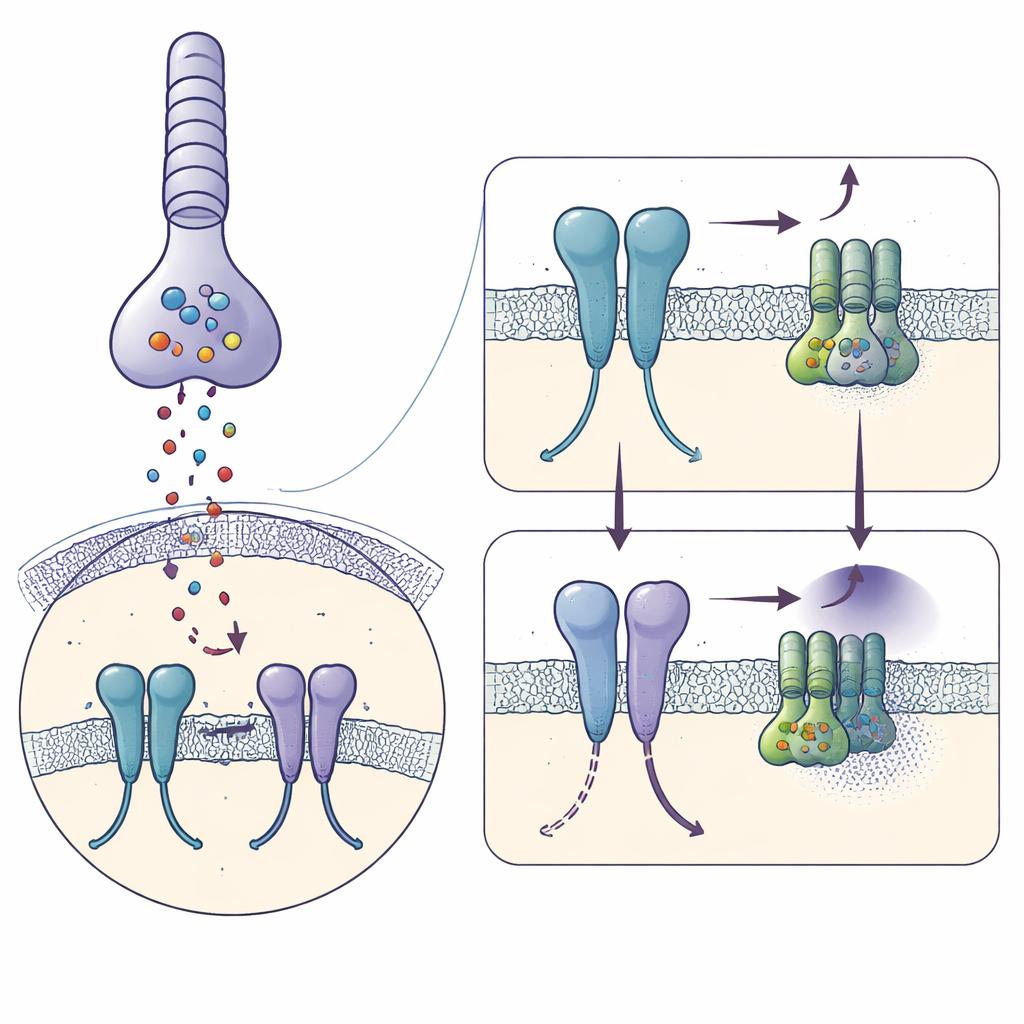
Capturando o receptor pouco antes de sinalizar
Usando crio‑microscopia eletrônica, os autores congelaram mGlu6 humano purificado ligado a um ativador potente, a L‑serina O‑fosfato, e reconstruíram sua forma a 3,2 ångström de resolução. Cada molécula de mGlu6 forma um par, ou dímero, composto por três regiões empilhadas: uma grande “concha” externa que captura o glutamato, um segmento médio flexível rico em pontes dissulfeto, e um feixe de sete hélices que atravessa a membrana onde as proteínas G se ligam. O ativador prende os domínios externos em uma pose fechada, semelhante à ativa, e aproxima os segmentos médios, enquanto as hélices na membrana se deslocam de modo que um par chave de hélices (chamadas TM6) entra em contato próximo — marcas de um receptor pronto para engajar uma proteína G.
Assimetria embutida: um parceiro lidera, o outro segue
Uma descoberta marcante é que as duas metades do dímero mGlu6 não adotam formas idênticas, embora ambas se liguem ao mesmo ativador. Uma subunidade se dobra com mais acentuamento, e suas hélices de membrana sobem ligeiramente em direção ao exterior da célula, produzindo uma interface assimétrica onde as duas hélices TM6 se encontram. Essa configuração assemelha‑se estreitamente ao estado engajado com proteína G observado em receptores relacionados, sugerindo que o mGlu6 está “pré‑armado” para o acoplamento de um lado. Análises de muitas imagens de partículas mostram que o dímero explora um continuum de ângulos de dobra, do quase simétrico ao fortemente assimétrico, o que implica que o receptor oscila dinamicamente entre estados, com a assimetria emergindo já antes da chegada da proteína G.
Um suporte oculto que acelera a sinalização
O trabalho também revela uma superfície de contato incomum entre a região média rica em cisteína e uma alça no lado externo da membrana. No mGlu6, essa alça é mais longa do que em receptores relacionados e forma uma teia de ligações salinas, pontes de hidrogênio e contatos hidrofóbicos que travam as regiões média e de membrana juntas. Quando resíduos-chave nessa interface são mutados, o receptor ainda alcança a superfície celular e pode ativar proteínas G, mas o faz mais lentamente, mesmo na presença de muitos receptores. Isso sugere que os contatos extras atuam como um reforço mecânico que transmite eficientemente o movimento induzido pelo glutamato da “concha” externa até as hélices da membrana, possibilitando respostas rápidas necessárias para a visão em tempo real.
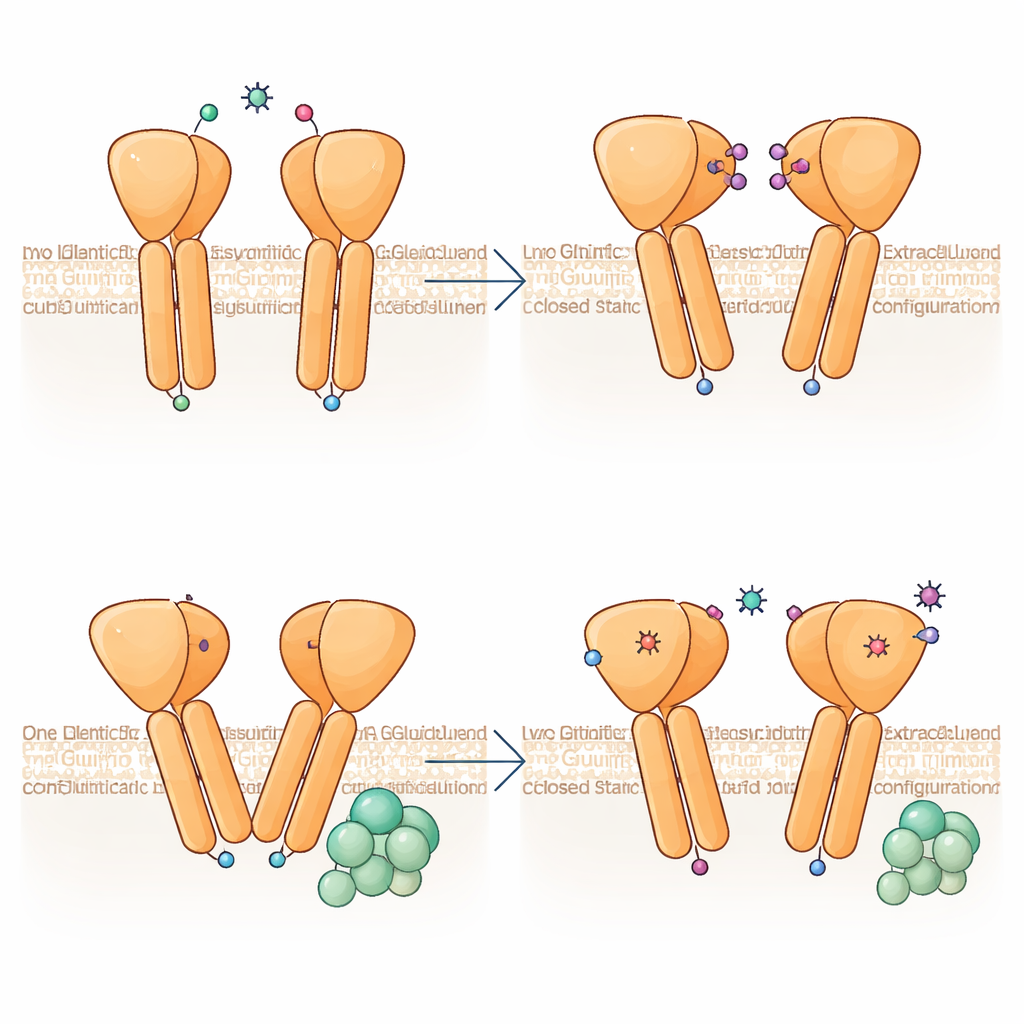
Explicando a cegueira noturna pela estrutura
Ao mapear cada mutação conhecida de pacientes com cegueira noturna estacionária congênita na nova estrutura, os autores mostram como alterações diversas podem comprometer o mGlu6. Algumas mutações deformam o bolso de ligação ao glutamato ou perturbam núcleos hidrofóbicos enterrados, desestabilizando o domínio externo; outras quebram pontes dissulfeto cruciais ou ligações salinas que unem as regiões média e de membrana, fazendo o receptor se dobrar incorretamente e falhar em alcançar a superfície celular. Muitas variantes reduzem a eficiência ou a velocidade de ativação da proteína G. Curiosamente, duas mutações na verdade aumentam a capacidade de sinalização uma vez que a expressão é normalizada, mas ainda assim provavelmente causam a doença porque os receptores são mal transportados ou mal posicionados nas sinapses. Em conjunto, esses achados vinculam defeitos estruturais específicos à sinalização prejudicada, oferecendo um mapa molecular para entender e, eventualmente, tratar distúrbios hereditários da visão noturna.
Citação: Lee, S.Y., Chang, CT., Yun, Y. et al. CryoEM structure of mGlu6 captures receptor activation prior to G protein coupling. Nat Commun 17, 3681 (2026). https://doi.org/10.1038/s41467-026-70436-w
Palavras-chave: cegueira noturna, sinalização retinal, receptores acoplados à proteína G, receptor metabotrópico de glutamato, crio‑microscopia eletrônica