Clear Sky Science · nl
CryoEM-structuur van mGlu6 legt receptoractivatie vast vóór G‑proteïne‑koppeling
Hoe onze ogen blijven functioneren in het donker
Zien bij weinig licht hangt af van een klein moleculair apparaat in het netvlies dat nooit rust. Dit apparaat, een receptor genaamd mGlu6, bevindt zich op de grens tussen staaffotoreceptoren en de zenuwcellen die signalen naar de hersenen doorgeven. Wanneer mGlu6 faalt, worden mensen geboren met een aandoening die congenitale stationaire nachtblindheid wordt genoemd — zij kunnen in zwak licht niet goed zien, terwijl hun ogen er verder normaal uitzien. Deze studie onthult de driedimensionale structuur van mGlu6 tot bijna atomair detail en verklaart hoe de beweging van de receptor nachtzicht mogelijk maakt en hoe erfelijke mutaties dat proces verstoren.
Een drukke poortwachter bij de eerste synaps van het zicht
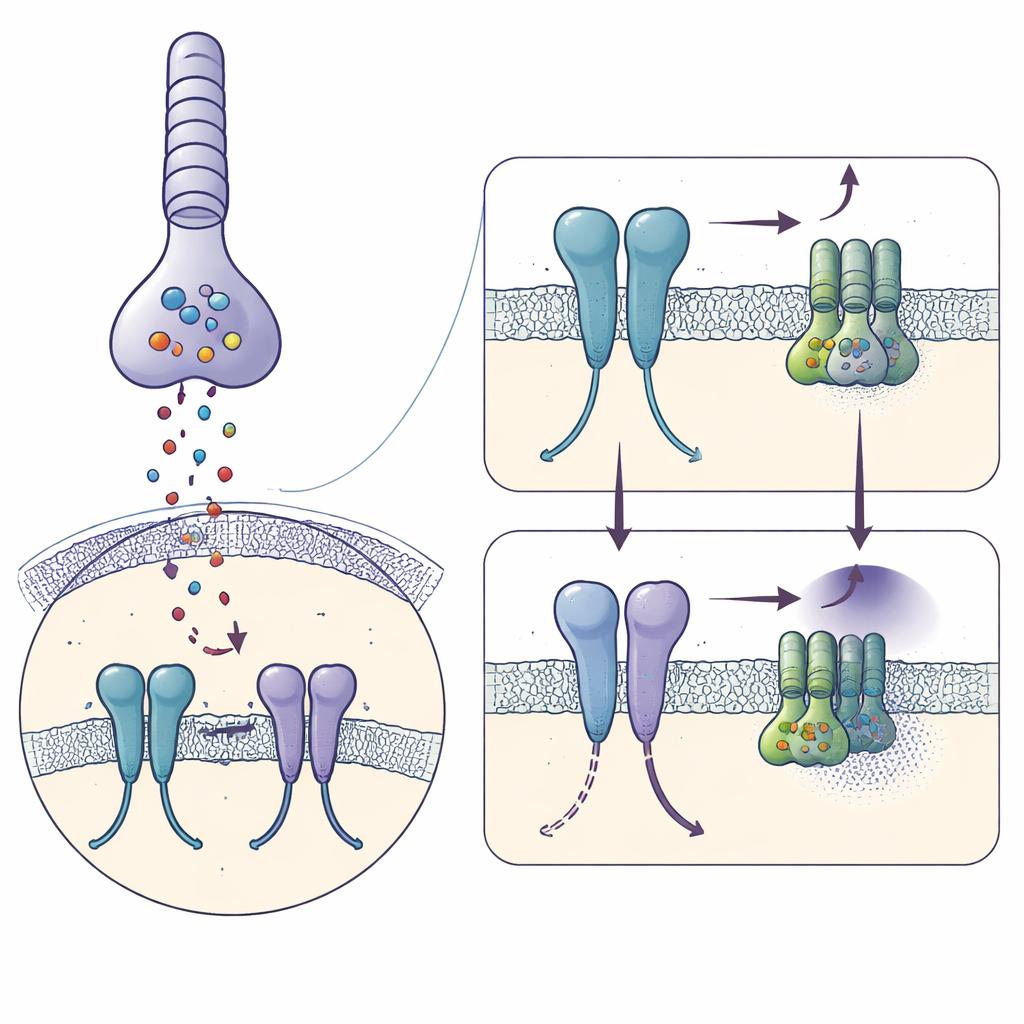
In het donker geven staafcellen in het netvlies continu de chemische boodschapper glutamaat af. Dit signaal wordt opgevangen door mGlu6 op het oppervlak van ON‑bipolaire cellen, die als eerste schakel fungeren voor door staven aangedreven zicht. Actieve mGlu6 schakelt een interne schakelaar in — een G‑eiwit genaamd Gαo — dat een ionenkanaal (TRPM1) gesloten houdt zodat de bipolaire cel stil blijft. Wanneer licht de staven raakt, daalt de glutamaatafgifte abrupt, schakelt de mGlu6‑signalering uit, gaat het kanaal open en wordt de bipolaire cel actief, waarmee de aanwezigheid van licht wordt doorgegeven. Omdat deze wissel snel en continu moet werken gedurende het hele leven, moet de structuur van mGlu6 zowel stabiel als uiterst precies afgesteld zijn.
De receptor vastleggen net voordat hij signaleert
Met behulp van kryo‑elektronenmicroscopie bevroren de auteurs gezuiverd humaan mGlu6 gebonden aan een sterke activator, L‑serine O‑fosfaat, en reconstrueren ze zijn vorm met een resolutie van 3,2 ångström. Elk mGlu6‑molecuul vormt een paar, of dimer, bestaande uit drie op elkaar gestapelde regio’s: een grote “schelphuls” buiten de cel die glutamaat opvangt, een flexibele middenpartij rijk aan disulfidebruggen, en een zeventraps helixbundle dat het membraan overspant waar G‑eiwitten binden. De activator klemt de buitenste domeinen in een gesloten, actief‑achtige houding en brengt de middensegmenten dicht bij elkaar, terwijl de membraanahelixen verschuiven zodat een sleutelpaar helixen (genoemd TM6) nauw contact maken — kenmerken van een receptor die klaarstaat om een G‑eiwit te engageren.
Ingebouwde asymmetrie: de ene partner leidt, de andere volgt
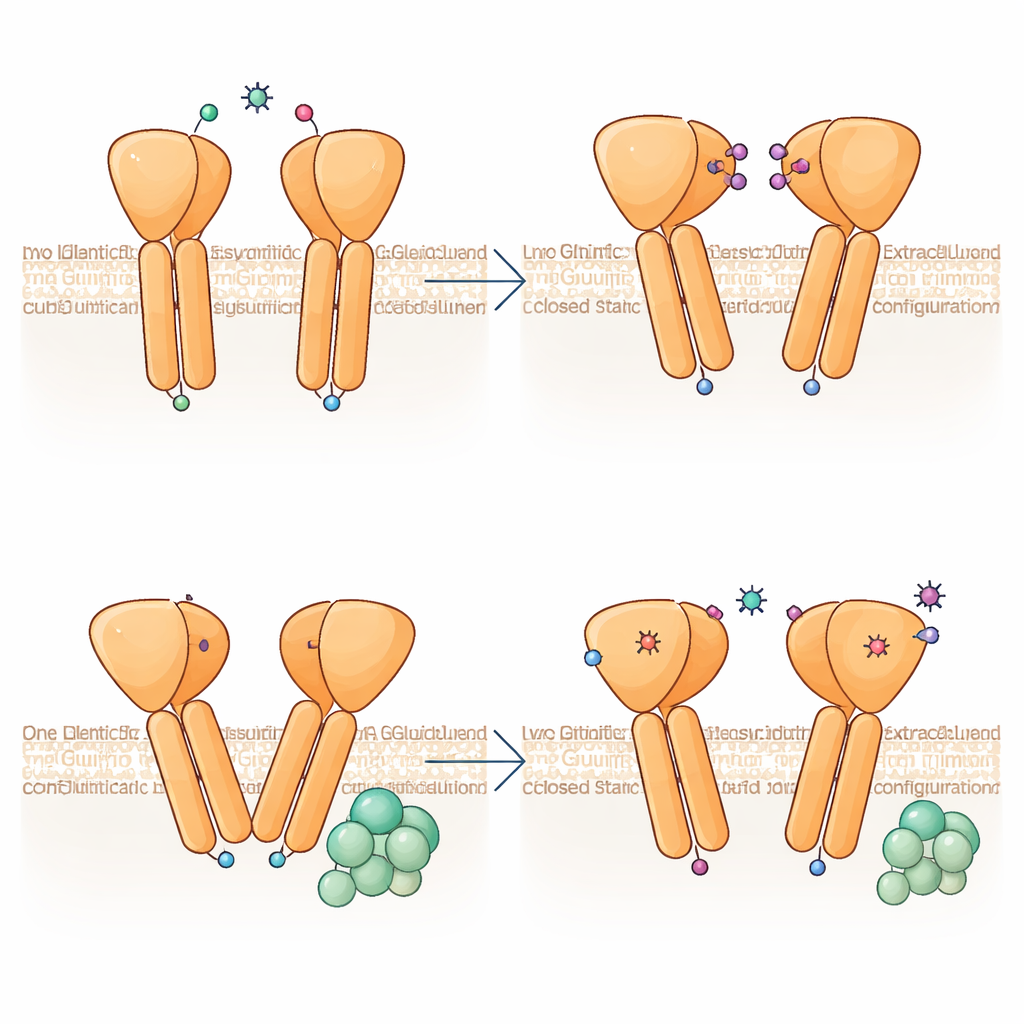
Een opvallende ontdekking is dat de twee helften van het mGlu6‑dimeer niet identieke vormen aannemen, ook al binden beide dezelfde activator. De ene subeenheid buigt scherper en zijn membraanahelixen steken iets hoger naar de buitenkant van de cel, wat een asymmetrisch oppervlak vormt waar de twee TM6‑helixen elkaar ontmoeten. Deze configuratie lijkt sterk op de G‑eiwitgebonden toestand die bij verwante receptoren wordt gezien, wat suggereert dat mGlu6 aan één kant “vooraf geprimed” is voor koppeling. Analyse van vele deeltjesbeelden toont dat het dimer een continuüm van buighoeken doorloopt, van bijna symmetrisch tot sterk asymmetrisch, wat impliceert dat de receptor dynamisch tussen toestanden schommelt, waarbij asymmetrie al ontstaat voordat een G‑eiwit arriveert.
Een verborgen ondersteunend geraamte dat signalering versnelt
Het werk onthult ook een ongebruikelijk contactvlak tussen het middengebied dat rijk is aan cysteïne en een lus aan de buitenzijde van het membraan. In mGlu6 is deze lus langer dan bij verwante receptoren en vormt ze een netwerk van zoutbruggen, waterstofbindingen en hydrofobe contacten die midden‑ en membraandomeinen stevig aan elkaar vergrendelen. Wanneer sleutelresiduen in dit interface worden gemuteerd, bereikt de receptor nog steeds het celoppervlak en kan G‑eiwitten activeren, maar doet dat langzamer, zelfs wanneer veel receptoren aanwezig zijn. Dit suggereert dat de extra contacten fungeren als een mechanische beugel die de door glutamaat geïnduceerde beweging van de buitenste “schelphuls” efficiënt doorgeeft aan de membraanhelixen, waardoor snelle reacties mogelijk zijn die nodig zijn voor real‑time zicht.
Nachtblindheid verklaren via structuur
Door elke bekende patiëntenmutatie voor congenitale stationaire nachtblindheid op de nieuwe structuur in kaart te brengen, tonen de auteurs hoe diverse veranderingen mGlu6 kunnen verlammen. Sommige mutaties vervormen het glutamaatbindend zakje of verstoren verborgen hydrofobe kernen, waardoor het buitenste domein destabiliseert; andere breken cruciale disulfidebruggen of zoutbruggen die midden‑ en membraandelen bijeengehouden, waardoor de receptor verkeerd opvouwt en er niet in slaagt het celoppervlak te bereiken. Veel varianten verminderen de efficiëntie of snelheid van G‑eiwitactivatie. Intrigerend genoeg versterken twee mutaties de signaleringscapaciteit zodra de expressie wordt genormaliseerd, maar veroorzaken waarschijnlijk toch ziekte omdat de receptoren slecht worden getransporteerd of verkeerd gepositioneerd in synapsen. Samen leggen deze bevindingen specifieke structurele defecten bloot die leiden tot gestoorde signalering, en bieden ze een moleculair stappenplan om erfelijke nachtzichtstoornissen te begrijpen en uiteindelijk te behandelen.
Bronvermelding: Lee, S.Y., Chang, CT., Yun, Y. et al. CryoEM structure of mGlu6 captures receptor activation prior to G protein coupling. Nat Commun 17, 3681 (2026). https://doi.org/10.1038/s41467-026-70436-w
Trefwoorden: nachtblindheid, retinale signalering, G-eiwit‑gekoppelde receptoren, metabotroop glutamaatreceptor, kryo-elektronenmicroscopie