Clear Sky Science · it
Struttura CryoEM di mGlu6 cattura l’attivazione del recettore prima dell’accoppiamento con la proteina G
Come i nostri occhi continuano a funzionare al buio
La visione in condizioni di scarsa illuminazione dipende da una piccola macchina molecolare nella retina che non si ferma mai. Questa macchina, un recettore chiamato mGlu6, si trova alla giunzione tra i fotorecettori a bastoncelli e le cellule nervose che inoltrano i segnali al cervello. Quando mGlu6 non funziona, le persone nascono con una condizione nota come cecità notturna stazionaria congenita: non riescono a vedere correttamente in luce fioca, pur avendo occhi dall’aspetto normale. Questo studio rivela la struttura tridimensionale di mGlu6 a dettaglio quasi atomico e spiega come il suo movimento permetta la visione notturna e come le mutazioni ereditarie interrompano quel processo.
Un guardiano indaffarato alla prima sinapsi della visione
Al buio, le cellule a bastoncelli nella retina rilasciano costantemente il messaggero chimico glutammato. Questo segnale viene catturato da mGlu6 sulla superficie delle cellule bipolari ON, che fungono da primo relay per la visione guidata dai bastoncelli. mGlu6 attivo attiva un interruttore interno—una proteina G chiamata Gαo—che mantiene chiuso un canale ionico (TRPM1) così che la cellula bipolare resti silente. Quando la luce colpisce i bastoncelli, il rilascio di glutammato cala bruscamente, il segnale di mGlu6 si spegne, il canale si apre e la cellula bipolare si attiva, segnalando la presenza della luce. Poiché questo interruttore deve funzionare rapidamente e continuamente per tutta la vita, la struttura di mGlu6 deve essere allo stesso tempo stabile e finemente sintonizzata.
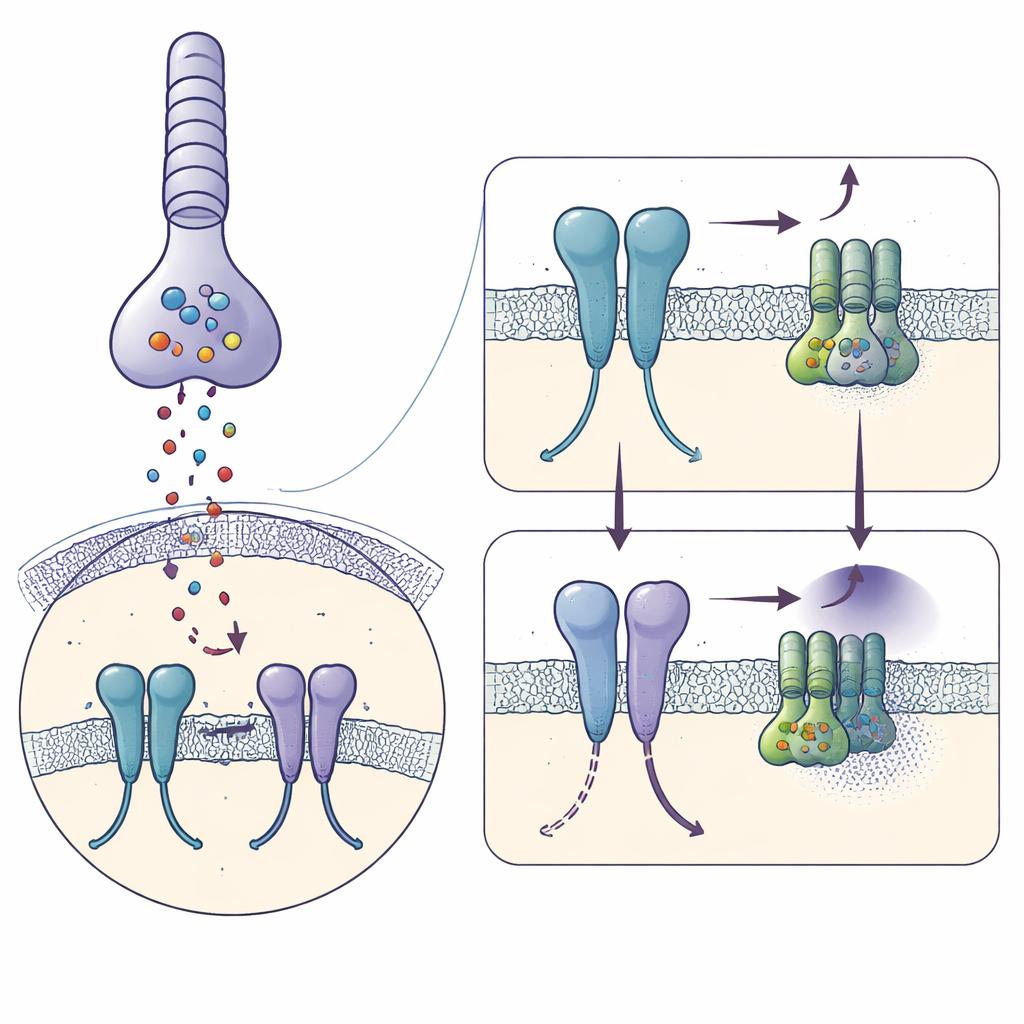
Catturare il recettore appena prima che segnali
Utilizzando la crio‑microscopia elettronica, gli autori hanno congelato mGlu6 umano purificato legato a un forte attivatore, l‑serina O‑fosfato, e hanno ricostruito la sua forma a una risoluzione di 3,2 Å. Ogni molecola di mGlu6 forma una coppia, o dima, composta da tre regioni sovrapposte: una grande “conchiglia” esterna alla cellula che cattura il glutammato, un segmento intermedio flessibile ricco di ponti disolfuro, e un fascio di sette eliche che attraversa la membrana dove si legano le proteine G. L’attivatore blocca i domini esterni in una posa chiusa, simile a quella attiva, e avvicina i segmenti intermedi, mentre le eliche transmembrana si spostano in modo che una coppia chiave di eliche (dette TM6) entri in stretto contatto—segni distintivi di un recettore pronto a interagire con una proteina G.
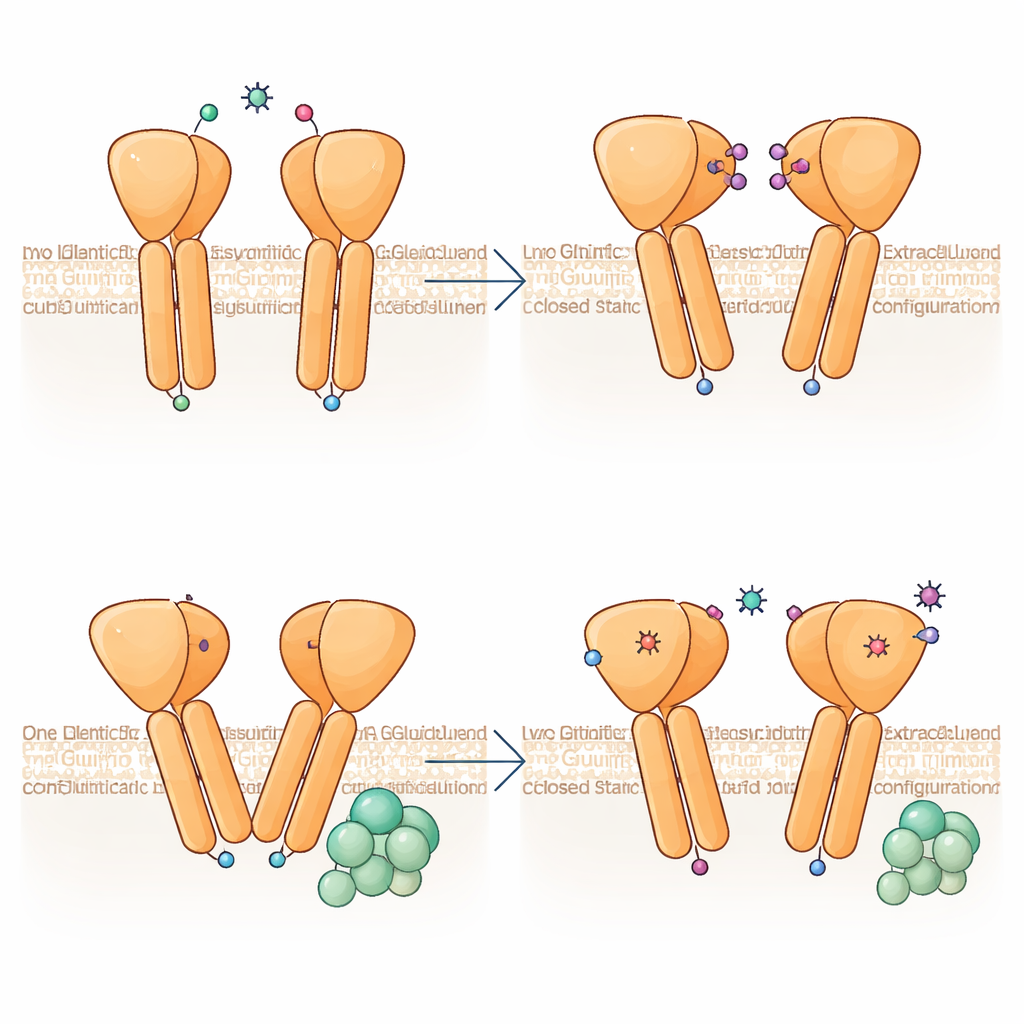
Asimmetria incorporata: un partner guida, l’altro segue
Una scoperta sorprendente è che le due metà della dima di mGlu6 non adottano forme identiche, anche se entrambe legano lo stesso attivatore. Un subunità si piega più marcatamente e le sue eliche transmembrana si sollevano leggermente verso l’esterno della cellula, producendo un’interfaccia asimmetrica dove si incontrano le due eliche TM6. Questa configurazione somiglia molto allo stato di accoppiamento con la proteina G osservato in recettori correlati, suggerendo che mGlu6 sia “pre‑preparato” per il coupling da un lato. Le analisi di molte immagini di particelle mostrano che la dima esplora un continuum di angoli di piega, da quasi simmetrici a fortemente asimmetrici, implicando che il recettore oscilli dinamicamente tra stati, con l’asimmetria che emerge già prima dell’arrivo della proteina G.
Un’impalcatura di supporto nascosta che accelera la segnalazione
Il lavoro rivela anche una superficie di contatto insolita tra la regione intermedia ricca di cisteine e una loop sul lato esterno della membrana. In mGlu6, questo loop è più lungo che nei recettori correlati e forma una rete di ponti salini, legami a idrogeno e contatti idrofobici che bloccano insieme le regioni intermedia e transmembrana. Quando residui chiave in questa interfaccia sono mutati, il recettore raggiunge comunque la superficie cellulare e può attivare le proteine G, ma lo fa più lentamente, anche in presenza di molti recettori. Ciò suggerisce che i contatti aggiuntivi fungano da staffatura meccanica che trasmette in modo efficiente il movimento indotto dal glutammato della «conchiglia» esterna fino alle eliche di membrana, permettendo risposte rapide necessarie per la visione in tempo reale.
Spiegare la cecità notturna attraverso la struttura
Mappando ogni mutazione nota di pazienti con cecità notturna stazionaria congenita sulla nuova struttura, gli autori mostrano come cambiamenti diversi possano compromettere mGlu6. Alcune mutazioni deformano la tasca di legame del glutammato o disturbano i core idrofobici sepolti, destabilizzando il dominio esterno; altre rompono ponti disolfuro cruciali o ponti salini che tengono unite le regioni intermedia e transmembrana, causando il malripiegamento del recettore e il fallimento nel raggiungere la superficie cellulare. Molte varianti riducono l’efficienza o la velocità di attivazione della proteina G. È interessante che due mutazioni aumentino effettivamente la capacità di segnalazione una volta normalizzata l’espressione, ma causano comunque la malattia probabilmente perché i recettori sono mal trasportati o mal posizionati alle sinapsi. Insieme, questi risultati collegano difetti strutturali specifici a una segnalazione compromessa, offrendo una mappa molecolare per comprendere e, in futuro, trattare i disturbi ereditari della visione notturna.
Citazione: Lee, S.Y., Chang, CT., Yun, Y. et al. CryoEM structure of mGlu6 captures receptor activation prior to G protein coupling. Nat Commun 17, 3681 (2026). https://doi.org/10.1038/s41467-026-70436-w
Parole chiave: cecità notturna, segnalazione retinica, recettori accoppiati a proteine G, recettore metabotropico del glutammato, crio microscopía elettronica