Clear Sky Science · zh
核糖核酸酶4在感觉神经元介导的神经稳态中的功能
这对长期与疼痛共处的人意味着什么
疼痛神经常被视为在受伤时发出警报的简单“传声筒”。本研究揭示,其中一些疼痛感受神经元——称为伤害感受器——也在悄然管理邻近神经纤维的健康。研究聚焦于一种较少被关注的分子,核糖核酸酶4(RNase4),并显示它既有助于维持疼痛信号的平衡,又参与受损神经的分解与重建过程。理解这一双重角色可能为治疗慢性疼痛和促进损伤后神经修复开辟新途径。
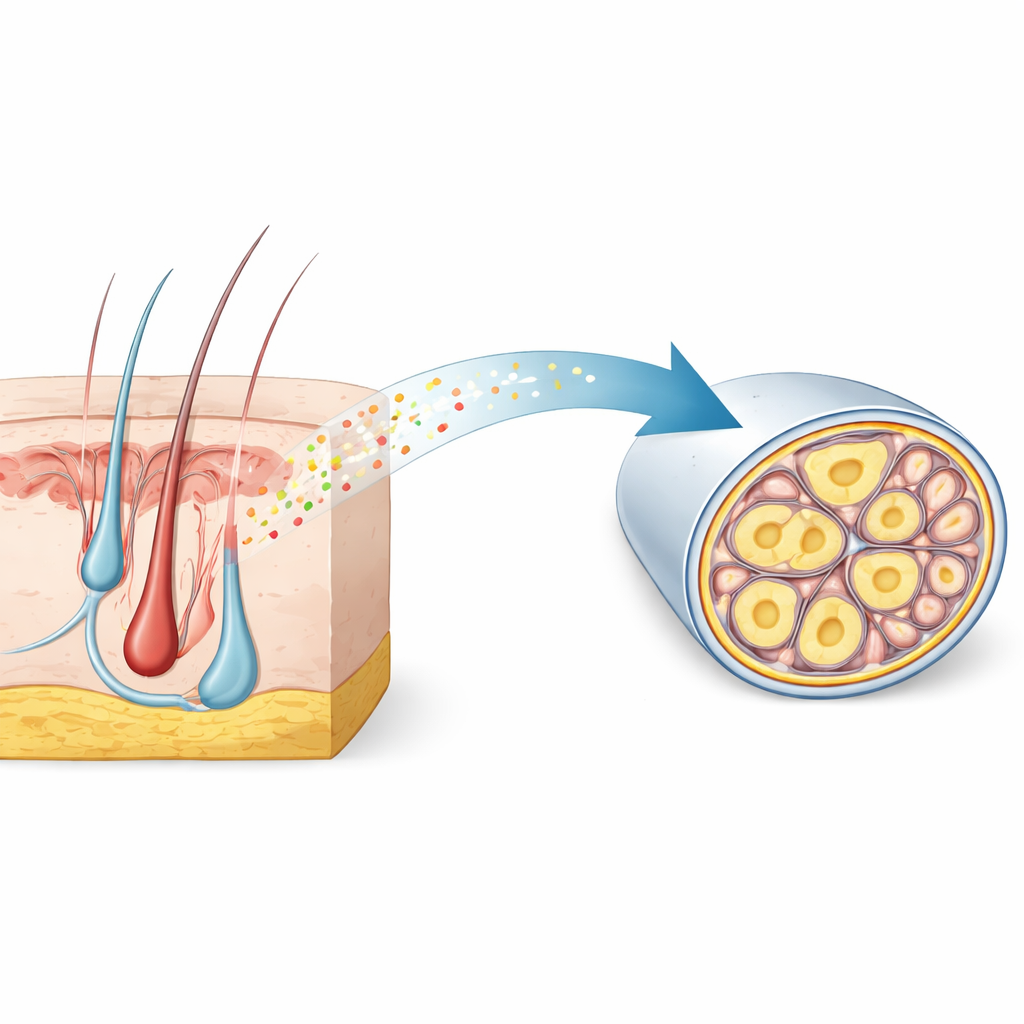
疼痛感受神经中的一种隐藏特征
研究人员首先挖掘了大型单细胞感觉节遗传图谱——这些神经节将来自身体的触觉和疼痛传递到脊髓。他们寻找在细小、无髓的伤害感受器中特异性开启的基因,这类细胞负责缓慢、隐隐的疼痛。在数千个候选基因中,RNase4脱颖而出,成为在小鼠中高度选择性的标志,并在人类组织中表现出相似分布。显微镜结果证实,RNase4主要存在于小直径、无髓的伤害感受器系谱神经元,而不出现在处理快速触觉和振动的重髓鞘神经元中。这种跨物种的保守性表明RNase4标记了一类具有共同行为学角色的专门疼痛感受细胞。
从内部塑造神经行为
为探究RNase4的作用,团队构建了可以在发育早期或仅在成体伤害感受器中删除该基因的小鼠模型。当在发育期间移除RNase4时,疼痛回路的基本连线以及对热和触觉的正常敏感性总体保持完好。然而,单细胞核RNA测序显示伤害感受器内许多基因的表达发生了变化,包括转录因子、结构蛋白以及参与设定神经元电兴奋阈值的钾通道组分。在成体小鼠中,仅在伤害感受器中关闭RNase4会引发短暂的机械性痛觉敏感性增加:动物对用丝线轻触爪垫的刺激反应更强,而对热的敏感性保持稳定。大约一个月内,这种增强的机械敏感性逐渐消退,提示其他通路会随时间补偿以恢复平衡。
向邻近细胞发出外向信号
RNase4可以被分泌到细胞外,这提示伤害感受器可能影响邻近的神经纤维和支持细胞。在细胞培养中,向类感觉神经元细胞系加入RNase4可抑制PI3K–AKT–mTOR通路的活性,该通路是一个关键的生长与存活信号枢纽。在活体小鼠中,作者采用坐骨神经压迫模型模拟外伤性神经损伤随后发生的退化与再生。损伤后,RNase4水平在许多伤害感受器亚型中自然上调,尤其在早期疼痛和恢复阶段。若伤害感受器中缺失RNase4,行为学测试显示小鼠的机械感觉恢复实际上比对照组更快,尽管热觉恢复可能根据删除策略有所滞后。这表明RNase4通常会抑制某些再生和敏感性方面,而移除它会使系统倾向于更快恢复触觉。
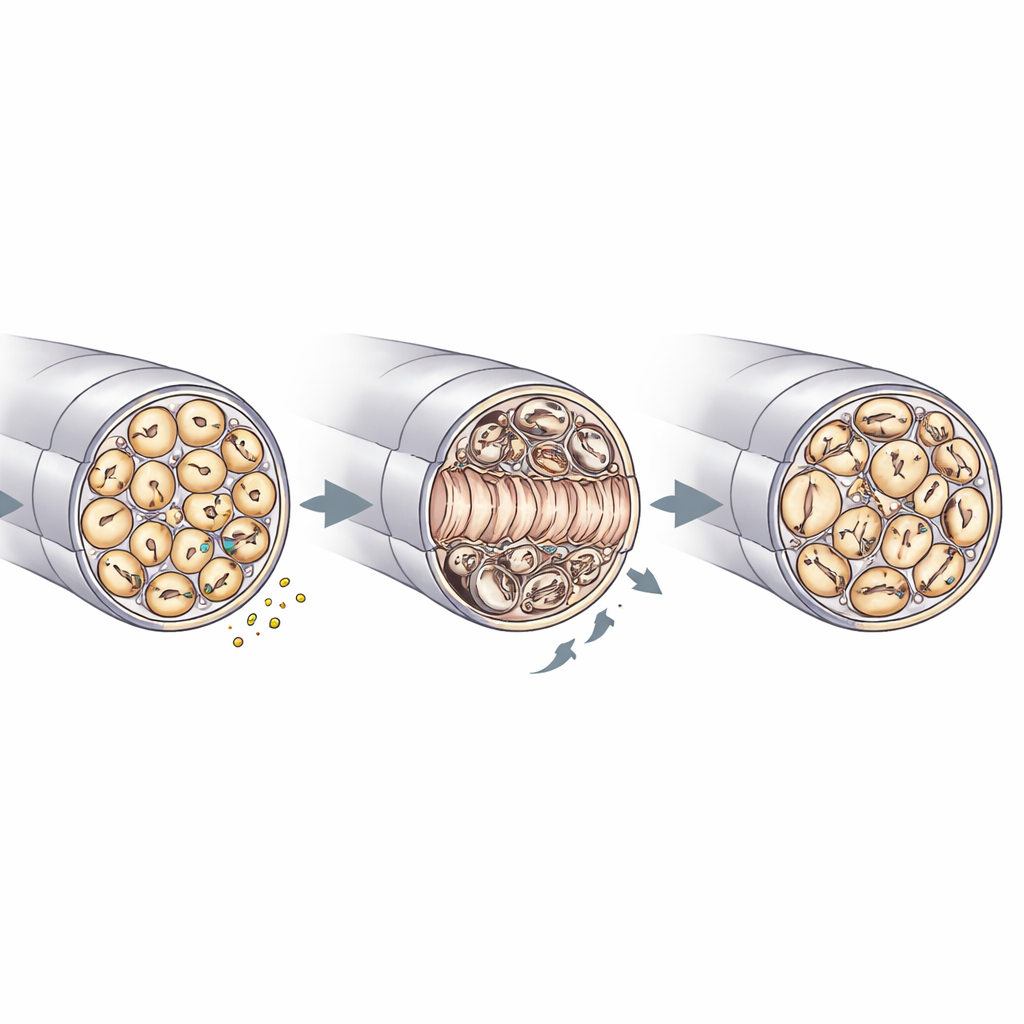
修复、髓鞘质量与神经清扫工作
对坐骨神经的电子显微镜观察提供了RNase4如何塑造神经结构的更细致视角。损伤前,敲除与对照神经在轴突直径、密度和髓鞘厚度方面相似。然在压迫损伤后,缺乏RNase4的神经在受损段显示更多再生轴突,并且无髓“Remak”束——容纳许多细纤维的结构——的再充填更快。同时,这些敲除神经表现出更多髓鞘不规则性,如折叠、内陷和局部增厚,并显示施旺细胞的应激迹象;免疫细胞内的髓鞘残骸也更少,符合更高效的清除和更快的结构重建。结合信号通路研究,这些发现支持一种模型:来自伤害感受器的RNase4调节PI3K–AKT活性,并通过非局部效应协调轴突的再生、髓鞘的重塑及免疫细胞参与的清理过程。
这对未来治疗意味着什么
简单来说,这项研究把伤害感受器描绘成不仅是警报器,还是局部的神经健康管理者。RNase4既是分子制动器也是引导者:在伤害感受器内,它有助于维持正常的放电特性和细胞身份;在细胞外,它限制过度的再生并塑造损伤后髓鞘与支持细胞的反应。移除RNase4可以加速损伤后触觉的恢复,但代价是更多髓鞘缺陷和改变的疼痛敏感性。任何旨在阻断或增强RNase4活性的疗法都需要在这些利弊间找到平衡。不过,该工作仍将RNase4及其信号网络作为同时调控疼痛与促进更有序神经修复的有前景的目标。
引用: Feng, X., Zhang, K., Techameena, P. et al. Ribonuclease 4 Functions in Nociceptor-Mediated Nerve Homeostasis. Nat Commun 17, 2862 (2026). https://doi.org/10.1038/s41467-026-70365-8
关键词: 伤害感受器, 神经再生, 髓鞘, 神经病理性疼痛, RNase4