Clear Sky Science · pl
Ribonukleaza 4 pełni funkcje w homeostazie nerwów zależnej od nocyceptorów
Dlaczego ma to znaczenie dla osób żyjących z bólem
Nerwy przewodzące ból często przedstawia się jako proste przekaźniki, które alarmują, gdy coś boli. To badanie pokazuje, że niektóre z tych neuronów czuciowych, zwane nocyceptorami, dyskretnie dbają również o stan pobliskich włókien nerwowych. Praca koncentruje się na mało znanej cząsteczce, ribonukleazie 4 (RNase4), i wykazuje, że pomaga ona utrzymać równowagę sygnałów bólowych, a także wpływa na sposób, w jaki uszkodzone nerwy ulegają degradacji i odbudowie. Zrozumienie tej podwójnej roli może otworzyć nowe drogi leczenia przewlekłego bólu i poprawy naprawy nerwów po urazie.
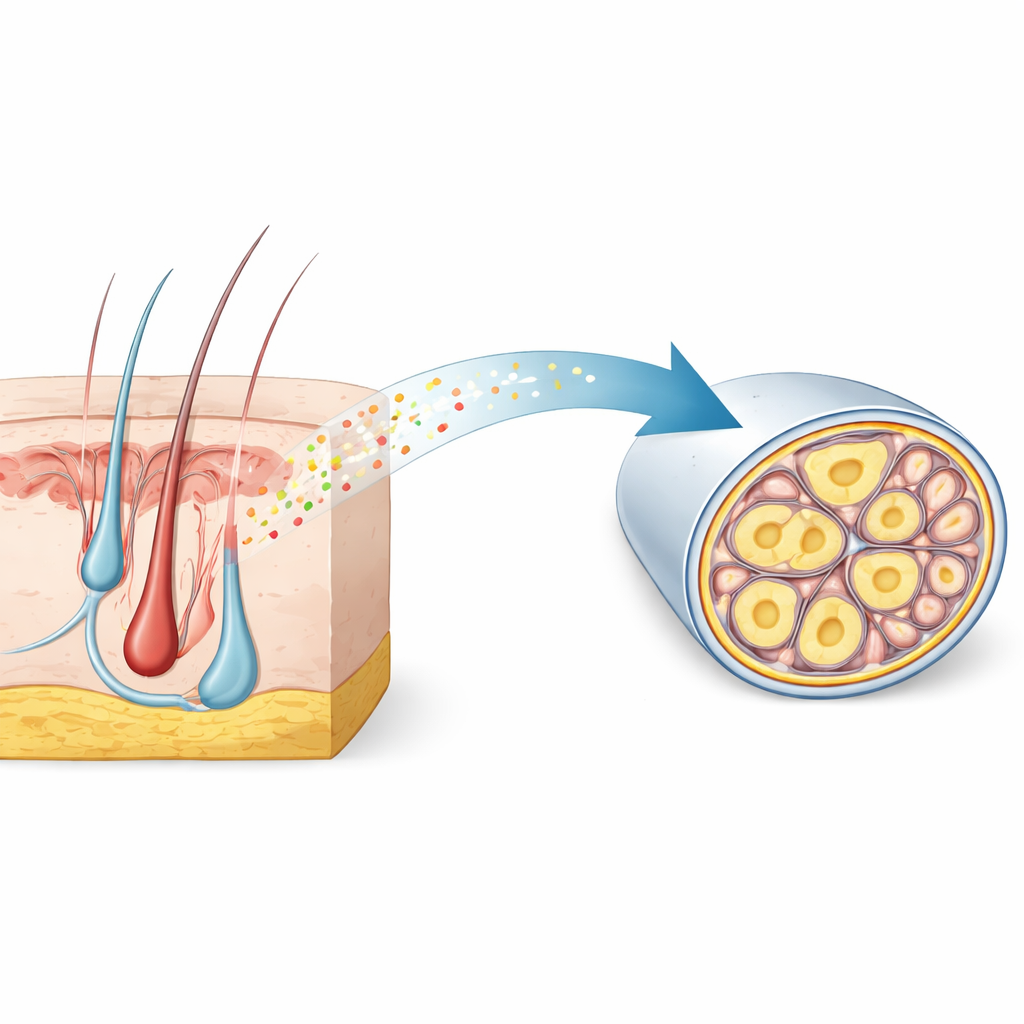
Ukryty znak wewnątrz nerwów czujących ból
Naukowcy zaczęli od analizy dużych pojedynczych atlazów genetycznych zwojów czuciowych — skupisk neuronów przekazujących dotyk i ból z ciała do rdzenia kręgowego. Szukali genów aktywnych specyficznie w cienkich, niemielinowanych nocyceptorach, które przenoszą powolny, tępy ból. Spośród tysięcy kandydatów RNase4 wyróżniała się jako wysoce selektywny marker u myszy i wykazywała podobny wzorzec w tkance ludzkiej. Mikroskopia potwierdziła, że RNase4 występuje głównie w neuronach o małej średnicy, niemielinowanych, należących do linii nocyceptorów, a nie w silnie mielinowanych neuronach obsługujących szybki dotyk i wibracje. Zachowanie tego wzorca między gatunkami sugeruje, że RNase4 oznacza wyspecjalizowaną podpopulację komórek czujących ból o wspólnej roli biologicznej.
Modelowanie zachowania nerwu od wewnątrz
Aby zbadać funkcję RNase4, zespół skonstruował myszy, u których gen można było usunąć albo wcześnie podczas rozwoju, albo jedynie w dorosłych nocyceptorach. Gdy RNase4 usunięto w trakcie rozwoju, podstawowe okablowanie obwodowych obwodów bólowych oraz normalna wrażliwość na ciepło i dotyk pozostały w dużej mierze nienaruszone. Jednak analiza RNA pojedynczych jąder komórkowych wykazała, że w nocyceptorach zmieniła się aktywność wielu genów, w tym czynników transkrypcyjnych, białek strukturalnych i elementów kanałów potasowych, które pomagają ustalać próg pobudliwości neuronów. U dorosłych myszy wyłączenie RNase4 jedynie w nocyceptorach wywołało chwilowy wzrost wrażliwości na bodźce mechaniczne: zwierzęta reagowały silniej na lekki dotyk przy użyciu włókienek aplikowanych na łapę, podczas gdy wrażliwość na ciepło pozostała stabilna. W ciągu około miesiąca nasilona wrażliwość mechaniczna ustępowała, co sugeruje, że z czasem inne szlaki rekompensują zmianę i przywracają równowagę.
Wysyłanie sygnałów na zewnątrz do komórek sąsiednich
RNase4 może być wydzielana poza komórkę, co daje możliwość, że nocyceptory wpływają na pobliskie włókna nerwowe i komórki wspierające. W hodowli komórek dodanie RNase4 do linii przypominającej neurony czuciowe osłabiło aktywność szlaku PI3K–AKT–mTOR, centralnego węzła sygnałowego sterującego wzrostem i przeżyciem. W żywych myszach autorzy zastosowali model miażdżenia nerwu kulszowego, który naśladuje uraz nerwu z następującą degeneracją i regeneracją. Po urazie poziomy RNase4 naturalnie wzrastały w wielu podtypach nocyceptorów, zwłaszcza we wczesnych fazach bólu i regeneracji. Gdy RNase4 brakowało w nocyceptorach, testy behawioralne wykazały, że myszy odzyskiwały czucie mechaniczne szybciej niż kontrolne, chociaż regeneracja temperaturowa mogła się opóźniać w zależności od strategii usunięcia genu. Sugeruje to, że RNase4 normalnie hamuje pewne aspekty odrostu i wrażliwości, a jego usunięcie przesuwa równowagę w kierunku szybszego powrotu czucia dotykowego.
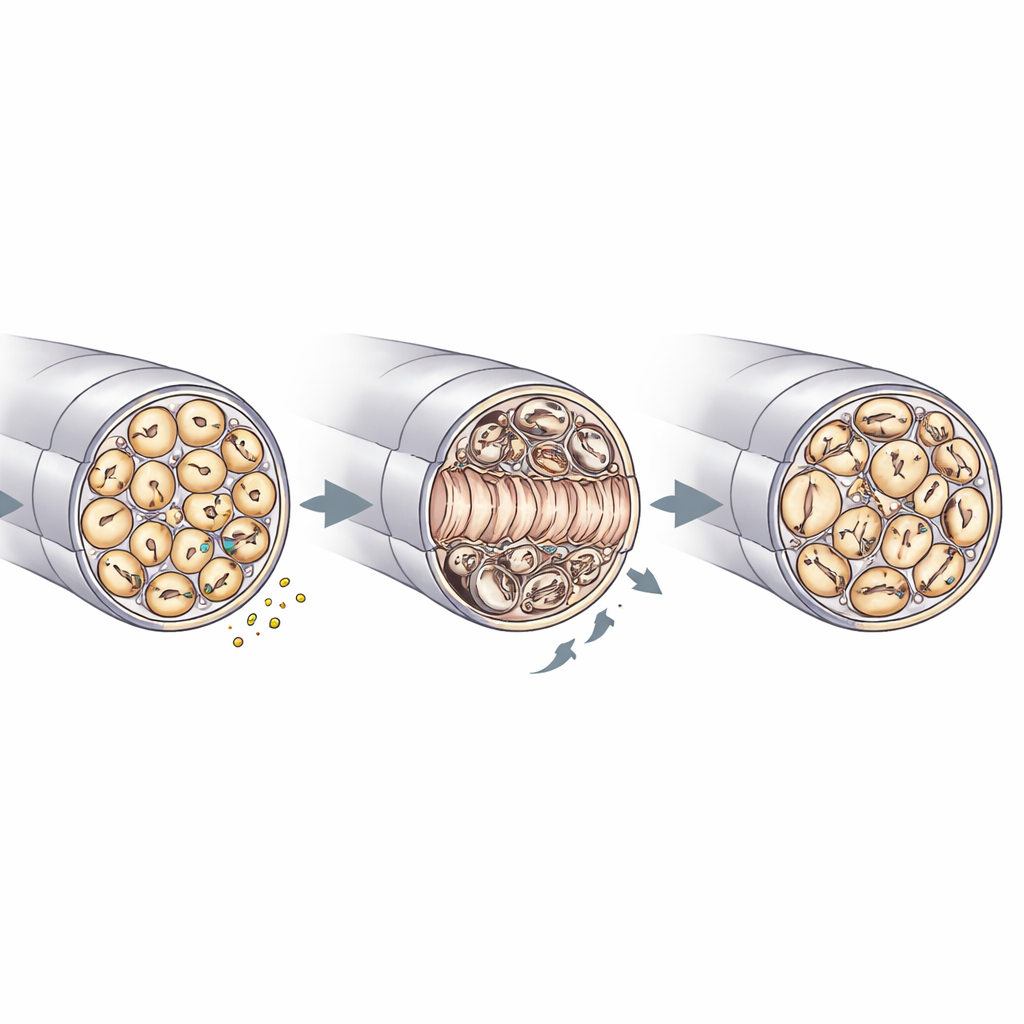
Naprawa, jakość mieliny i porządki w nerwie
Mikroskopia elektronowa nerwów kulszowych pozwoliła przyjrzeć się bliżej, jak RNase4 kształtuje architekturę nerwów. Przed urazem nerwy typu knockout i kontrolne wyglądały podobnie, z porównywalnymi średnicami aksonów, gęstościami i grubością osłonek mielinowych. Po urazie jednak nerwy pozbawione RNase4 zawierały więcej zregenerowanych aksonów w uszkodzonym odcinku i wykazywały szybsze ponowne wypełnianie niemielinowanych pęczków typu "Remak", które mieszczą wiele cienkich włókien. Jednocześnie te nerwy knockout wykazywały więcej nieregularności mieliny — takich jak fałdy, wpuklenia i ogniskowe pogrubienia — oraz oznaki stresu w komórkach Schwanna, glejowych komórkach osłaniających aksony. Odnotowano również mniej resztek mieliny wewnątrz komórek układu odpornościowego, co zgadza się z bardziej efektywnym usuwaniem odpadów i szybszą odbudową strukturalną. W połączeniu z badaniami sygnałowymi te obserwacje wspierają model, w którym RNase4 pochodząca z nocyceptorów strojkuje aktywność PI3K–AKT i poprzez efekty poza komórkowe koordynuje, jak aksony odrastają, jak przebudowywana jest mielina i jak komórki odpornościowe biorą udział w sprzątaniu.
Co to oznacza dla przyszłych terapii
Mówiąc prostymi słowami, badanie przedstawia nocyceptory nie tylko jako gongi alarmowe, lecz jako lokalnych menedżerów zdrowia nerwów. RNase4 działa jak molekularny hamulec i przewodnik: wewnątrz nocyceptorów pomaga utrzymać ich normalne właściwości pobudzeniowe i tożsamość; na zewnątrz ogranicza nadmierny odrost i kształtuje reakcję mieliny oraz komórek wspierających po urazie. Usunięcie RNase4 może przyspieszyć powrót czucia dotykowego po uszkodzeniu nerwu, ale kosztem większej liczby defektów mieliny i zmienionej wrażliwości bólowej. Każda terapia mająca na celu zablokowanie lub wzmocnienie RNase4 będzie musiała wyważyć te kompromisy. Mimo to praca wskazuje RNase4 i jego sieć sygnałową jako obiecujące dźwignie do jednoczesnego modulowania bólu i wspierania bardziej uporządkowanej naprawy nerwów.
Cytowanie: Feng, X., Zhang, K., Techameena, P. et al. Ribonuclease 4 Functions in Nociceptor-Mediated Nerve Homeostasis. Nat Commun 17, 2862 (2026). https://doi.org/10.1038/s41467-026-70365-8
Słowa kluczowe: nocyceptory, regeneracja nerwów, mielina, ból neuropatyczny, RNase4