Clear Sky Science · ar
وظائف ريبونوكلياز 4 في الحفاظ على موصلية الأعصاب الحسية للألم
لماذا يهم هذا الأشخاص الذين يعيشون مع الألم
غالبًا ما تُصوَّر أعصاب الألم كرسائل بسيطة تصرخ عند حدوث ضرر. تكشف هذه الدراسة أن بعض الخلايا العصبية الحساسة للألم، المسماة المستقبلات المؤلمة، تدير بهدوء صحة الألياف العصبية المجاورة أيضًا. يركز العمل على جزيء قليل المعرفة، ريبونوكلياز 4 (RNase4)، ويبيّن أنه يساعد على ضبط إشارات الألم بينما يوجّه أيضًا كيف تتحطم الأعصاب المتضررة وتُعيد بناء نفسها. فهم هذا الدور المزدوج قد يفتح طرقًا جديدة لعلاج الألم المزمن وتحسين إصلاح الأعصاب بعد الإصابات.
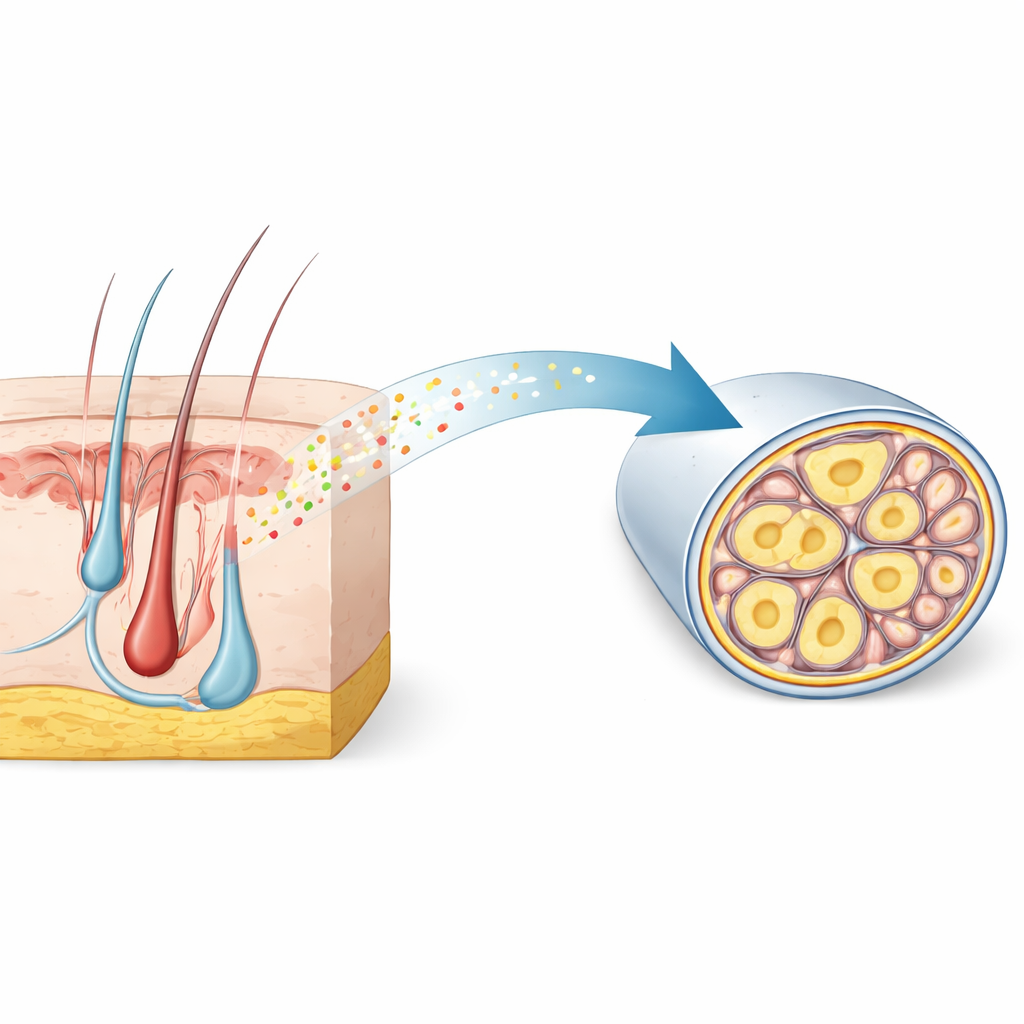
بصمة مخفية داخل أعصاب الإحساس بالألم
بدأ الباحثون بتعدين خرائط جينية أحادية الخلية كبيرة للعناقيد الحسية—مجموعات الخلايا العصبية التي تنقل اللمس والألم من الجسم إلى النخاع الشوكي. بحثوا عن جينات تُشغّل خصيصًا في المستقبلات المؤلمة الرفيعة غير المغلفة بالمايلين، التي تنقل الألم البطيء والآلام المستمرة. من بين آلاف المرشحين، برز RNase4 كعلامة انتقائية للغاية في الفئران وأظهر نمطًا مماثلاً في الأنسجة البشرية. أكدت الميكروسكوبية أن RNase4 يوجد أساسًا في الخلايا العصبية ذات القُطر الصغير غير المغلفة التي تنتمي إلى سلالة المستقبلات المؤلمة، لكنه غير موجود في الخلايا العصبية المغلفة بكثافة بالمايلين التي تتعامل مع اللمس والذبذبة السريعة. هذا الحفظ عبر الأنواع يوحي بأن RNase4 يميّز مجموعة متخصصة من خلايا الإحساس بالألم ذات دور بيولوجي مشترك.
تشكيل سلوك العصب من الداخل
للبحث في وظيفة RNase4، صنع الفريق فئرانًا معدّلة يمكن حذف الجين فيها إما مبكرًا أثناء التطور أو فقط في المستقبلات المؤلمة لدى البالغين. عندما أُزيل RNase4 أثناء التطور، بقيت الدوائر الأساسية للألم والحس بحرارة ولمس طبيعية إلى حد كبير. مع ذلك، كشف تسلسل RNA النووي أحادي النواة أن العديد من الجينات غيّرت نشاطها داخل المستقبلات المؤلمة، بما في ذلك عوامل النسخ، وبروتينات الهيكل، ومكونات قنوات البوتاسيوم التي تساعد على تحديد عتبة إثارة الخلايا العصبية كهربائيًا. في الفئران البالغة، أدى إيقاف RNase4 فقط في المستقبلات المؤلمة إلى زيادة مؤقتة في الحساسية الميكانيكية: تفاعلت الحيوانات بقوة أكبر مع اللمسات الخفيفة بواسطة خيوط مطبقة على الكف، بينما بقي الحس للحرارة مستقرًا. على مدى نحو شهر، تلاشت هذه الحساسية الميكانيكية المرتفعة، مما يوحي بأن مسارات أخرى تعوّض مع الوقت لاستعادة التوازن.
إرسال إشارات إلى الخلايا المجاورة
يمكن إفراز RNase4 خارج الخلية، مما يطرح احتمال أن المستقبلات المؤلمة تؤثر على الألياف العصبية المجاورة وخلايا الدعم. في مزارع الخلايا، قلّلت إضافة RNase4 إلى سلالة تشبه الخلايا العصبية الحسية من نشاط مسار PI3K–AKT–mTOR، وهو محور مركزي لإشارات النمو والبقاء. في الفئران الحية، استخدم المؤلفون نموذج سحق العصب الوركي الذي يحاكي إصابة عصبية صادمة يتبعها تراجع وإعادة نمو. بعد الإصابة، ارتفعت مستويات RNase4 طبيعيًا عبر العديد من أنواع المستقبلات المؤلمة، خصوصًا خلال مراحل الألم والانتعاش المبكرة. عندما كان RNase4 غائبًا من المستقبلات المؤلمة، أظهرت الاختبارات السلوكية أن الفئران استعادت الإحساس الميكانيكي أسرع من الضوابط، رغم أن التعافي الحراري قد يتأخر اعتمادًا على استراتيجية الحذف. هذا يوحي أن RNase4 عادةً يكبح جوانب معينة من إعادة النمو والحساسية، وأن إزالته تميل بالنظام نحو استعادة لمسية أسرع.
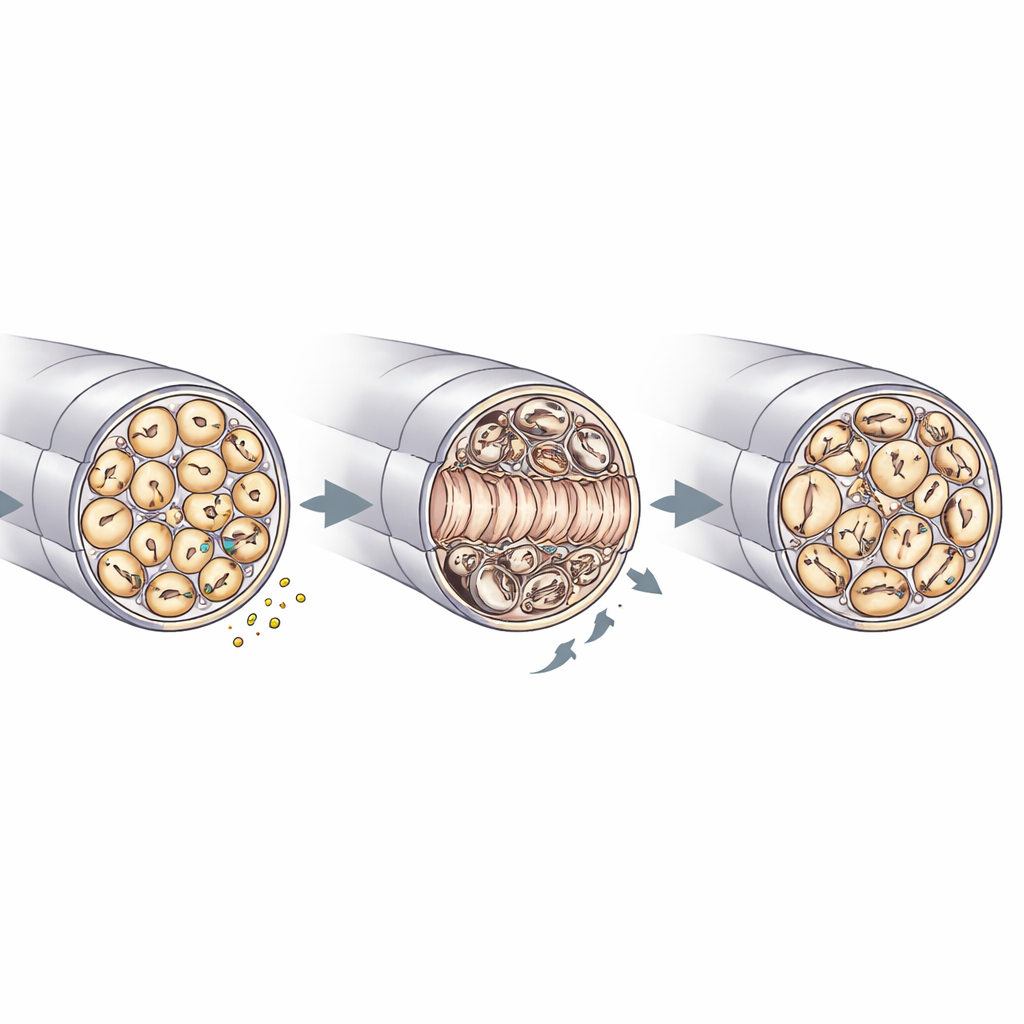
الإصلاح، جودة المايلين، وصيانة الأعصاب
قدمت المجهر الإلكتروني نظرة مقربة على كيفية تشكيل RNase4 لبنية الأعصاب. قبل الإصابة، بدا أن الأعصاب في الفئران المعدّلة والمقصورة مماثلة، مع أقطار ومحاور وكثافات وسمك مايلين متقاربة. بعد إصابة السحق، مع ذلك، احتوت الأعصاب الخالية من RNase4 على محاور متجددة أكثر في الجزء التالف وأظهرت تعبئة أسرع لحزم "ريماك" غير المغلفة التي تحتضن العديد من الألياف الرقيقة. في الوقت نفسه، أظهرت هذه الأعصاب المعدّلة مزيدًا من عدم انتظامات المايلين—مثل الطيات، والانطباعات، والتثخن البؤري—وعلامات إجهاد في خلايا شوان، وهي الخلايا الدبقية التي تغلف المحاور. كما كان هناك حطام مايلين أقل داخل الخلايا المناعية، وهو ما يتوافق مع إزالة أكثر كفاءة وإعادة بناء هيكلية أسرع. إلى جانب دراسات الإشارة، تدعم هذه النتائج نموذجًا ترى أن RNase4 المشتق من المستقبلات المؤلمة يضبط نشاط PI3K–AKT ومن خلال تأثيرات غير محلية ينسق كيفية إعادة نمو المحاور، وإعادة تشكيل المايلين، ومشاركة الخلايا المناعية في التنظيف.
ماذا يعني هذا للعلاجات المستقبلية
بعبارات بسيطة، تصوّر الدراسة المستقبلات المؤلمة ليس فقط كأجراس إنذار بل كمديرين محليين لصحة الأعصاب. يعمل RNase4 كمكبح وجهاز توجيه جزيئي: داخل المستقبلات المؤلمة، يساعد على الحفاظ على خصائص إطلاقها الكهربائية وهويتها؛ وخارجها، يحد من إعادة النمو المفرطة ويشكّل كيفية استجابة المايلين وخلايا الدعم بعد الإصابة. قد تُسرّع إزالة RNase4 عودة الإحساس باللمس بعد تلف العصب لكنها تأتي بتكلفة مزيد من عيوب المايلين وتغيرات في حساسية الألم. أي علاج يستهدف حجب أو تعزيز RNase4 سيحتاج إلى موازنة هذه المقايضات. ومع ذلك، يبرز العمل RNase4 وشبكة إشاراته كأذرع واعدة للتأثير على الألم وتعزيز إصلاح أعصاب أكثر انتظامًا في آن واحد.
الاستشهاد: Feng, X., Zhang, K., Techameena, P. et al. Ribonuclease 4 Functions in Nociceptor-Mediated Nerve Homeostasis. Nat Commun 17, 2862 (2026). https://doi.org/10.1038/s41467-026-70365-8
الكلمات المفتاحية: المستقبلات المؤلمة, تجدد الأعصاب, المايلين, الألم الاعتلالي العصبي, RNase4