Clear Sky Science · fr
La ribonucléase 4 intervient dans l’homéostasie nerveuse médiée par les nocicepteurs
Pourquoi cela compte pour les personnes vivant avec la douleur
Les nerfs de la douleur sont souvent présentés comme de simples messagers qui avertissent quand quelque chose fait mal. Cette étude montre que certains de ces neurones détecteurs de douleur, appelés nocicepteurs, gèrent discrètement aussi la santé des fibres nerveuses voisines. Le travail se concentre sur une molécule peu connue, la ribonucléase 4 (RNase4), et montre qu’elle aide à maintenir les signaux douloureux sous contrôle tout en guidant la dégradation et la reconstruction des nerfs blessés. Comprendre ce double rôle pourrait ouvrir de nouvelles voies pour traiter la douleur chronique et améliorer la réparation nerveuse après une lésion.
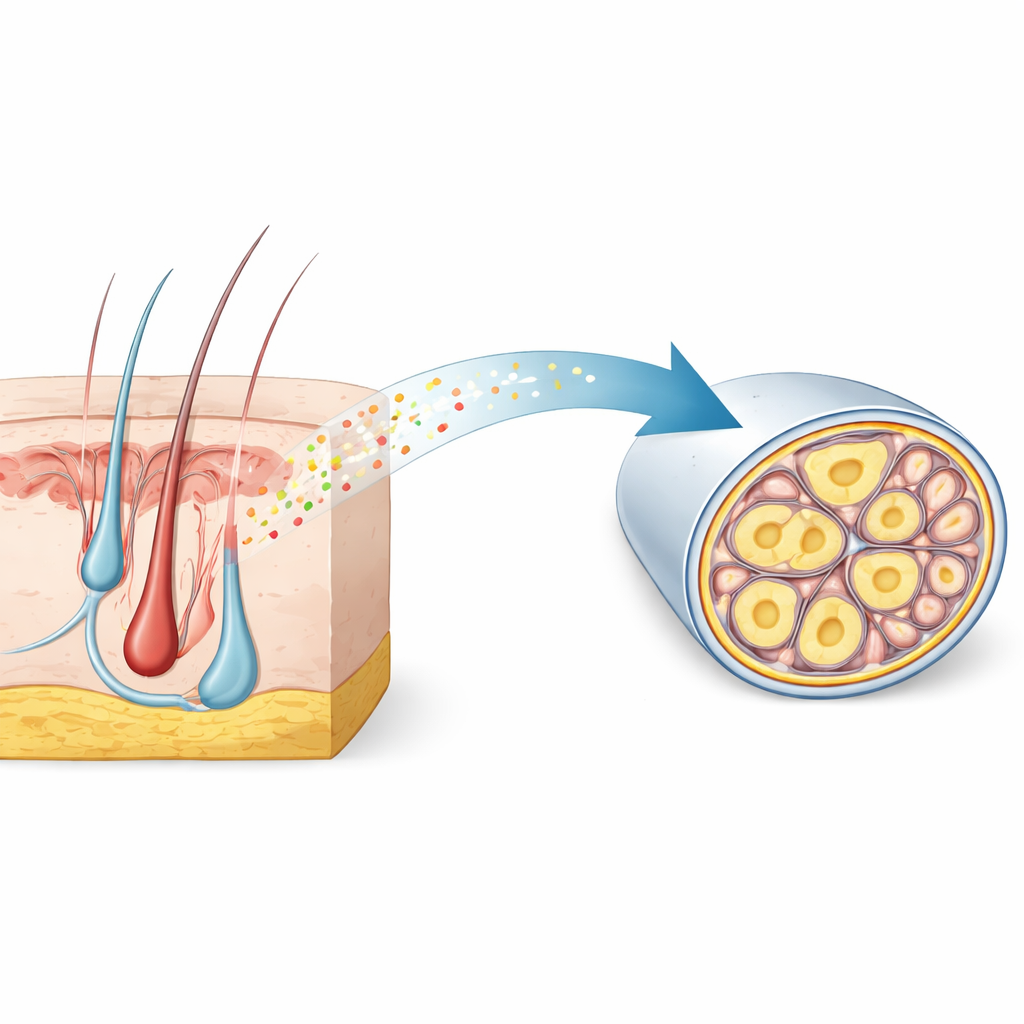
Une signature cachée au sein des neurones sensibles à la douleur
Les chercheurs ont commencé par exploiter de grands atlas génétiques unicellulaires des ganglions sensoriels — des amas de neurones qui relayent le toucher et la douleur du corps vers la moelle épinière. Ils ont cherché des gènes exprimés spécifiquement dans les nocicepteurs fins et non myélinisés, qui véhiculent la douleur lente et sourde. Parmi des milliers de candidats, RNase4 s’est distinguée comme un marqueur fortement sélectif chez la souris et présentait un profil correspondant dans les tissus humains. La microscopie a confirmé que RNase4 se trouve principalement dans des neurones de petit diamètre, non myélinisés, appartenant à la lignée des nocicepteurs, mais pas dans les neurones fortement myélinisés qui traitent le toucher et les vibrations rapides. Cette conservation entre espèces suggère que RNase4 marque un sous-ensemble spécialisé de cellules détectrices de la douleur partageant un rôle biologique commun.
Façonner le comportement nerveux de l’intérieur
Pour étudier la fonction de RNase4, l’équipe a conçu des souris dans lesquelles le gène pouvait être supprimé soit tôt au cours du développement, soit uniquement chez les nocicepteurs adultes. Quand RNase4 a été supprimée pendant le développement, l’architecture de base des circuits de la douleur et la sensibilité normale à la chaleur et au toucher restaient globalement intactes. Cependant, le séquençage d’ARN nucléaire à cellule unique a révélé que de nombreux gènes changeaient d’activité au sein des nocicepteurs, notamment des facteurs de transcription, des protéines structurales et des composantes de canaux potassiques qui contribuent à fixer le seuil d’excitabilité électrique des neurones. Chez les souris adultes, l’extinction de RNase4 uniquement dans les nocicepteurs a déclenché une augmentation temporaire de la sensibilité mécanique : les animaux réagissaient plus fortement à un toucher léger appliqué sur la patte, tandis que la sensibilité à la chaleur restait stable. Sur environ un mois, cette sensibilité mécanique accrue s’est atténuée, ce qui suggère que d’autres voies compensent progressivement pour rétablir l’équilibre.
Envoyer des signaux vers les cellules voisines
RNase4 peut être sécrétée à l’extérieur de la cellule, ce qui ouvre la possibilité que les nocicepteurs influencent les fibres nerveuses et les cellules de soutien voisines. En culture cellulaire, l’ajout de RNase4 à une lignée semblable à des neurones sensoriels a atténué l’activité de la voie PI3K–AKT–mTOR, un nœud central de signalisation de croissance et de survie. Chez la souris vivante, les auteurs ont ensuite utilisé un modèle d’écrasement du nerf sciatique, qui imite une lésion nerveuse traumatique suivie de dégénérescence et de repousse. Après la blessure, les niveaux de RNase4 augmentaient naturellement dans de nombreux sous-types de nocicepteurs, en particulier pendant les phases précoces de douleur et de récupération. Lorsque RNase4 faisait défaut dans les nocicepteurs, les tests comportementaux ont montré que les souris retrouvaient en fait la sensation mécanique plus rapidement que les témoins, bien que la récupération thermique puisse être retardée selon la stratégie de suppression. Cela suggère que RNase4 freine normalement certains aspects de la repousse et de la sensibilité, et que son absence favorise une récupération tactile plus rapide.
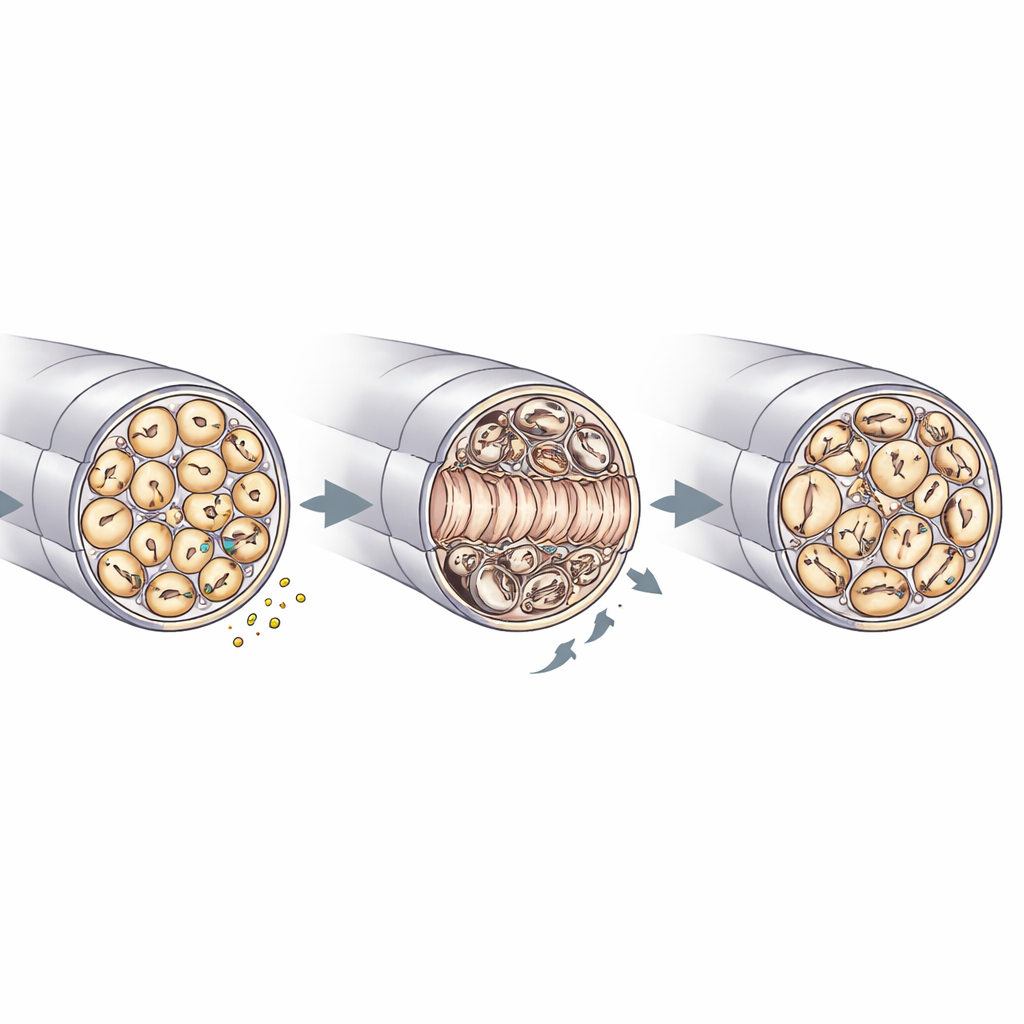
Réparation, qualité de la myéline et entretien des nerfs
La microscopie électronique du nerf sciatique a permis d’examiner de plus près comment RNase4 façonne l’architecture nerveuse. Avant la lésion, les nerfs des animaux knock-out et des témoins se ressemblaient, avec des diamètres d’axone, des densités et des épaisseurs de myéline comparables. Après l’écrasement, cependant, les nerfs dépourvus de RNase4 contenaient plus d’axones régénérés dans le segment endommagé et montraient un comblement plus rapide des faisceaux non myélinisés « Remak » qui abritent de nombreuses fibres fines. Parallèlement, ces nerfs knock-out présentaient davantage d’irrégularités de la myéline — telles que plis, invaginations et épaississements focaux — et des signes de stress dans les cellules de Schwann, les cellules gliales qui entourent les axones. On observait aussi moins de débris de myéline à l’intérieur des cellules immunitaires, cohérent avec un nettoyage plus efficace et une reconstruction structurelle plus rapide. Avec les études de signalisation, ces résultats soutiennent un modèle dans lequel la RNase4 dérivée des nocicepteurs module l’activité de PI3K–AKT et, par des effets non locaux, coordonne la repousse axonale, le remodelage de la myéline et la participation des cellules immunitaires au nettoyage.
Ce que cela implique pour les traitements futurs
En clair, l’étude présente les nocicepteurs non seulement comme des systèmes d’alarme mais comme des gestionnaires locaux de la santé nerveuse. RNase4 agit comme un frein et un guide moléculaires : à l’intérieur des nocicepteurs, elle aide à maintenir leurs propriétés d’excitabilité et leur identité ; à l’extérieur, elle limite la repousse excessive et influence la réponse de la myéline et des cellules de soutien après une lésion. La suppression de RNase4 peut accélérer le retour du toucher après une lésion nerveuse, mais au prix de plus de défauts de myéline et d’une sensibilité à la douleur altérée. Toute thérapie visant à bloquer ou stimuler RNase4 devra donc équilibrer ces compromis. Néanmoins, ce travail met en lumière RNase4 et son réseau de signalisation comme des leviers prometteurs pour moduler simultanément la douleur et favoriser une réparation nerveuse plus ordonnée.
Citation: Feng, X., Zhang, K., Techameena, P. et al. Ribonuclease 4 Functions in Nociceptor-Mediated Nerve Homeostasis. Nat Commun 17, 2862 (2026). https://doi.org/10.1038/s41467-026-70365-8
Mots-clés: nocicepteurs, régénération nerveuse, myéline, douleur neuropathique, RNase4