Clear Sky Science · nl
Ribonuclease 4 speelt een rol in door nociceptoren gereguleerde zenuwhomeostase
Waarom dit belangrijk is voor mensen die met pijn leven
Pijnzenuwen worden vaak afgeschilderd als simpele boodschappers die lawaai maken wanneer iets pijn doet. Deze studie laat zien dat sommige van die pijngevoelige neuronen, nociceptoren genoemd, stilletjes ook de gezondheid van nabije zenuwvezels beheren. Het werk richt zich op een weinig bekende molecule, ribonuclease 4 (RNase4), en toont aan dat deze helpt pijnsignalen te reguleren en tegelijk beïnvloedt hoe beschadigde zenuwen afbreken en zich weer opbouwen. Inzicht in deze dubbele rol kan nieuwe wegen openen voor de behandeling van chronische pijn en het verbeteren van zenuwherstel na letsel.
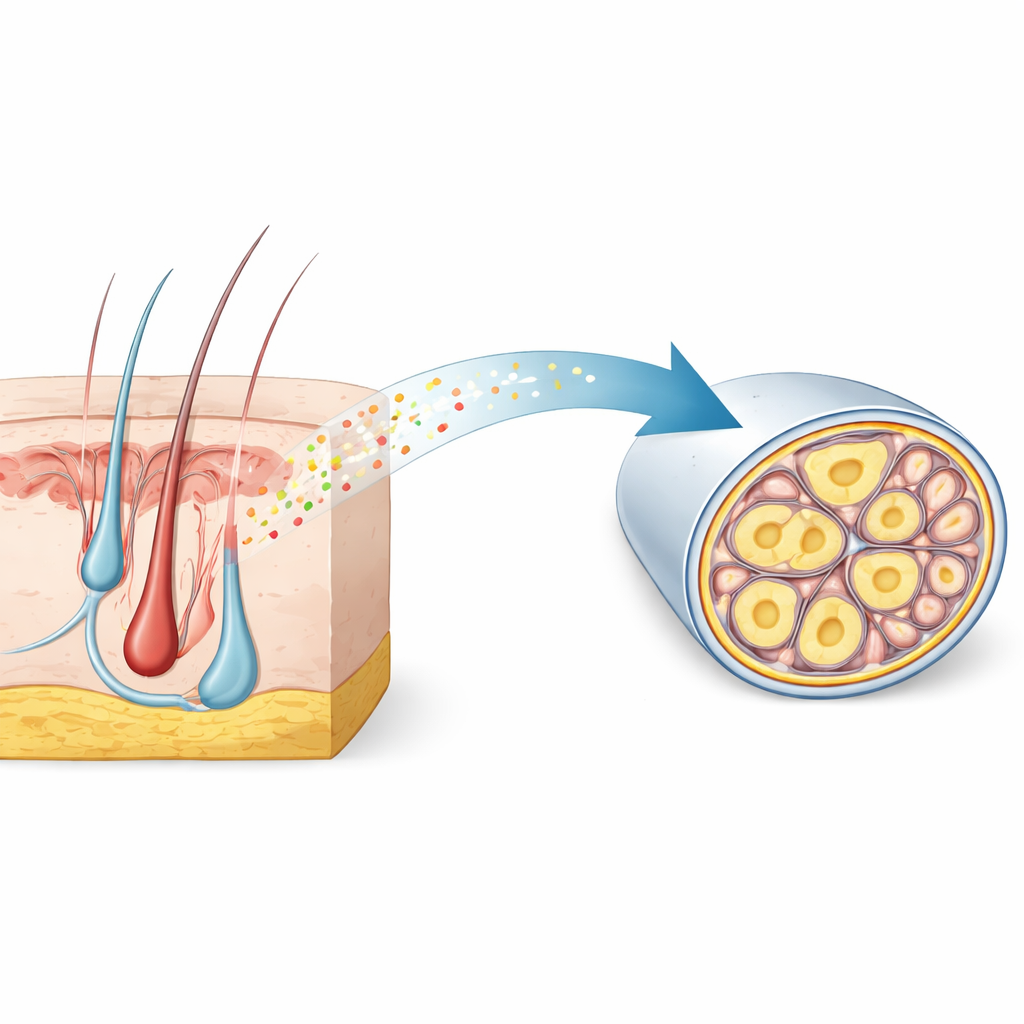
Een verborgen signatuur binnen pijnzenuwen
De onderzoekers begonnen met het analyseren van grote enkelcelligenetische atlasgegevens van sensorische ganglia—clusters neuronen die aanraking en pijn van het lichaam naar het ruggenmerg geleiden. Ze zochten naar genen die specifiek aan staan in dunne, niet-gemyeliniseerde nociceptoren, die trage, zeurende pijn geleiden. Uit duizenden kandidaten sprong RNase4 eruit als een zeer selectieve marker in muizen en vertoonde een overeenkomstig patroon in menselijk weefsel. Microscopen bevestigden dat RNase4 vooral voorkomt in kleine-diameter, niet-gemyeliniseerde neuronen van de nociceptore afstamming, maar niet in zwaar gemyeliniseerde neuronen die snelle aanraking en vibratie verwerken. Deze conservedheid tussen soorten suggereert dat RNase4 een gespecialiseerde subset van pijnzintuigcellen markeert met een gedeelde biologische rol.
Het gedrag van zenuwen van binnenuit vormen
Om te onderzoeken wat RNase4 doet, creëerde het team muizen waarin het gen verwijderd kon worden, ofwel vroeg in de ontwikkeling of alleen in volwassen nociceptoren. Wanneer RNase4 tijdens de ontwikkeling werd verwijderd, bleef de basale bedrading van pijncircuits en de normale gevoeligheid voor warmte en aanraking grotendeels intact. Echter, single-nucleus RNA-sequencing toonde aan dat veel genen in nociceptoren van activiteit veranderden, waaronder transcriptiefactoren, structurele eiwitten en componenten van kaliumkanalen die helpen de elektrische drempel voor neuronale vuring te bepalen. Bij volwassen muizen leidde het uitschakelen van RNase4 alleen in nociceptoren tot een tijdelijke toename van mechanische pijngevoeligheid: de dieren reageerden sterker op lichte aanraking met vezels op de poot, terwijl warmtegevoeligheid stabiel bleef. Over ongeveer een maand vervaagde deze verhoogde mechanische gevoeligheid, wat erop wijst dat andere paden in de loop van de tijd compenseren om het evenwicht te herstellen.
Signalen naar naburige cellen uitzenden
RNase4 kan buiten de cel worden uitgescheiden, wat de mogelijkheid opent dat nociceptoren naburige zenuwvezels en ondersteunende cellen beïnvloeden. In celkweek dempte het toevoegen van RNase4 aan een sensoriële neuron-achtige cellijn de activiteit van de PI3K–AKT–mTOR-route, een centraal groeu- en overlevingssignaalpad. In levende muizen gebruikten de auteurs vervolgens een model van sciaticuszenuwkneuzing, dat traumatisch zenuwletsel gevolgd door degeneratie en hergroei nabootst. Na letsel stegen de RNase4-niveaus van nature in veel nociceptor-subtypen, vooral tijdens de vroege pijn- en herstelstadia. Wanneer RNase4 ontbrak in nociceptoren, lieten gedragsmetingen zien dat muizen de mechanische sensatie feitelijk sneller herkregen dan controles, hoewel het thermische herstel kon achterblijven afhankelijk van de deletiestrategie. Dit suggereert dat RNase4 normaal gezien bepaalde aspecten van hergroei en gevoeligheid remt, en dat het weghalen ervan het systeem kantelt richting snellere tactiele herstelprocessen.
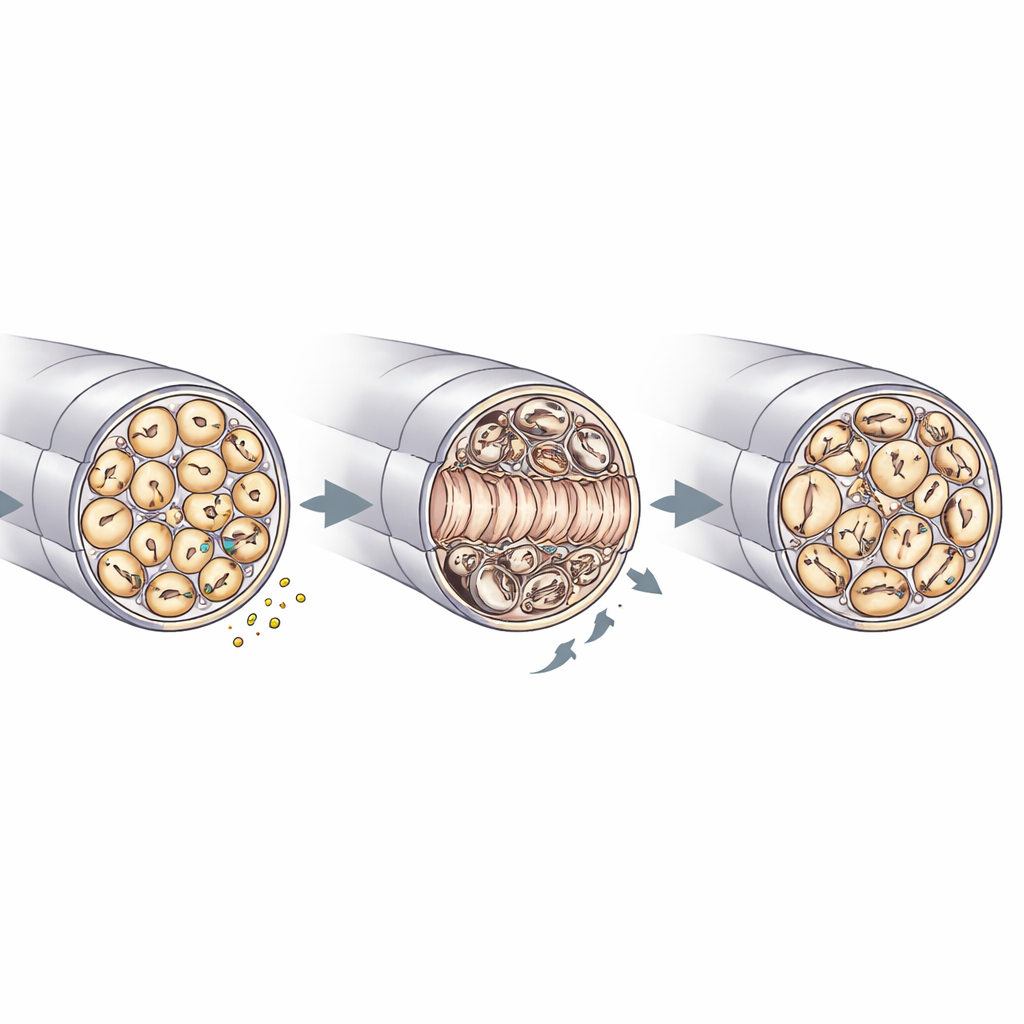
Herstel, myelinekwaliteit en zenuwonderhoud
Elektromicroscopie van de sciaticuszenuwen gaf een gedetailleerder beeld van hoe RNase4 de zenuwarchitectuur vormt. Voor het letsel zagen knockout- en controlezenuwen er vergelijkbaar uit, met vergelijkbare axondiameters, dichtheden en myelinedikte. Na kneuzing bevatten zenuwen zonder RNase4 echter meer geregenereerde axonen in het beschadigde segment en vertoonden ze snellere heropvulling van niet-gemyeliniseerde “Remak”-bundels die veel dunne vezels huisvesten. Tegelijkertijd toonden deze knockout-zenuwen meer myeline-onregelmatigheden—zoals plooien, invouwingen en focale verdikkingen—en tekenen van stress in Schwanncellen, de gliacellen die axonen omhullen. Er was ook minder mylineafval in immuuncellen, wat overeenstemt met efficiëntere opruiming en snellere structurele heropbouw. Samen met de signaleringsstudies ondersteunen deze bevindingen een model waarin nociceptor-afgeleide RNase4 PI3K–AKT-activiteit afstemt en, via niet-lokale effecten, coördineert hoe axonen hergroeien, hoe myeline wordt gemodelleerd en hoe immuuncellen deelnemen aan het opruimproces.
Wat dit betekent voor toekomstige behandelingen
Kort gezegd schildert de studie nociceptoren niet alleen als alarmbellen maar als lokale managers van zenuwgezondheid. RNase4 fungeert als een moleculaire rem en gids: binnen nociceptoren helpt het hun normale vuringseigenschappen en identiteit te behouden; buiten de cel beperkt het overdreven hergroei en bepaalt het hoe myeline en ondersteunende cellen reageren na letsel. Het weghalen van RNase4 kan het terugkeren van tastzin na zenuwbeschadiging versnellen, maar met als prijs meer myelinefouten en veranderde pijngevoeligheid. Elke therapie die gericht is op het blokkeren of versterken van RNase4 zal deze afwegingen moeten balanceren. Toch benadrukt het werk RNase4 en het bijbehorende signaalnetwerk als veelbelovende knoppen om tegelijk pijn te moduleren en ordelijker zenuwherstel te bevorderen.
Bronvermelding: Feng, X., Zhang, K., Techameena, P. et al. Ribonuclease 4 Functions in Nociceptor-Mediated Nerve Homeostasis. Nat Commun 17, 2862 (2026). https://doi.org/10.1038/s41467-026-70365-8
Trefwoorden: nociceptoren, zenuwregeneratie, myeline, neuropathische pijn, RNase4