Clear Sky Science · de
Ribonuklease 4 wirkt auf die Homöostase von Nerven durch nozizeptorvermittelte Prozesse
Warum das für Menschen mit Schmerzen wichtig ist
Schmerznerven werden oft als einfache Boten dargestellt, die Alarm schlagen, wenn etwas wehtut. Diese Studie zeigt, dass einige dieser schmerzempfindenden Neuronen, die Nozizeptoren genannt werden, zugleich stillschweigend die Gesundheit benachbarter Nervenfasern mitverwalten. Im Mittelpunkt steht ein bislang wenig bekanntes Molekül, die Ribonuklease 4 (RNase4), das sowohl dazu beiträgt, Schmerzsignale zu regulieren, als auch zu steuern, wie geschädigte Nerven abgebaut und wieder aufgebaut werden. Das Verständnis dieser Doppelrolle könnte neue Wege zur Behandlung chronischer Schmerzen und zur Verbesserung der Nervenreparatur nach Verletzungen eröffnen.
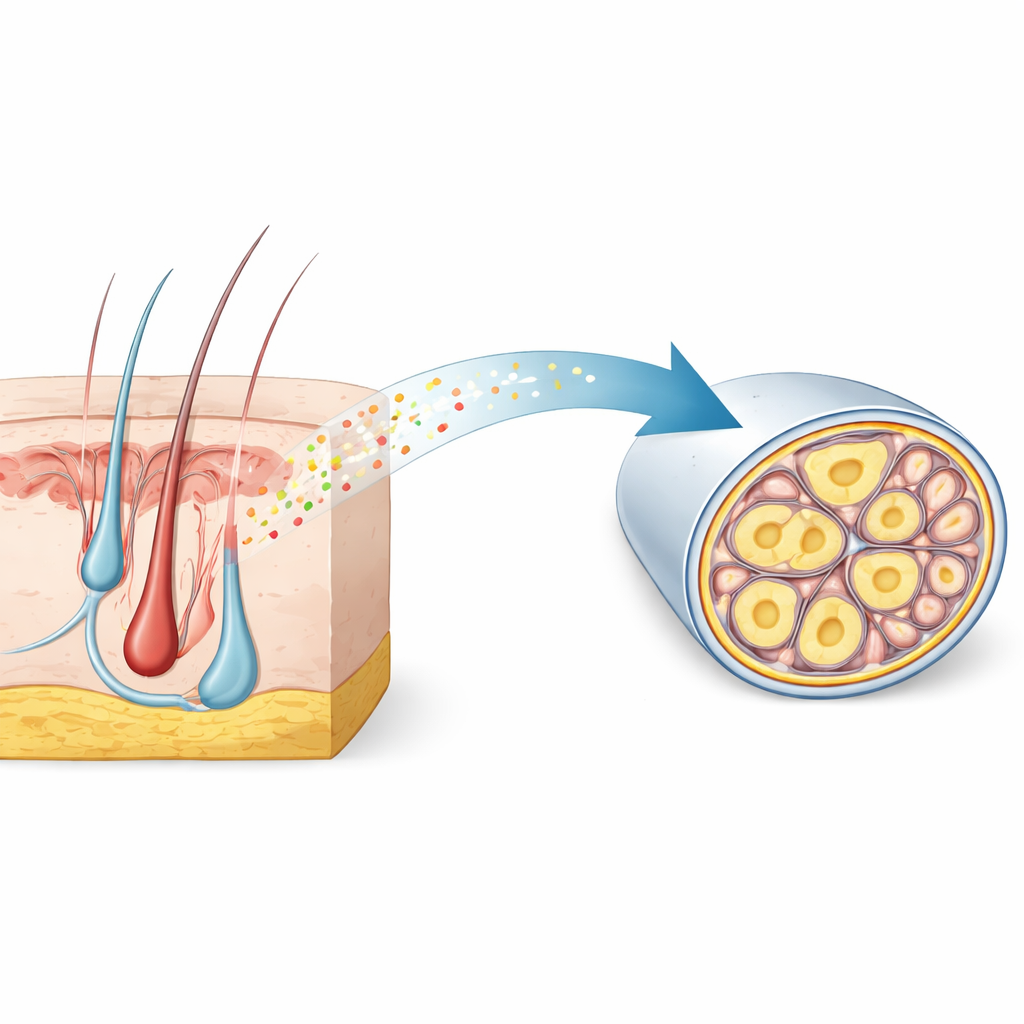
Eine verborgene Signatur innerhalb schmerzempfindender Nerven
Die Forschenden begannen damit, umfangreiche Einzelzell-Genatlanten sensorischer Ganglien zu analysieren—Cluster von Neuronen, die Berührung und Schmerz vom Körper zum Rückenmark leiten. Sie suchten nach Genen, die speziell in dünnen, unmyelinisierten Nozizeptoren aktiviert sind, welche langsamen, dumpfen Schmerz übertragen. Unter Tausenden von Kandidaten hob sich RNase4 als hochselektiver Marker in Mäusen ab und zeigte in menschlichem Gewebe ein ähnliches Muster. Mikroskopie bestätigte, dass RNase4 vor allem in kleinradrigen, unmyelinisierten Neuronen des Nozizeptor-Lineage vorkommt, nicht jedoch in stark myelinisierten Neuronen, die schnelle Berührung und Vibration verarbeiten. Diese konservierte Verteilung über die Arten hinweg deutet darauf hin, dass RNase4 eine spezialisierte Untergruppe von schmerzempfindenden Zellen mit gemeinsamer biologischer Funktion kennzeichnet.
Das Verhalten von Nerven von innen formen
Um die Funktion von RNase4 zu untersuchen, erzeugte das Team Mäuse, bei denen das Gen entweder früh in der Entwicklung oder nur in erwachsenen Nozizeptoren gelöscht werden konnte. Wurde RNase4 während der Entwicklung entfernt, blieben die grundlegende Verschaltung der Schmerzkreisläufe sowie die normale Wärme- und Berührungsempfindlichkeit größtenteils intakt. Einzelkern-RNA-Sequenzierung zeigte jedoch, dass in Nozizeptoren viele Gene in ihrer Aktivität verändert waren, darunter Transkriptionsfaktoren, Strukturproteine und Komponenten von Kaliumkanälen, die die elektrische Erregbarkeit der Neuronen mitbestimmen. Bei erwachsenen Mäusen führte das selektive Abschalten von RNase4 in Nozizeptoren zu einer vorübergehenden Zunahme der mechanischen Schmerzempfindlichkeit: Die Tiere reagierten stärker auf leichte Berührung mit Filamenten an der Pfote, während die Temperaturempfindlichkeit stabil blieb. Innerhalb von etwa einem Monat ließ diese gesteigerte mechanische Empfindlichkeit nach, was darauf hindeutet, dass andere Wege im Laufe der Zeit kompensieren und das Gleichgewicht wiederherstellen.
Signale nach außen an benachbarte Zellen senden
RNase4 kann aus der Zelle ausgeschieden werden, was die Möglichkeit eröffnet, dass Nozizeptoren benachbarte Nervenfasern und Stütz-Zellen beeinflussen. In Zellkultur dämpfte die Zugabe von RNase4 an eine sensorische Neuronen-ähnliche Zelllinie die Aktivität des PI3K–AKT–mTOR-Wegs, eines zentralen Wachstums- und Überlebenssignalwegs. In lebenden Mäusen verwendeten die Autorinnen und Autoren anschließend ein Modell der Schädigung des Ischiasnervs durch Quetschung, das eine traumatische Nervenverletzung mit anschließendem Abbau und Wiederaufbau nachahmt. Nach der Verletzung stiegen die RNase4-Spiegel natürlicherweise in vielen Nozizeptor-Subtypen an, besonders in den frühen Schmerzs- und Erholungsphasen. Fehlt RNase4 in Nozizeptoren, zeigten Verhaltenstests, dass Mäuse die mechanische Empfindung tatsächlich schneller wiedererlangten als Kontrollen, obwohl die thermische Wiederherstellung je nach Löschstrategie verzögert sein konnte. Das deutet darauf hin, dass RNase4 normalerweise bestimmte Aspekte des Wiederaufbaus und der Sensitivität bremst und seine Entfernung das System in Richtung schnellerer taktiler Erholung verschiebt.
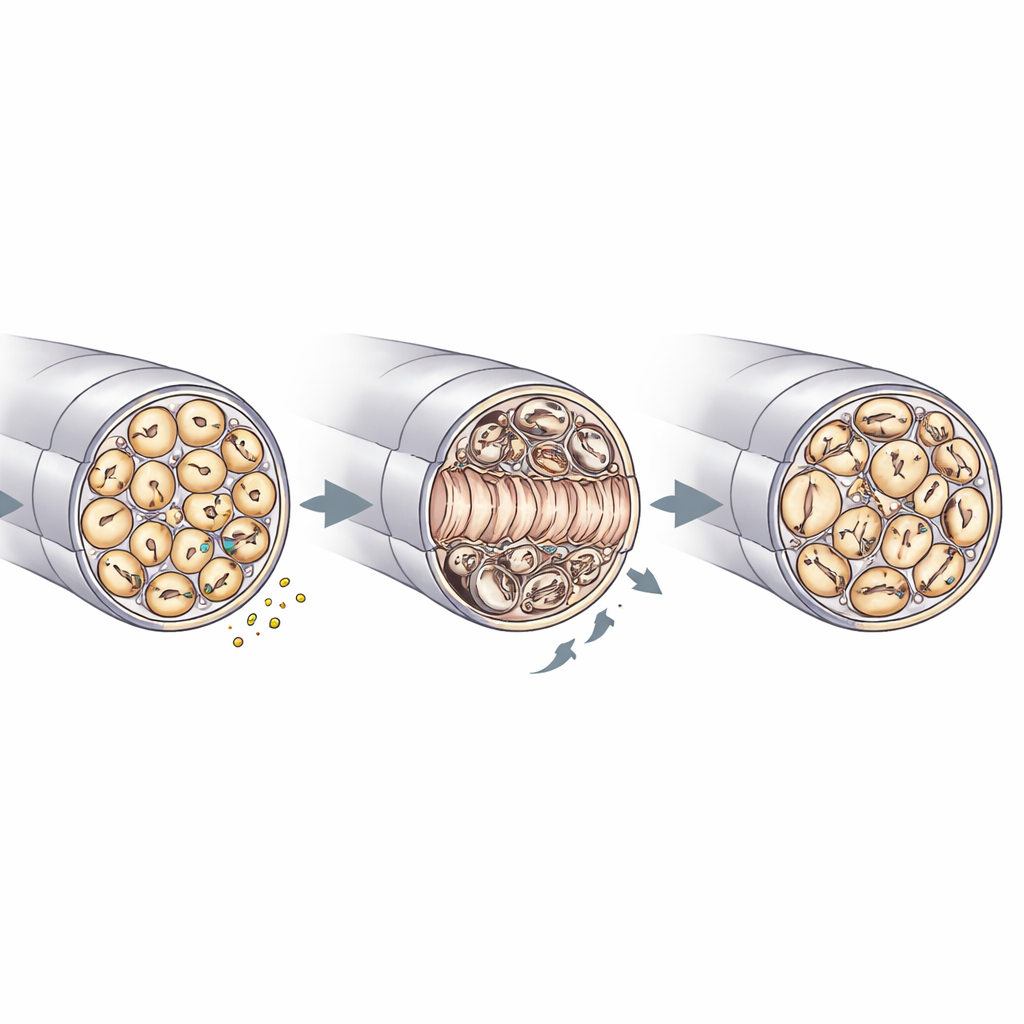
Reparatur, Myelinqualität und Nerven-Haushalt
Elektronenmikroskopie des Ischiasnervs lieferte einen genaueren Blick darauf, wie RNase4 die Nervenarchitektur beeinflusst. Vor der Verletzung wirkten Knockout- und Kontrollnerven ähnlich, mit vergleichbaren Axondurchmessern, Dichten und Myelindicken. Nach der Quetschverletzung enthielten die Nerven ohne RNase4 jedoch mehr regenerierte Axone im geschädigten Abschnitt und zeigten eine schnellere Wiederauffüllung nicht-myelinisierter "Remak"-Bündel, die viele dünne Fasern beherbergen. Gleichzeitig wiesen diese Knockout-Nerven mehr Myelinunregelmäßigkeiten auf—wie Falten, Einfaltungen und lokale Verdickungen—und Anzeichen von Stress in Schwann-Zellen, den Gliazellen, die Axone umhüllen. Es gab auch weniger Myelinschutt in Immunzellen, was zu einer effizienteren Beseitigung und schnellerem strukturellem Wiederaufbau passt. Zusammen mit den Signalstudien stützen diese Befunde ein Modell, in dem nozizeptorderiviertes RNase4 die PI3K–AKT-Aktivität abstimmt und über nicht-lokale Effekte koordiniert, wie Axone nachwachsen, wie Myelin umgebaut wird und wie Immunzellen an der Reinigung beteiligt sind.
Was das für zukünftige Therapien bedeutet
Ganz praktisch betrachtet zeichnet die Studie Nozizeptoren nicht nur als Alarmglocken, sondern als lokale Manager der Nervengesundheit. RNase4 wirkt als molekularer Brems- und Lenkmechanismus: In Nozizeptoren hilft es, ihre normalen Feuereigenschaften und Identität aufrechtzuerhalten; außerhalb begrenzt es übermäßigen Wiederaufwuchs und beeinflusst, wie Myelin und Stütz-Zellen nach einer Verletzung reagieren. Das Entfernen von RNase4 kann die Wiederkehr der Tastempfindung nach Nervenschaden beschleunigen, allerdings auf Kosten vermehrter Myelindefekte und veränderter Schmerzempfindlichkeit. Jede Therapie, die auf die Hemmung oder Verstärkung von RNase4 abzielt, muss diese Abwägungen ausbalancieren. Dennoch hebt die Arbeit RNase4 und sein Signalnetzwerk als vielversprechende Ansatzpunkte hervor, um Schmerz zu modulieren und zugleich einen geordneten Nervenaufbau zu fördern.
Zitation: Feng, X., Zhang, K., Techameena, P. et al. Ribonuclease 4 Functions in Nociceptor-Mediated Nerve Homeostasis. Nat Commun 17, 2862 (2026). https://doi.org/10.1038/s41467-026-70365-8
Schlüsselwörter: Nozizeptoren, Nerveregeneration, Myelin, neuropathischer Schmerz, RNase4