Clear Sky Science · sv
Ribonukleas 4:s funktioner i nociceptor-meddragen nervhomeostas
Varför detta är viktigt för personer som lever med smärta
Smärtnerver framställs ofta som enkla budbärare som skriker när något gör ont. Denna studie visar att några av dessa smärtsensoriska neuroner, kallade nociceptorer, också tyst ansvarar för hälsan hos närliggande nervfibrer. Arbetet fokuserar på en relativt okänd molekyl, ribonukleas 4 (RNase4), och visar att den hjälper till att hålla smärtsignaler i schack samtidigt som den styr hur skadade nerver bryts ner och återuppbyggs. Att förstå denna dubbla roll kan öppna nya vägar för behandling av kronisk smärta och förbättrad nervreparation efter skada.
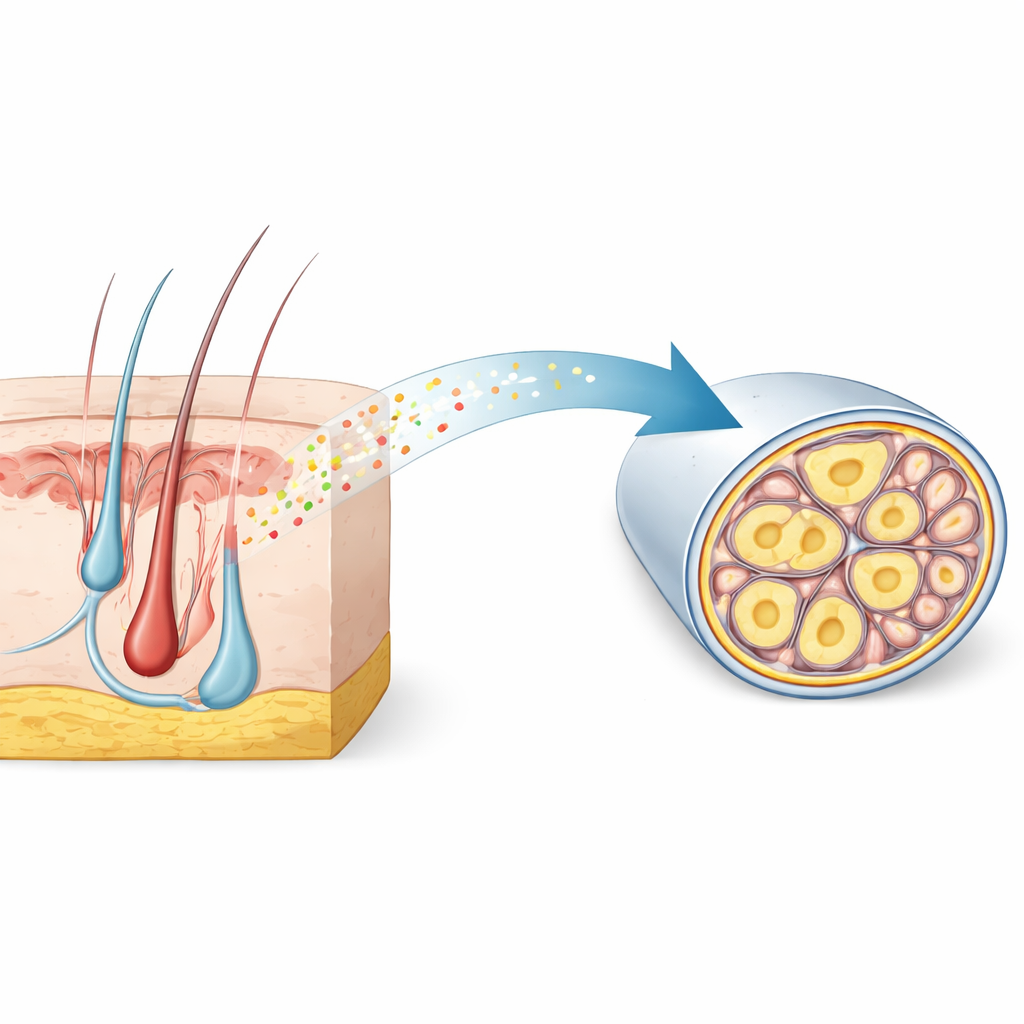
Ett dolt signaturmönster i smärtsensoriska nerver
Forskarlaget började med att granska stora enklacellsgenetiska atlaser av sensoriska ganglier—kluster av neuroner som förmedlar beröring och smärta från kroppen till ryggmärgen. De sökte efter gener som var aktiva specifikt i tunna, omyeliniserade nociceptorer som förmedlar långsammare, molande smärta. Bland tusentals kandidater framstod RNase4 som en högst selektiv markör hos möss och visade ett motsvarande mönster i mänsklig vävnad. Mikroskopi bekräftade att RNase4 främst finns i smådiameter, omyeliniserade neuroner som tillhör nociceptorlinjen, men inte i kraftigt myeliniserade neuroner som hanterar snabb beröring och vibration. Denna konservering mellan arter tyder på att RNase4 markerar en specialiserad undergrupp av smärtsensoriska celler med en gemensam biologisk funktion.
Formar nervbeteende inifrån
För att undersöka vad RNase4 gör konstruerade teamet möss där genen kunde tas bort antingen tidigt i utvecklingen eller bara i vuxna nociceptorer. När RNase4 togs bort under utvecklingen förblev den grundläggande kopplingen i smärtbanorna och normal värme- och känselkänslighet i stort sett intakta. Men singelnukleär RNA-sekvensering visade att många gener ändrade aktivitetsnivå inne i nociceptorerna, inklusive transkriptionsfaktorer, strukturella proteiner och komponenter i kaliumkanaler som hjälper till att ställa in neuroners elektriska tröskel för fyrning. Hos vuxna möss gav avstängning av RNase4 endast i nociceptorer en tillfällig ökning av mekanisk smärtkänslighet: djuren reagerade starkare på lätt beröring med filament applicerade på tassen, medan värmekänsligheten förblev stabil. Under ungefär en månad avtog denna förhöjda mekaniska känslighet, vilket tyder på att andra vägar kompenserar över tid för att återställa balans.
Skickar signaler utåt till intilliggande celler
RNase4 kan utsöndras utanför cellen, vilket öppnar för att nociceptorer påverkar närliggande nervfibrer och stödjeceller. I cellkultur dämpade tillsats av RNase4 aktiviteten i PI3K–AKT–mTOR‑vägen, en central signaleringsnod för tillväxt och överlevnad. I levande möss använde författarna sedan en modell med krosskada av ischiasnerven, som efterliknar traumatisk nervskada följd av degeneration och återväxt. Efter skada ökade RNase4‑nivåerna naturligt över många nociceptorsubtyper, särskilt under tidiga smärt- och återhämtningsfaser. När RNase4 saknades i nociceptorer visade beteendetester att mössen faktiskt återfick mekanisk känsel snabbare än kontroller, även om termisk återhämtning kunde fördröjas beroende på deletionsstrategi. Detta antyder att RNase4 normalt dämpar vissa aspekter av återväxt och känslighet, och att borttagning av den förskjuter systemet mot snabbare taktil återhämtning.
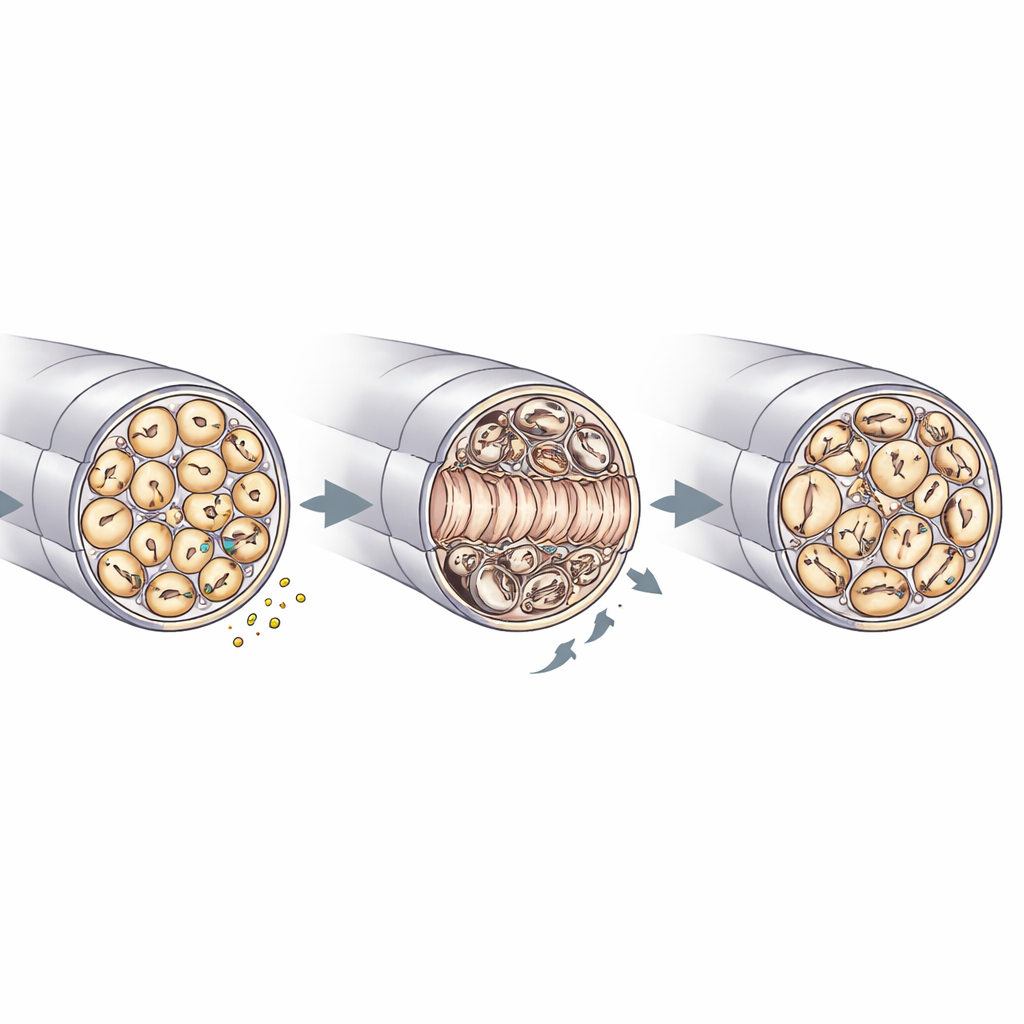
Reparation, myelinkvalitet och nervunderhåll
Elektronmikroskopi av ischiasnerver gav en närmare bild av hur RNase4 formar nervarkitekturen. Före skada såg knockout- och kontrollnervarna liknande ut, med jämförbara axondiametrar, densiteter och myelintjocklek. Efter krosskadan innehöll nerver utan RNase4 däremot fler regenererade axoner i den skadade delen och visade snabbare återfyllnad av icke‑myeliniserade "Remak"‑buntar som rymmer många tunna fibrer. Samtidigt uppvisade dessa knockout‑nerver fler myelinrubbningar—såsom veck, infoldningar och fokal förtjockning—och tecken på stress i Schwann‑cellerna, de gliaceller som omsluter axonen. Det fanns också mindre myelinskräp inne i immunceller, i linje med effektivare bortstädning och snabbare strukturell återuppbyggnad. Tillsammans med signaleringsstudierna stöder dessa fynd en modell där nociceptor‑härlett RNase4 finjusterar PI3K–AKT‑aktivitet och genom icke‑lokala effekter samordnar hur axoner växer ut igen, hur myelin omformas och hur immunceller deltar i städningen.
Vad detta betyder för framtida behandlingar
Enkelt uttryckt framställer studien nociceptorer inte bara som alarmklockor utan som lokala förvaltare av nervhälsa. RNase4 fungerar som en molekylär broms och vägvisare: inuti nociceptorer hjälper den till att bevara deras normala fyrningsegenskaper och identitet; utanför begränsar den överivrig återväxt och formar hur myelin och stödjeceller reagerar efter skada. Att ta bort RNase4 kan snabba upp återkomsten av beröring efter nervskada men på bekostnad av fler myelinavvikelser och förändrad smärtkänslighet. All behandling som syftar till att blockera eller förstärka RNase4 måste väga dessa kompromisser. Ändå pekar arbetet på RNase4 och dess signalnätverk som lovande spakar för att samtidigt modulera smärta och främja mer ordnad nervreparation.
Citering: Feng, X., Zhang, K., Techameena, P. et al. Ribonuclease 4 Functions in Nociceptor-Mediated Nerve Homeostasis. Nat Commun 17, 2862 (2026). https://doi.org/10.1038/s41467-026-70365-8
Nyckelord: nociceptorer, nervregeneration, myelin, neuropatisk smärta, RNase4