Clear Sky Science · ru
Функции рибонуклеазы 4 в поддержании гомеостаза нервов, зависящего от ноцицепторов
Почему это важно для людей, живущих с болью
Нервные окончания боли часто изображают как простые посланцы, которые кричат, когда что‑то болит. Это исследование показывает, что часть этих болевых нейронов, называемых ноцицепторами, тихо управляет и здоровьем соседних нервных волокон. Работа сосредоточена на малоизвестной молекуле — рибонуклеазе 4 (RNase4) — и демонстрирует, что она помогает сдерживать болевые сигналы и одновременно направляет процессы разрушения и восстановления повреждённых нервов. Понимание этой двойной роли может открыть новые пути для лечения хронической боли и улучшения восстановления нервов после травм.
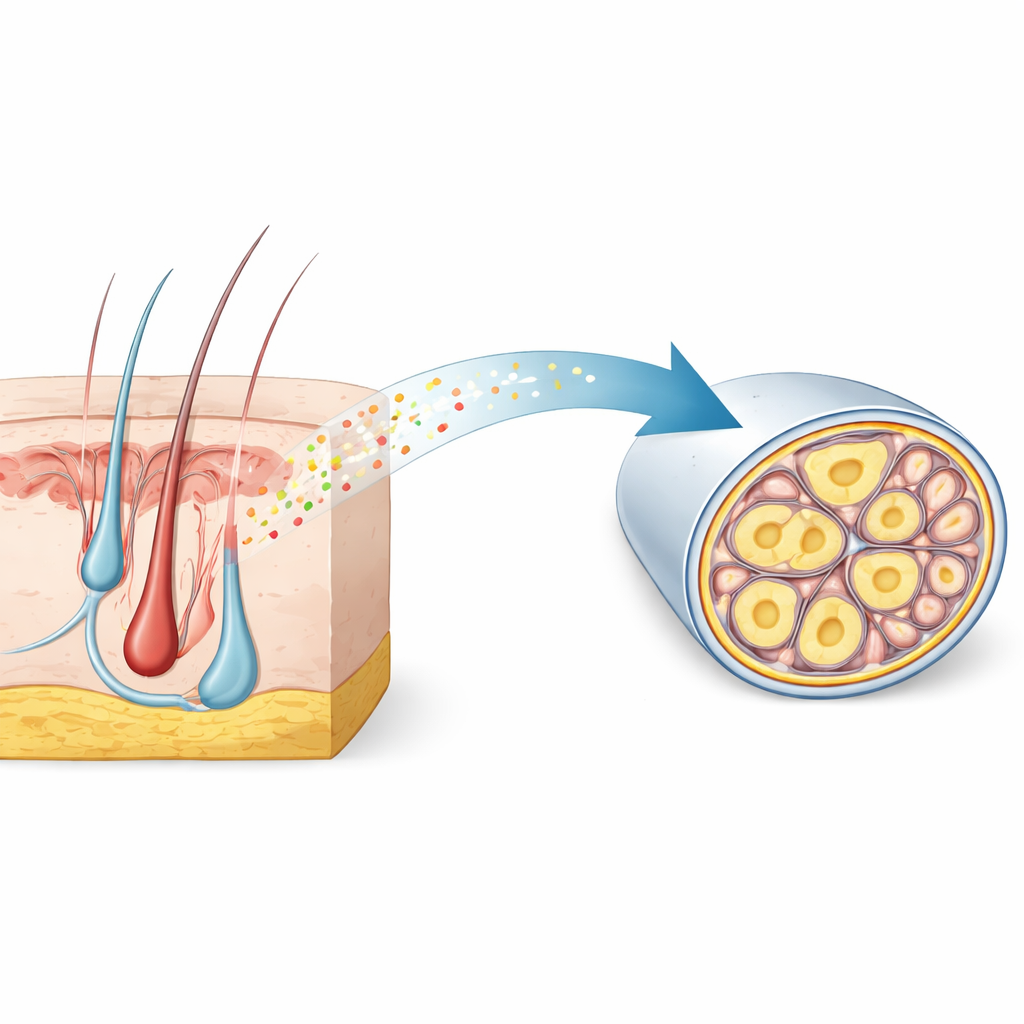
Скрытая подпись внутри болевых нервов
Исследователи начали с анализа больших атласов одиночных клеток сенсорных ганглиев — скоплений нейронов, передающих прикосновение и боль от тела к спинному мозгу. Они искали гены, включённые специфически в тонких немиелинизированных ноцицепторах, которые несут медленную, тянущую боль. Среди тысяч кандидатов RNase4 выделялась как высокоселективный маркер у мышей и демонстрировала похожую картину в тканях человека. Микроскопия подтвердила, что RNase4 локализуется преимущественно в мелкодиаметрических немиелинизированных нейронах, принадлежащих к линейке ноцицепторов, но не обнаруживается в сильно миелинизированных нейронах, отвечающих за быструю тактильную чувствительность и вибрацию. Такая консервация между видами указывает на то, что RNase4 отмечает специализированный подтип болевых сенсорных клеток с общей биологической ролью.
Формирование поведения нерва изнутри
Чтобы выяснить функцию RNase4, группа создала мышей, у которых ген можно было удалить либо на ранних стадиях развития, либо только в зрелых ноцицепторах. При удалении RNase4 в ходе развития базовая проводящая схема болевых путей и нормальная чувствительность к теплу и прикосновению в целом сохранялись. Однако одиночное ядерное РНК‑секвенирование выявило изменения экспрессии множества генов внутри ноцицепторов, включая факторы транскрипции, структурные белки и компоненты калиевых каналов, задающих порог электрической возбудимости нейронов. У взрослых мышей выключение RNase4 только в ноцицепторах вызывало временное повышение механической болевой чувствительности: животные сильнее реагировали на лёгкое прикосновение филиалами к подушечке лапы, тогда как чувствительность к теплу оставалась стабильной. Примерно через месяц повышенная механическая чувствительность угасала, что указывает на компенсацию со стороны других путей с восстановлением баланса.
Посыл сигналов наружу к соседним клеткам
RNase4 может секретироваться за пределы клетки, что повышает вероятность того, что ноцицепторы влияют на соседние нервные волокна и клетки‑опорники. В культуре клеток добавление RNase4 к линии, похожей на сенсорные нейроны, подавляло активность пути PI3K–AKT–mTOR — ключевого сигнального узла роста и выживания. В живых мышах авторы применили модель раздавливания седалищного нерва, имитирующую травматическое повреждение с последующей дегенерацией и регенерацией. После травмы уровни RNase4 естественным образом повышались во многих подтипах ноцицепторов, особенно на ранних этапах боли и восстановления. При отсутствии RNase4 в ноцицепторах поведенческие тесты показали, что мыши восстанавливали механическую чувствительность быстрее, чем контрольные животные, хотя тепловое восстановление могло отставать в зависимости от стратегии удаления гена. Это указывает на то, что RNase4 обычно сдерживает некоторые аспекты регенерации и чувствительности, а его удаление склоняет систему к более быстрому тактильному восстановлению.
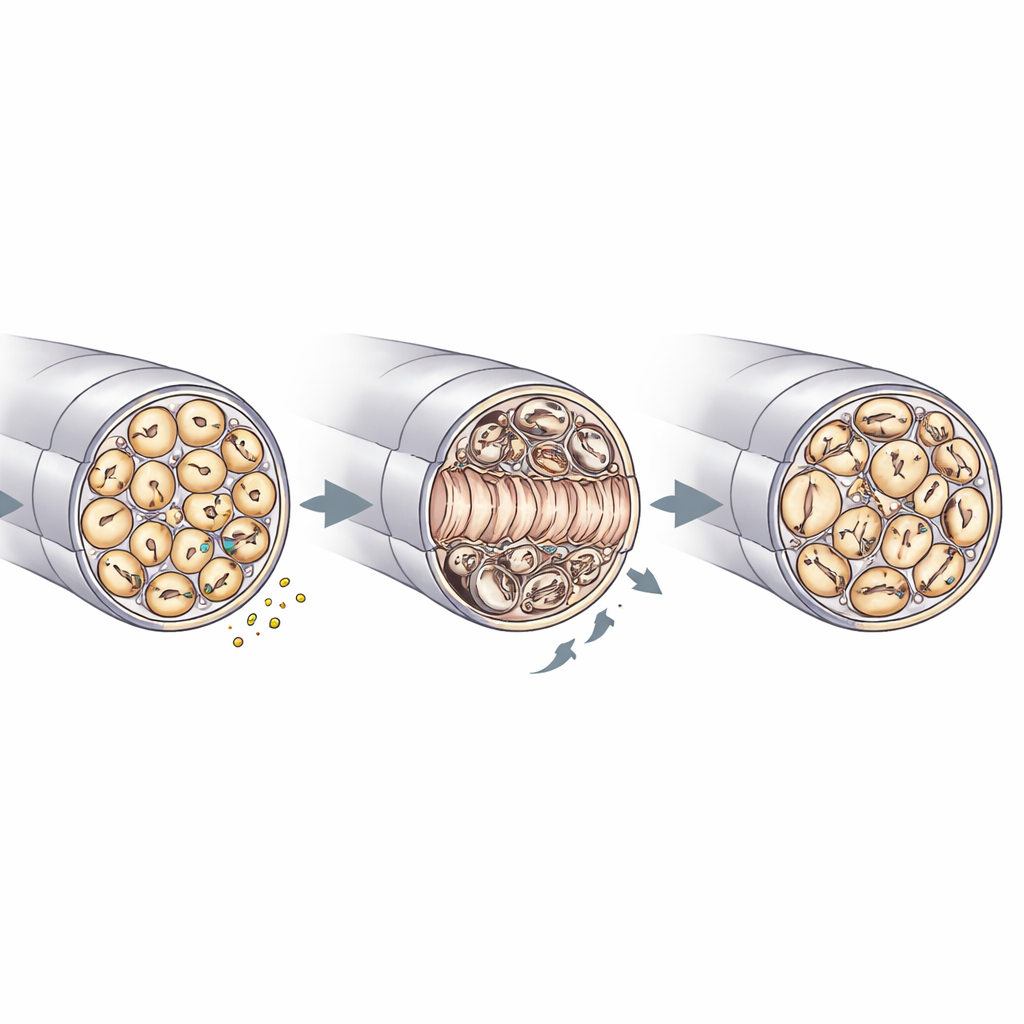
Ремонт, качество миелина и «уборка» в нервах
Электронная микроскопия седалищных нервов дала более детальное представление о том, как RNase4 формирует архитектуру нервов. До повреждения нервы с нокаутом и контрольные нервы выглядели схожим образом: сопоставимы диаметры аксонов, плотность и толщина миелина. После раздавливания же в нервах без RNase4 оказалось больше регенерировавших аксонов в повреждённом сегменте, и быстрее заполнялись немиелинизированные «пучки Ремека», где размещается множество тонких волокон. Вместе с тем в этих нокаутах наблюдались более частые нарушения миелина — складки, вхождения и локальные утолщения — и признаки стресса в шванновских клетках, которые оплетают аксоны. Также внутри иммунных клеток было меньше остатков миелина, что согласуется с более эффективным очищением и ускоренным структурным восстановлением. В сочетании с данными о сигнальных путях эти наблюдения поддерживают модель, в которой RNase4, выделяемая ноцицепторами, регулирует активность PI3K–AKT и через внеклеточные эффекты координирует регростаксию аксонов, ремоделирование миелина и участие иммунных клеток в «уборке».
Что это значит для будущих лечений
Проще говоря, исследование рисует ноцицепторы не только как сигнализаторы тревоги, но и как локальных управляющих здоровья нервов. RNase4 действует как молекулярный тормоз и наставник: внутри ноцицепторов она поддерживает их нормальные свойства возбуждаемости и идентичность; снаружи — ограничивает необузданную регенерацию и формирует ответ миелина и вспомогательных клеток после повреждения. Удаление RNase4 может ускорить восстановление тактильной чувствительности после повреждения нерва, но это происходит ценой большего числа дефектов миелина и изменённой болевой реактивности. Любая терапия, направленная на блокирование или усиление RNase4, должна будет взвешивать эти компромиссы. Тем не менее работа выделяет RNase4 и его сигнальную сеть как перспективные рычаги для одновременной модуляции боли и содействия более упорядоченному восстановлению нервов.
Цитирование: Feng, X., Zhang, K., Techameena, P. et al. Ribonuclease 4 Functions in Nociceptor-Mediated Nerve Homeostasis. Nat Commun 17, 2862 (2026). https://doi.org/10.1038/s41467-026-70365-8
Ключевые слова: ноцицепторы, регенерация нервов, миелин, невропатическая боль, RNase4