Clear Sky Science · pt
Ribonuclease 4 funciona na homeostase nervosa mediada por nociceptores
Por que isso importa para pessoas que vivem com dor
Os nervos de dor costumam ser reduzidos a mensageiros simples que alertam quando algo dói. Este estudo revela que alguns desses neurônios sensor de dor, chamados nociceptores, também gerenciam discretamente a saúde das fibras nervosas vizinhas. O trabalho concentra-se em uma molécula pouco conhecida, a ribonuclease 4 (RNase4), e mostra que ela ajuda a manter os sinais de dor sob controle ao mesmo tempo em que orienta como nervos danificados se degradam e se reconstroem. Entender esse papel duplo pode abrir novos caminhos para tratar dor crônica e melhorar a reparação nervosa após lesão.
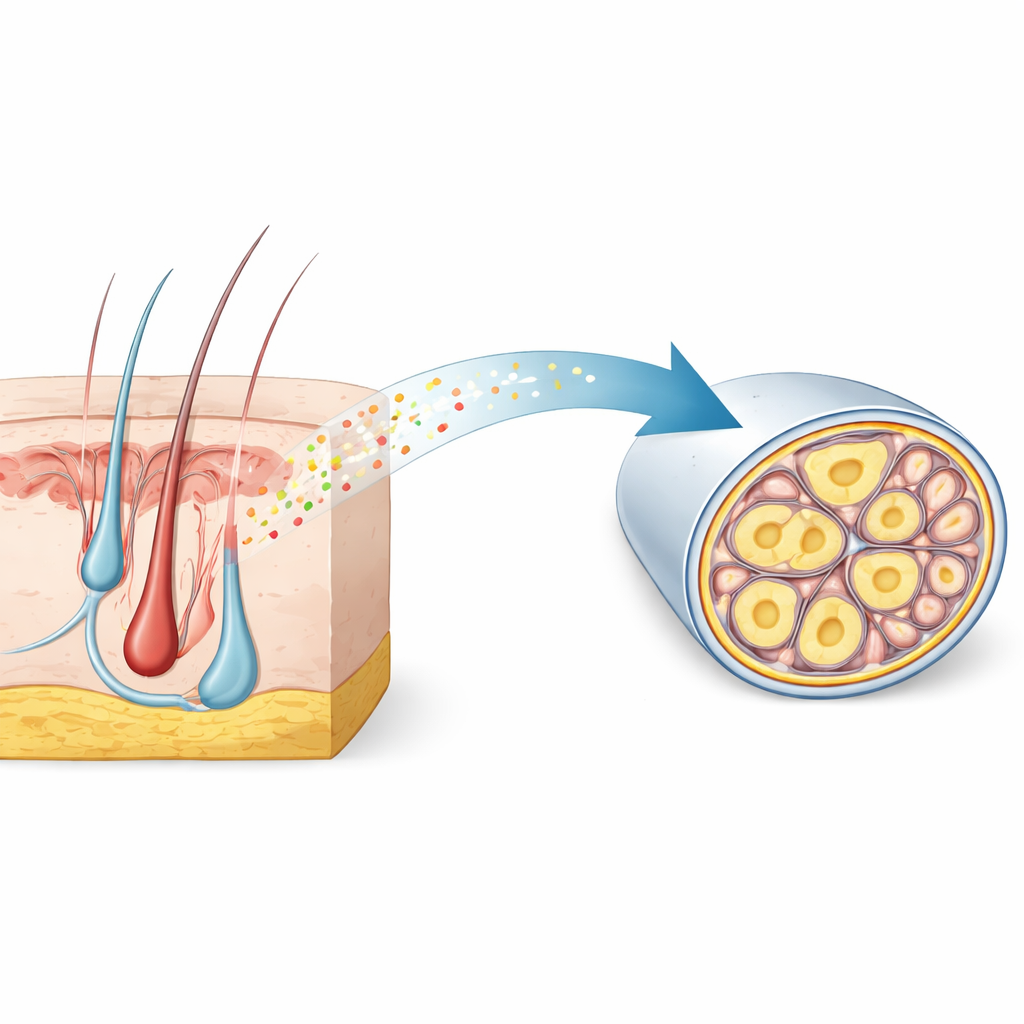
Uma assinatura oculta dentro dos nervos sensoriais de dor
Os pesquisadores começaram vasculhando grandes atlas genéticos de célula única dos gânglios sensoriais — aglomerados de neurônios que transmitem toque e dor do corpo para a medula espinhal. Eles procuraram genes ativados especificamente em nociceptores finos e não mielinizados, que conduzem a dor lenta e incômoda. Entre milhares de candidatos, RNase4 destacou-se como um marcador altamente seletivo em camundongos e mostrou um padrão correspondente em tecido humano. A microscopia confirmou que RNase4 é encontrada principalmente em neurônios de pequeno diâmetro e não mielinizados pertencentes à linhagem dos nociceptores, mas não em neurônios fortemente mielinizados que lidam com toque rápido e vibração. Essa conservação entre espécies sugere que RNase4 marca um subconjunto especializado de células sensoriais de dor com um papel biológico compartilhado.
Moldando o comportamento nervoso de dentro para fora
Para investigar o que RNase4 faz, a equipe criou camundongos em que o gene podia ser deletado ou cedo no desenvolvimento ou apenas nos nociceptores adultos. Quando RNase4 foi removida durante o desenvolvimento, a fiação básica dos circuitos de dor e a sensibilidade normal ao calor e ao toque permaneceram amplamente intactas. Contudo, o sequenciamento de RNA de núcleo único revelou que muitos genes alteraram sua atividade dentro dos nociceptores, incluindo fatores de transcrição, proteínas estruturais e componentes de canais de potássio que ajudam a definir o limiar elétrico de disparo dos neurônios. Em camundongos adultos, desligar RNase4 apenas nos nociceptores desencadeou um aumento temporário na sensibilidade à dor mecânica: os animais reagiram mais intensamente a toques leves com filamentos aplicados à pata, enquanto a sensibilidade ao calor permaneceu estável. Ao longo de cerca de um mês, essa sensibilidade mecânica elevada diminuiu, sugerindo que outras vias compensam com o tempo para restaurar o equilíbrio.
Enviando sinais para células vizinhas
RNase4 pode ser secretada para fora da célula, levantando a possibilidade de que os nociceptores influenciem fibras nervosas vizinhas e células de suporte. Em cultura celular, adicionar RNase4 a uma linha semelhante a neurônios sensoriais reduziu a atividade da via PI3K–AKT–mTOR, um centro de sinalização central para crescimento e sobrevivência. Em camundongos vivos, os autores então usaram um modelo de esmagamento do nervo ciático, que imita lesão nervosa traumática seguida por degeneração e crescimentos vindos depois. Após a lesão, os níveis de RNase4 aumentaram naturalmente em muitos subtipos de nociceptores, especialmente durante as fases iniciais de dor e recuperação. Quando RNase4 estava ausente nos nociceptores, testes comportamentais mostraram que os camundongos, na verdade, recuperaram a sensação mecânica mais rápido que os controles, embora a recuperação térmica pudesse atrasar dependendo da estratégia de deleção. Isso sugere que RNase4 normalmente restringe certos aspectos do recrescimento e da sensibilidade, e que removê-la inclina o sistema para uma recuperação tátil mais rápida.
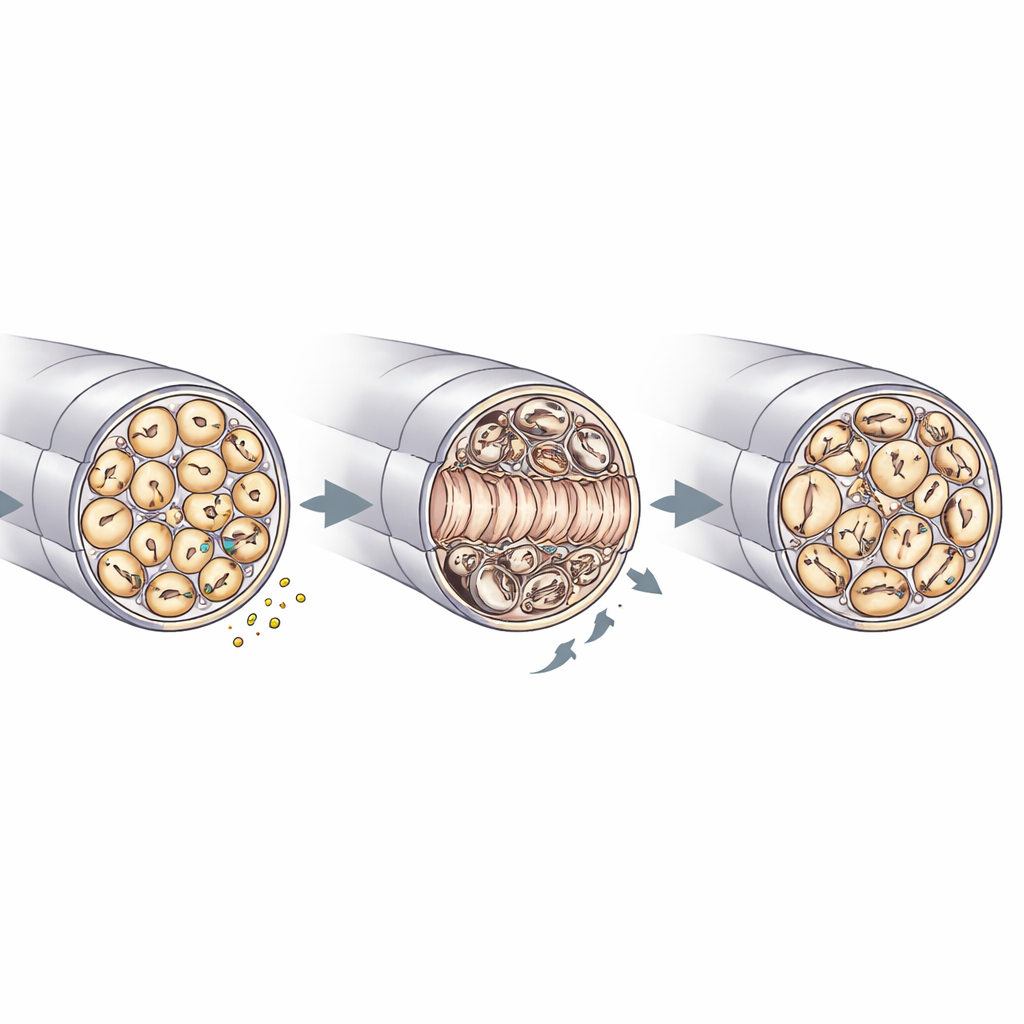
Reparo, qualidade da mielina e manutenção nervosa
A microscopia eletrônica do nervo ciático ofereceu um olhar mais detalhado sobre como RNase4 molda a arquitetura nervosa. Antes da lesão, nervos nocaute e controles pareciam semelhantes, com diâmetros axonais, densidades e espessura da mielina comparáveis. Após o esmagamento, no entanto, nervos sem RNase4 continham mais axônios regenerados no segmento danificado e mostraram um reenchimento mais rápido de feixes não mielinizados “Remak” que abrigam muitas fibras finas. Ao mesmo tempo, esses nervos nocaute exibiram mais irregularidades na mielina — como dobras, inflexões e espessamento focal — e sinais de estresse em células de Schwann, as gliais que envolvem os axônios. Havia também menos detritos de mielina dentro das células imunes, consistente com uma limpeza mais eficiente e reconstrução estrutural mais rápida. Juntamente com os estudos de sinalização, esses achados sustentam um modelo no qual a RNase4 derivada de nociceptores ajusta a atividade da PI3K–AKT e, por efeitos não locais, coordena como os axônios reganham, como a mielina é remodelada e como células imunes participam da limpeza.
O que isso significa para tratamentos futuros
Em termos simples, o estudo descreve os nociceptores não apenas como alarmes, mas como administradores locais da saúde nervosa. RNase4 atua como um freio e guia molecular: dentro dos nociceptores, ajuda a manter suas propriedades de disparo e identidade normais; fora, limita o recrescimento excessivo e molda como a mielina e as células de suporte respondem após a lesão. Remover RNase4 pode acelerar o retorno do tato após dano nervoso, mas ao custo de mais defeitos na mielina e sensibilidade dolorosa alterada. Qualquer terapia destinada a bloquear ou aumentar RNase4 precisará equilibrar esses trade-offs. Ainda assim, o trabalho destaca RNase4 e sua rede de sinalização como alavancas promissoras para modular simultaneamente a dor e promover uma reparação nervosa mais ordenada.
Citação: Feng, X., Zhang, K., Techameena, P. et al. Ribonuclease 4 Functions in Nociceptor-Mediated Nerve Homeostasis. Nat Commun 17, 2862 (2026). https://doi.org/10.1038/s41467-026-70365-8
Palavras-chave: nociceptores, regeneração nervosa, mielina, dor neuropática, RNase4